Аналитическая химия. Катионы 1 аналитической группы
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Общая характеристика катионов первой аналитической группы
К первой аналитической группе относятся катионы щелочных металлов — К + , Na + NH 4 + . Большинство солей катионов 1-ой группы представляют собой кристаллические порошки, хорошо растворимые в воде. Вследствие этого катионы 1-ой аналитической группы не имеют группового реактива и их открывают с помощью специальных дробных реакций. Открытию катионов 1-ой аналитической группы мешают катионы других групп, поэтому при проведении качественного анализа из раствора сначала необходимо удалить катионы других групп с помощью осадочных реакций.
Калий и натрий образуют сильные основания КОН и Na ОН. Их соли с сильными кислотами типа соляной, серной, азотной в воде устойчивы и не подвергаются гидролизу. Гидроксид аммония NH 4ОН – слабое основание, поэтому соли аммония с сильными кислотами в воде легко гидролизуют. Соли аммония летучи и в отличие от солей щелочных металлов легко удаляются при нагревании и прокаливании смесей солей. Эти свойством пользуются при удалении из смеси солей аммония.
Катионы 1-ой аналитической группы широко распространены в природе, являясь важными составными частями земной коры, океанов, морей, биосферы. Их соли получили широкое распространение в химии, с.х. и т.д.
Применение в медицине и фармации солей катионов 1-ой аналитической группы
Катионы калия и натрия входят в состав протоплазмы, крови, тканей и органов растений и животных. Поэтому их используют в медицине и фармации.
Хлорид натрия входит в состав физиологических растворов, кровозаменителей, широко применяется как вспомогательное средство при приготовлении таблеток, микстур. Бромид натрия, бромид калия и бромид аммония часто применяют как средства, действующие на нервную систему, регулирующие ее деятельность. Сульфат натрия используют как слабительное средство.
Гидрокарбонат натрия применяют при повышенной кислотности желудочного сока, вводят в состав кровозаменяющих растворов, ряда лекарственных веществ для регуляции рН.
Гидроксид аммония в виде 10% раствора используют при обморочных состояниях, как средство, возбуждающее при вдыхании паров деятельность дыхательных центров, для мытья рук в хирургической практике.
Хлорид аммония применяют диуретическое и отхаркивающее средство.
Катионы калия, натрия и аммония входят в состав многих лекарственных препаратов типа кислот.
Реакции катионов натрия Na +
Реакция с дигидроантимонатом калия KH 2 SbO 4
Образуется белый мелкокристаллический осадок дигидроантимоната натрия, растворимый в щелочах и кислотах. Проведению реакции мешают соли лития.
Реакция с цинкуранилацетатом HZn ( UO 2 ) 3 ( CH 3 COO ) 9 *9 H 2 O :
Образуется мелкокристаллический осадок цинкуранилацетата натрия. Осадок растворим в щелочах и кислотах. Проведению реакции мешают соли лития.
Реакция окрашивания пламени. При внесении солей натрия в пламя газовой горелки появляется желтая окраска пламени.
Реакции катионов калия К +
Реакция с гидротартратом NaHC 4 H 4 O 6 :
Образуется белый мелкокристаллический осадок гидротартрата калия, растворимый в щелочах и кислотах. Проведению реакции мешают катионы аммония
Реакция с гексанитро(3) кобальтом натрия Na 3 [ Co ( NO 2 ) 6 ]
Образующийся осадок желтого цвета растворим в кислотах и щелочах. Проведению реакции мешают катионы аммония.
Реакция с гексанитро(3) купратом свинца и натрия Na 2 Pb [ Cu ( NO 2 ) 6 ]
Образуется осадок черного цвета, растворим в кислотах и щелочах.
Реакция окрашивания пламени. При внесении солей калия в пламя окраска пламени становится фиолетовой.
Реакция со щелочами:
NH 4 Cl + NaOH → NH 4 OH + NaCl
При проведении реакции вследствие разложения образующегося гидроксида аммония на аммиак и воду появляется запах аммиака. Выделение аммиака можно определить с помощью красной лакмусовой бумажки или фенолфталеиновой бумажки, смоченной водой. При выделении аммиака лакмусовая бумажка изменяет цвет на синий,а фенолфталеиновая бумажка краснеет.
Реакция с гидротартратом натрия.
Образуется белый кристаллический осадок гидротартрата аммония, растворимый в щелочах и кислотах. Проведению реакции мешают катионы калия.
Реакция с реактивом Несслера (смесь тетрайодо(2) меркурата калия с гидроксидом калия ) K 2 [ HgI 4 ]+ KOH :
Образуется красно-бурый осадок, растворимый в кислотах и щелочах. Реакция очень чувствительна и специфична.
Реакция с гексанитро(3) кобальтом натрия Na 3 [Co(NO 2 ) 6 ]:
Образуется осадок желтого цвета, растворимый в кислотах и щелочах. Проведению реакции мешают катионы калия.
Реакция с гексанитро(3) купратом свинца и натрия Na 2 Pb[Cu(NO 2 ) 6 ]
Образуется осадок черного цвета, растворим в кислотах и щелочах. Проведению реакции мешают катионы калия.
Возгонка и разложение аммониевых солей при нагревании. При нагревании соли аммония способны возгоняться, образуя белые налеты на охлаждающем предмете.
Анализ смеси катионов первой аналитической группы.
Смесь солей, содержащих катионы 1-ой группы, растворяют в воде и проводят качественные реакции. Ввиду того, что катионы калия и аммония дают одинаковые реакции, сначала открывают ион аммония специфичными для него реакциями с реактивом Несслера и со щелочами. В присутствии катиона аммония, калий открыть нельзя, поэтому для того, чтобы открыть калий. Необходимо удалить катион аммония. Удаление проводят, упаривая часть раствора и прокаливая осадок в тигле. Охлаждают тигель и растворяют осадок в воде. Полноту удаления аммония проверяют реактивом Несслера. Открытие катиона натрия осуществляют, используя раствор цинкуранилацетата, получившиеся кристаллы рассматривают под микроскопом
Катион калия открывают реакциями с гидротартратом натрия, гексанитро(3) кобальтом натрия и гексанитро(3) купратом свинца и натрия.
Общая характеристика катионов I аналитической группы
Первая группа катионов
К первой аналитической группе относят катионы Na + , K + и NH4 + .
Соответствующие первым двум катионам элементы Na и К находятся в главной подгруппе первой группы периодической системы Д. И. Менделеева и являются s 1 — элементами. Все s 1 элементы — сильные восстановители, легко от- дают электрон, образуя катионы с зарядом + 1 и оболочкой инертного газа.
Катион NH4 + сложный ион, свойства его сходны со свойствами катиона К + , что объясняется зарядом ионов и близким значением их ионных радиусов. Сходные свойства приводят к одинаковому действию некоторых реактивов на эти ионы.
Соединения катионов Na + , K + , NH4 + , как правило, характеризуются хорошей растворимостью в воде и других полярных растворителях. Именно поэтому группа не имеет группового реактива. Только с крупными анионами катионы I группы дают труднорастворимые соединения, например, КНС4Н4О6, Na3[Со(NO2)6], K[Sb(OH)6]. Поэтому реактивы, содержащие подобные анионы, служат для обнаружения катионов I группы.
Гидроксиды калия и натрия — сильные щелочи, раствор аммиака в воде (гидроксид аммония NH4OH) — слабое основание.
Ионы Na + и К + гидролизу не подвергаются, поэтому соли этих катионов и сильных кислот имеют нейтральную реакцию раствора, а соли слабых кислот — щелочную. Катион NH4 + гидролизуется:
Следовательно, его соли, образованные сильными кислотами, имеют кислую реакцию раствора, а соли слабых кислот — нейтральную, слабокислую или слабощелочную, в зависимости от константы диссоциации слабой кислоты.
Катионы К + , Na + , NH4 + в растворе бесцветны и большинство их соединений также бесцветны, окрашенными являются соли, например, К2СrO4 (анион СrO 2- имеет желтую окраску), КМпО4 (анион МпО4 — имеет фиолетовую окраску).
Катионы I группы не проявляют способности к комплексообразованию, но могут входить во внешнюю сферу комплексных соединений.
Ионы Na + и К + имеют постоянную, устойчивую степень окисления и не участвуют в окислительно-восстановительных реакциях. Катион NH4 + может быть окислен только
очень сильными окислителями (хлорная вода, царская водка и другие) до свободного азота. Характерными реакциями этих ионов являются реакции обмена.
Соединения катионов I группы склонны к образованию пересыщенных растворов, поэтому при выполнении аналитических реакций, сопровождающихся образованием осадков, требуется тщательное перемешивание реакционной смеси. Как правило, осадки медленно кристаллизуются и имеют характерную форму кристаллов, что позволяет открывать эти ионы микрокристаллоскопическими реакциями. Для обнаружения катионов Na + и К + широко используют метод окрашивания пламени.
Реакции катиона калия К +
1. Гидротартрат натрия NaHC4H4O6(кислая соль винной кислоты) об- разует с растворами солей калия белый кристаллический осадок:
Осадок растворим в минеральных кислотах и щелочах (образование средних солей). Составьте и запишите соответствующие уравнения реакций.
Опыт.В пробирку налить 4 — 5 капель раствора соли калия (КСl, KNO3, K2SO4), прибавить равный объем гидротартрата натрия. Перемешать реакционную смесь стеклянной палочкой (если осадок не выпадает, слегка потереть ею о стенки пробирки) и охладить раствор под струей водопроводной воды. Чтобы убедиться в том, что осадок кристаллический, следует, закрыв про- бирку, сильно наклонить ее и рассмотреть прилипшие к стенкам и ко дну кристаллы КНС4Н4О6 (при подобном испытании аморфные и мелкокристаллические осадки легко отстают от стенок пробирки).
Испытать действие кислот и щелочей на осадок. Для этого, взмутив раствор, разделить его на три пробы. К первой добавить 1 — 2 капли сильной кислоты, ко второй — щелочи. К содержимому третьей пробы прибавить 2 капли дистиллированной воды и нагреть на водяной бане, осадок растворится. Он также растворяется при добавлении холодной воды. Реакция эта сравнительно малочувствительна (предельное разбавление 1:1000). На основании вышеизложенного можно сделать заключение об условиях проведения реакции. Реакцию необходимо проводить в нейтральной среде, при охлаждении и при достаточно большой концентрации ионов калия (разбавленные растворы можно предварительно упарить). Открытию катиона К + мешают ионы NH4 + , образующие с реактивом аналогичный осадок.
2. Гексанитрокобальтат(III) натрияNa3[Co(NO2)6] образует с катионом К + кристаллический желтый осадок комплексной соли гексанитро(III)кобальтата натрия-калия:
Осадок растворим в сильных кислотах (образование нестойкой кислоты Н3[Со(NO)2)6]). Присутствие щелочей мешает реакции, так как щелочь разлагая реактив, образует темно-бурый осадок Со(ОН)3.
Опыт.В пробирку налить 1 — 2 капли раствора КС1, прибавить 1 — 2 капли раствора реактива. Если осадок не выпадает, потереть стеклянной палочкой о стенки пробирки. Убедиться в том, что осадок кристаллический. Разделить осадок на две части. К первой добавить сильную кислоту до растворения осадка, ко второй — 4-5 капель уксусной кислоты СН3СООН (осадок не растворяется). Следовательно, реакцию необходимо проводить в нейтральной или слабокислой среде. Кроме того, следует учесть, что реактив должен быть свежеприготовленным, т. к. он сравнительно быстро разлагается и его бурая окраска переходит в розовую. Катион NH4 + мешает обнаружению иона К + . Реакция более чувствительная, чем первая (предельное разбавление составляет 1 : 13000).
3. Гексанитрокупрат (II) натрия-свинца Na2Pb[Cu(NO2)6]образует с катионами К + черные или коричневые кристаллы кубической формы:
Опыт А)В пробирку налить 2-3 капли раствора КС1, прибавить равный объем реактива, дать постоять и рассмотреть образовавшийся осадок.
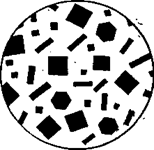
Б)Реакцию можно выполнять микрокристаллоскопическим методом. На чистое, сухое предметное стекло нанести каплю раствора соли калия, выпарить досуха, охладить и обработать каплей реактива. Через минуту рассмотреть образовавшиеся кристаллы под микроскопом (рис. 1).
Условия проведения реакции — в слабокислой или нейтральной среде (рН = 6 ÷ 7). Реакция достаточно чувствительная, обнаруживаемый минимум 7,5 мкг.
 |
2. Окрашивание пламени.Ионы К + окрашивают пламя в бледно- фиолетовый цвет.
Опыт.Платиновую или нихромовую проволочку тщательно очистить, для чего смочить ее в растворе НС1 и прокалить в пламени горелки до полного исчезновения окраски пламени. Ушком раскаленной проволочки при- коснуться к кристаллам соли калия и внести его в пламя горелки. Фиолетовое окрашивание пламени лучше наблюдать через синее стекло или флакон с раствором индиго.
Реакции катиона натрия Na +
1. Гексагидроксостибат (V) калияK[Sb(OH)6] образует с катионом Na + белый кристаллический осадок Na[Sb(OH)6]:
Осадок растворим в щелочи:
Кислоты разлагают реактив с образованием аморфного осадка метасурьмяной кислоты HSbO3:
Опыт.В пробирку налить 2 — 3 капли раствора соли NaCl, прибавить равный объем реактива, перемешать стеклянной палочкой и, если осадок не выпадает, потереть ею о стенки пробирки и охладить. Убедиться в том, что осадок кристаллический. Реакция малочувствительная, обнаруживаемый минимум — 0,3 мг. Реакция проводится в строго нейтральной среде при достаточно большой концентрации ионов Na + в растворе, при охлаждении и в отсутствии катионов NH4 + .
2. Окрашивание пламени.Соли натрия окрашивают пламя в желтый цвет. Окраска устойчивая, не исчезает в течение нескольких секунд. Реакция очень чувствительная; предел обнаружения этой реакции составляет 3 ∙ 10 -4 мкг, поэтому с ее помощью можно открывать ион Na + как примесь в реактивах. Вывод о присутствии натрия надо делать с большой осторожностью, только при очень яркой окраске пламени.
Опыт.Реакция проводится так же, как и на ион К + .
Реакции катиона аммония NH4 +
1. Щелочи NaOH и КОНпри нагревании разлагают соли аммония с вы- делением газообразного аммиака:
Опыт.В пробирку поместить 2 — 3 капли соли аммония, прибавить 1 — 2 капли раствора щелочи (не касаясь края пробирки) и нагреть. Выделение аммиака можно обнаружить по характерному запаху (специфическая реакция) или по изменению окраски влажной индикаторной бумаги, поднесенной к отверстию пробирки. Красная лакмусовая бумага синеет.
Реакция чувствительная, обнаруживаемый минимум — 0,01 мкг.
2. Реактив Несслера— раствор тетраиодомерурат (II) калия K2[HgJ4] и КОН образует с солями аммония красно-бурый аморфный осадок иодида оксодимеркурат (II) аммония [NH2Hg2O]J:
Опыт.К капле разбавленного раствора соли аммония на предметном стекле (или в пробирке) добавить 1-2 капли реактива Несслера. Наблюдать выпадение осадка.
Реакция очень чувствительная (обнаруживаемый минимум — 0,25 мкг).
Условия проведения опыта: при выполнении опыта необходимо брать избыток реактива Несслера, так как осадок растворим в солях аммония; открытию катиона NH4 + мешают катионы Fe 3+ , Cr 3+ , Co 2+ , Ni 2+ и другие, образующие окрашенные осадки с КОН.
В табл.1 представлены результаты действия некоторых реагентов на катионы I группы.
Частные реакции катионов первой аналитической группы
Читайте также:
|
| Ион | Реагент | Условия проведения реакции | Уравнение реакции в молекулярном и ионном виде | Внешний эффект реакции | Вывод |
Реакции обнаружения катиона калия К +
1. Гидротартрат натрия NaHC4H4O6,или винная кислота,в присутствии ацетата натрия при достаточной концентрации ионов калия К + в растворе дает белый кристаллический осадок гидротартрата калия:
Осадок растворяется в сильных кислотах и щелочах, поэтому реакцию проводят в нейтральной или слабокислой средах:
Реакцию следует проводить при охлаждении под струей водопроводной воды, так как растворимость осадка гидротартрата калия КНС4Н4О6 повышается при увеличении температуры.
Для ускорения выпадения осадка стенки пробирки потирают стеклянной палочкой для образования центров кристаллизации.
Реакция протекает при больших концентрациях ионов калия К + и является малочувствительной. Ионы аммония NH + 4 мешают определению ионов калия К + из-за того, что тоже дают белый кристаллический осадок с этими реагентами и поэтому соли аммония предварительно разлагают при нагревании.
Реакция является фармакопейной.
2. Гексанитрокобальтат (III) натрия Na3[Co(NO2)6] в нейтральном или слабокислом растворе с ионом калия К + дает желтый кристаллический осадок гексанитрокобальтата (III) калия-натрия:
В щелочной среде реакцию обнаружения К + проводить нельзя, так как в этой среде гексанитрокобальтат (III) натрия разлагается с образованием гидроксида кобальта (III) бурого цвета:
В сильных кислотах осадок K2Na[Co(NO2)6] растворяется с образованием нестойкой кислоты гексанитрокобальтата (III) водорода H3[Co(NO2)6].
Реакцию обнаружения ионов калия следует проводить в отсутствии ионов NH4 , так как последние дают аналогичный осадок с Na3[Co(NO2)6]. Рассматриваемая реакция обнаружения иона калия более чувствительна, чем реакция с гидротартратом натрия и является также фармакопейной.
3. Окрашивание пламени. При выполнении этой реакции платиновую проволочку, впаянную в стеклянную палочку, смачивают хлороводородной кислотой и вносят в бесцветное пламя горелки. Прокаливают до тех пор, пока окрашивание пламени не прекратится. Затем раскаленной проволокой касаются мелкого порошка или опускают ее в раствор соли калия и снова вносят в бесцветное пламя горелки. Если в образце или растворе присутствуют ионы калия, то пламя горелки окрашивается в фиолетовый цвет. Присутствие ничтожных следов натрия, окрашивающего пламя в желтый цвет, маскирует окраску.
Эта реакция используется при анализе фармацевтических препаратов.
Реакции обнаружения катиона натрия Na +
1. Гексагидроксостибиат калия K[Sb(OH)6] образует с ионом натрия белый кристаллический осадок гексагидроксостибиат (V) натрия:
Обнаружение иона Na + с помощью гексагидроксостибиата (V) калия проводят в нейтральном или слабощелочном растворе, так как кислоты разлагают реагент:
образуя белый аморфный осадок метасурьмяной кислоты. Щелочи растворяют осадок Na[Sb(OH)6] с образованием хорошо растворимой средней соли:
Соли аммония, дающие в результате гидролиза кислую реакцию среды, также разлагают исходный реактив с образованием метасурьмяной кислоты. Поэтому добиваются отсутствия в растворе ионов NH + 4 до определения в нем ионов К + .
Для образования центров кристаллизации и скорейшего выпадения осадка гексагидроксостибиата (V) натрия реакцию проводят при охлаждении и потирают стенки пробирки стеклянной палочкой.
2. Микрокристаллоскопическая реакция. Ацетат уранила UO2(CH3COO)2 образует в уксуснокислой среде с солями натрия желтоватые кристаллы уранилацетата натрия Na[(UO2)(CH3COO)3]:
При выполнении реакции раствор соли натрия выпаривают досуха и обрабатывают ацетатом уранила. Выпавшие кристаллы имеют форму желтоватых тетраэдров (или октаэдров) под микроскопом ( рис. 8.1).
Рис. 8.1. Кристаллы уранилацетата натрия
Реакция используется в фармакопее.
3. Окрашивание пламени. Соли натрия окрашивают бесцветное пламя горелки в желтый цвет. Реакция очень характерна и является фармакопейной.
Установить присутствие натрия в исследуемом веществе по окрашиванию бесцветного пламени можно только тогда, когда желтая окраска пламени сохраняется 25-30 с.
Реакции обнаружения катиона аммония NH + 4
1. Щелочи NaOH и КОН разрушают аммонийные соли с выделением аммиака:
Выделяющийся аммиак можно обнаружить с помощью влажной красной или фиолетовой лакмусовой бумажки. Образующиеся по реакции
гидроксид-ионы ОН — изменяют окраску лакмуса в синий цвет. Подобную реакцию можно провести в газовой камере (см. рис. 7.8). При большой концентрации выделяющегося аммиака его можно обнаружить и по запаху. Реакция фармакопейная.
2. Реактив Несслера (смесь K2[HgI4] и КОН). Этот реактив дает с аммонийными солями красно-бурый осадок:
При очень малых количествах солей аммония вместо осадка образуется желтый раствор; при большом их количестве — осадок растворяется. Реакция очень чувствительна. Ионы калия и натрия не мешают определению ионов аммония.
Дата добавления: 2014-11-13 ; просмотров: 58 ; Нарушение авторских прав
http://poisk-ru.ru/s8148t13.html
http://lektsii.com/1-6402.html



