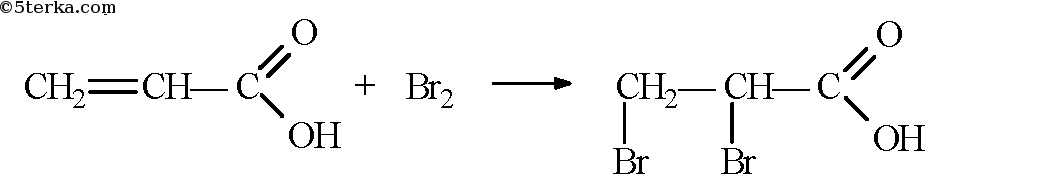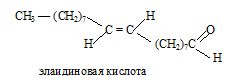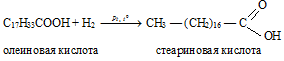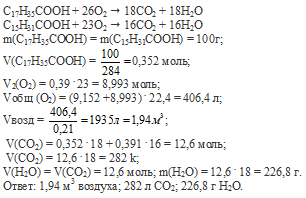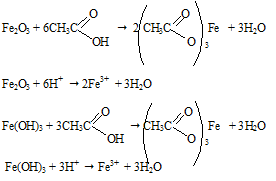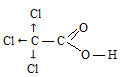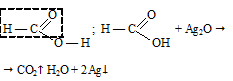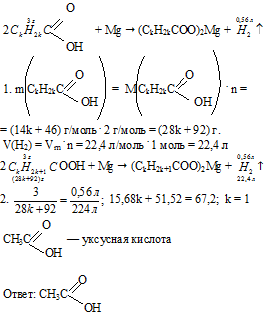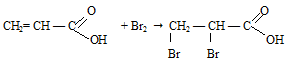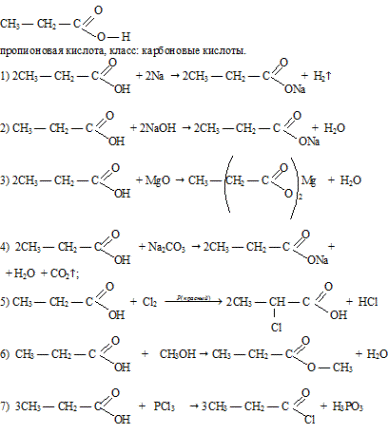12. Предложите несложный лабораторный способ, с помощью которого можно распознать пропановую и акриловую кислоты.
Даже в отсутствие катализатора акриловая кислота обесцвечивает бромную воду.
Пропионовая кислота в подобных условиях не реагирует с бромом.

задача №12
к главе «Глава 4. Кислородсодержащие соединения. § 20. Карбоновые кислоты».
Строение и свойства карбоновых кислот
Непредельные карбоновые кислоты
Вопрос 1.
Элаидиновая кислота (транс-9-октадеценовая кислота)
Сокращенная структурная формула элаидиновой кислоты:
Структурная формула элаидиновой кислоты:
Жирные карбоновы кислоты
Вопрос 2.
В результате реакции гидрирования олеиновой кислоты получается стеариновая кислота:
Вопрос 3.
Вопрос 4.
Вопрос 5.
Свойства и применение карбоновых кислот
Вопрос 6.
Если обработать раствором кислоты пятно ржавчины, то оно исчезает, так как происходит химическая реакция, ржавчина превращается в растворимый ацетат железа (III), а с водой ни Fe2O3, ни Fe(OH)3 не реагируют, поэтому пятна не удаляются.
Вопрос 7.
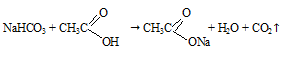
Образование пены можно объяснить бурным выделением пузырьков углекислого газа, выделяющегося при реакции кислоты и соды.
Вопрос 8.
Это можно объяснить строением молекул.
Атомы хлора, как более электроотрицательные, по сравнению с атомами углерода, кислорода и водорода, оттягивают электронную плотность на себя, тем самым не позволяя радикалу компенсировать недостаток электронной плотности на атоме углерода, входящему в состав карбоксильной группы, вследствие чего связь О—Н более полярна.
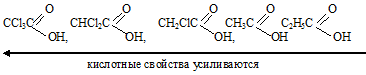
Так как в состав последующих кислот входит меньшее количество атомов хлора, следовательно, связи
О—Н в них менее полярны и кислоты с уменьшением количества атомов хлора становятся слабее:
Пропионовая кислота слабее этановой, так как радикал C2H5 — обладает большим +I эффектом, чем СН3 —, т. е. больше отталкивает от себя электронную плотность и связь O—H становится менее полярна по сравнению с таковой в этановой кислоте.
Вопрос 9.
Так как в молекуле муравьиной кислоты отсутствует углеводородный радикал и присутствует альдегидная группа, то она вступает в «реакцию серебряного зеркала»:
В результате реакции выделяется углекислый газ.
Вопрос 10.
Характерным признаком произошедшей реакции является изменение окраски осадка: был голубой осадок Cu(OH)2, а выпал красный осадок Cu2O.
Вопрос 11.
Вопрос 12.
Даже в отсутствие катализатора акриловая кислота обесцвечивает бромную воду:
Пропионовая кислота в обычных условиях не реагирует с бромом.
Вопрос 13.
Вопрос 14.
Вопрос 15.
Веществом «А» является:
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. источники: http://buzani.ru/khimiya/o-s-gabrielyan-10kl/619-glava-4-kislorodsoderzhashchie-soedineniya-20 http://acetyl.ru/o/a31k2b3b.php |