Свойства алкинов
Свойства алкинов – физические и химические похожи на свойства алкенов и алкадиенов. Однако кислотные свойства алкинов создают ряд отличительных химических свойств.
Физические свойства алкинов
Алкины, за исключением ацетилена, не имеют цвета и запаха. При нормальных условиях первые 4 члена ряда являются газами, с 5 по 15 – жидкостями, более 15 – твердыми веществами.
Растворимость алкинов
Алкины являются относительно полярными молекулами, поэтому хорошо растворимы в полярных растворителях или растворителях с низкой полярностью. В воде алкины растворяются незначительно, но лучше, чем алканы и алкены.
Точки плавления и кипения алкинов
Как правило, алкины плавятся и кипят при более высоких температурах, по сравнению соответствующих алканов и алкенов. Температуры плавления и кипения алкинов, увеличиваются пропорционально их молекулярной массе.
В таблице приведены физические постоянные некоторых алкинов:
Химические свойства алкинов
В общем алкины более реакционноспособны, чем алканы и алкены. Большинство реакций, в которых они участвуют являются реакциями электрофильного присоединения. Однако терминальные алкины (тройная связь находится в конце цепи) также подвергаются и реакциям замещения. Атомы водорода при sp-гибридизованном атоме углерода способны подвергаться протонизации, вследствие чего алкины имеют относительно кислую природу.
Реакции электрофильного присоединения (реакции тройной углерод-углеродной связи)
1) Гидрирование алкинов. В присутствии активных катализаторов (никель, платина) восстанавление алкинов водородом происходит сразу до алканов. При использовании менее активных катализаторов (Pd, железо Ренея) реакция протекает через стадию образования алкена:
При гидрировании гомологов ацетилена на первой стадии получаются цис-олефины.
2) Галогенирование алкинов протекает в две легко разделимые стадии, из которых первая стадия протекает более энергично. При недостатке галогена реакция идет в одну стадию, при избытке – две стадии:
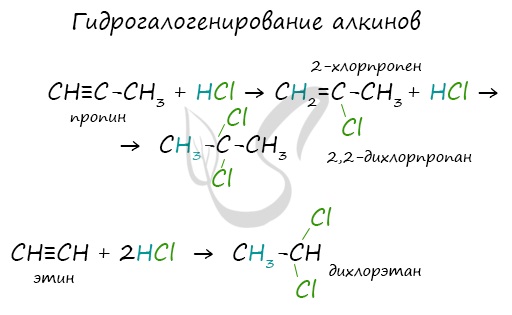
3) Гидрогалогенирование алкинов также протекает в две разделимые стадии. При гидрохлорировании ацетилена на первоначальном этапе образуется важный в промышленности продукт – хлористый винил, далее происходит образование 1,1-дихлорэтан:
Присоединение молекулы HCl к хлористому винилу происходит по правилу Марковникова. Аналогичным образом присоединяется молекула HBr.
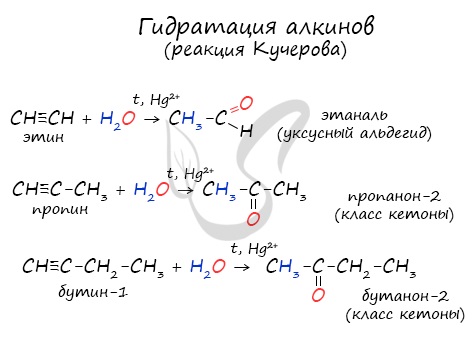
4) Гидратация алкинов происходит согласно правилу Марковникова с участием Hg 2+ в качестве катализатора (реакция Кучерова). В ходе такой реакции, из ацетилена образуется ацетальдегид, а из его гомологов — кетоны: 5) Присоединение спиртов и меркаптанов. При воздействии едкого кали ацетилен и монозамещенные ацетилены под давлением присоединяют спирты, образуя акрилвиниловые эфиры (Реппе, Фаворский А.Е., М.Ф. Шоствковский):
Подобным образом происходит присоединение меркаптанов.
6) Присоединение кислот.
Присоединение уксусной кислоты к ацетилену происходит в условиях гетерогенного катализа (H3PO4 или B2O3) с образованием винилацетата:
Винилацетат хорошо полимеризуется с образованием поливинилацетата (ПВА):
Присоединение синильной кислоты к ацетилену происходит с образованием акрилонитрила:
Акрилонитрил используют для получения полиакрилонитрила: 7) Присоединение хлоридов некоторых металлов к ацетилену:
8) Реакции полимеризации
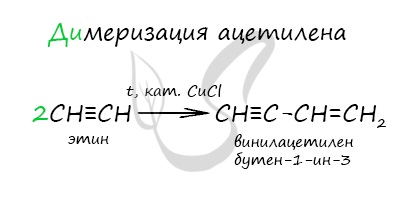
Димеризация ацетилена происходит в присутствии солей Cu (I) с образованием винилацетилена. Дальнейшее его взаимодействие с соляной кислотой приводит к образованию хлоропрена, который используют при получении хлоропреновых каучуков:
А.Д. Петров путем кросс-димеризации ацетилена получил изобутилен. В качестве катализаторов выступает никель в присутствии хлорида цинка:
Тримеризация ацетилена в присутствии активного угля и при температуре около 600°С ведет к образованию такого важного продукта, как бензол (реакция Зелинского):
Ученый Шеффер в 1966 г обнаружил, что при пропускании над хлоридом алюминия раствора диметилацетилена в бензоле, последний тримеризуется. Продуктом реакции является гексаметилбицикло[2,2,0]гексадиен (гексаметилдьюаровский бензол), который далее при при воздействии температуры подвергается изомеризации в гексаметилбензолПри использовании в качестве катализатора димезитиленкобальта гексаметилбензол получается непосредственно из диметилацетилена:
Тетрамеризация ацетилена под действием комплексных солей никеля ведет к образованию циклоокта-1,3,5,7-тетраена (синтез Реппе):
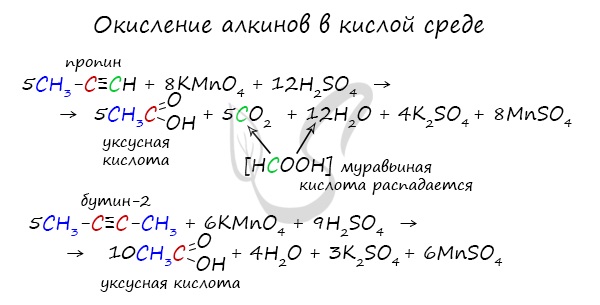
10) Окисление алкинов концентрированным раствором перманганата калия (KMnO4) в кислой среде протекает с образованием карбоновых кислот. Розовый раствор KMnO4 в ходе реакции обесцвечивается:
Окисление алкинов в мягких условиях, т.е. разбавленный раствор KMnO4, комнатная температура, происходит без разрыва связей. При окислении ацетилена продуктом реакции является щавелевая кислота, при окислении его гомологов в нейтральной среде реакцию можно остановить на стадии образования дикетонов:
При горении алкинов происходит их полное окисление до углекислого газа и воды. Реакция экзотермическая и протекает с выделением 1300 кДж/моль тепла:
Реакции замещения водородных атомов ацетилена
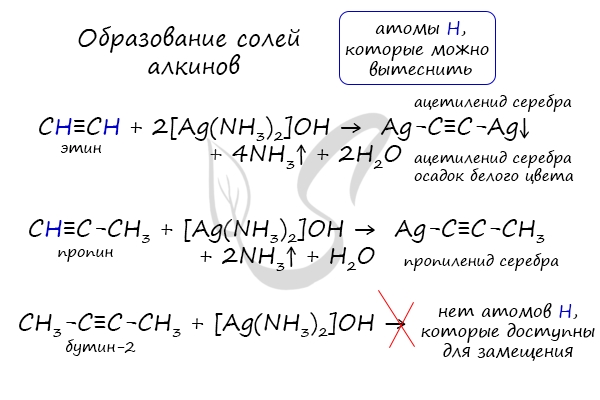
1) Взаимодействие с солями тяжелых металлов (качественная реакция). При взаимодействии ацетилена и монозамещенных гомологов с аммиачными растворами окиси серебра или полухлористой меди обрадуются нерастворимые осадки ацетиленидов:
Ацетилинид серебра Ag-C≡C-Ag – бесцветный и R-C≡C-Ag — белый
Ацетилинид меди Cu-C≡C-Cu – вишнево-бурый и R-C≡C-Cu – желто-бурый
Ацетилениды – взрывчатые вещества. Под действием кислот разлагаются с образованием ацетилена и соответствующих солей металлов.
2) Взаимодействие ацетилена и его гомологов с щелочными и щелочноземельными металлами в жидком аммиаке также приводит к образованию ацетилинидов:
Действие производных Na и Mg, известных как реактив Иоцича, подобно реактиву Греньяра, поэтому широко используются в органическом синтезе.
3) Взаимодействие ацетилена и его гомологов с кетонами в присутствии едкого кали, под небольшим давлением (А.Е. Фаворский): 4) Взаимодействие ацетилена и его гомологов с альдегидами в присутствии ацетилинида меди (Реппе):
5) Ацетилен-аллен-диеновая перегруппировка Фаворского происходит при нагревании ацетиленов с металлическим натрием. При этом расположенная «внутри» соединения тройная связь перемещается в конец. А при нагревании ацетиленов с расположенной в конце тройной связью со спиртовым раствором щелочи происходит перемещение тройной связи к центру молекулы:
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
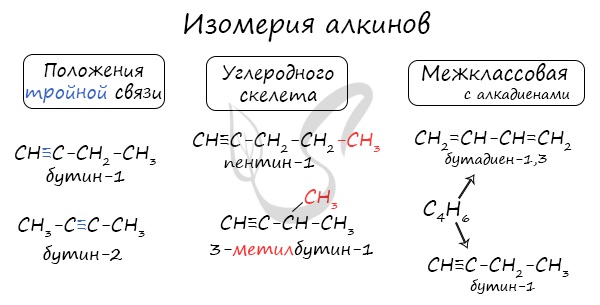
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. АлкиныАлкины — непредельные (ненасыщенные) углеводороды, имеющие в молекуле одну тройную связь С≡С. Каждая такая связь содержит одну сигма-связь (σ-связь) и две пи-связи (π-связи). Алкины также называют ацетиленовыми углеводородами. Первый член гомологического ряда — этин — CH≡CH (ацетилен). Общая формула их гомологического ряда — CnH2n-2. Номенклатура и изомерия алкиновНазвания алкинов формируются путем добавления суффикса «ин» к названию алкана с соответствующим числом: этин, пропин, бутин и т.д. При составлении названия алкина важно учесть, что главная цепь атомов углерода должна обязательно содержать тройную связь. Нумерация атомов углерода в ней начинается с того края, к которому ближе тройная связь. В конце названия указывают атом углерода у которых начинается тройная связь. Для алкинов характерна изомерия углеродного скелета, положения тройной связи, межклассовая изомерия с алкадиенами. Пространственная геометрическая изомерия для них невозможна, ввиду того, что каждый атом углерода, прилежащий к тройной связи, соединен только с одним единственным заместителем. Некоторые данные, касающиеся алкинов, надо выучить:
Получение алкиновАцетилен получают несколькими способами:
При нагревании метана до 1200-1500 °C происходит димеризация молекул метана, в ходе чего отщепляется водород. Осуществляется напрямую, из простых веществ. Протекает на вольтовой (электрической) дуге, в атмосфере водорода. 2C + H2 → (t, вольтова дуга) CH≡CH Разложение карбида кальция В результате разложения карбида кальция образуется ацетилен и гидроксид кальция II. Получение гомологов ацетилена возможно в реакциях дегидрогалогенирования дигалогеналканов, в которых атомы галогена расположены у одного атома углерода или у двух соседних атомов. Химические свойства алкиновАлкины — ненасыщенные углеводороды, легко вступающие в реакции присоединения. Реакции замещения для них не характерны. Водород присоединяется к атомам углерода, образующим тройную связь. Пи-связи (π-связи) рвутся, остается единичная сигма-связь (σ-связь). CH≡C-CH3 + H2 → (t, Ni) CH2=CH-CH3 (в реакции участвует 1 моль водорода) CH≡CH + 2H2 → (t, Ni) CH3-CH3 (в реакции участвует 2 моль водорода) Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение его по кратным связям к органическому веществу. Алкины вступают в реакции гидрогалогенирования, протекающие по типу присоединения. Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена — к наименее гидрированному атому углерода. Реакцией Кучерова называют гидратацию ацетиленовых соединений с образованием карбонильных соединений. Открыта русским химиком М.Г. Кучеровым в 1881 году. Катализатор — соли ртути Hg 2+ . Только в реакции с ацетиленом образуется уксусный альдегид. Во всех остальных реакциях (с гомологами ацетилена) образуются кетоны. При горении алкины, как и все органические соединения, сгорают с образование углекислого газа и воды — полное окисление. Сильные окислители (особенно в подкисленной среде) способны разрывать молекулы алкинов в самом слабом месте — в месте тройной связи. Так, при окислении пропина, образуется уксусная кислота и муравьиная кислота, окисляющаяся до угольной кислоты, которая распадается на углекислый газ и воду. Данная реакция протекает при пропускании ацетилена над активированным углем при t = 400°C. В результате образуется ароматический углеводород — бензол. Димеризация ацетилена происходит при наличии катализатора — солей меди I. В результате реакции две молекулы ацетилена соединяются, образуя винилацетилен. В случае если тройная связь прилежит к краевому атому углерода, то имеющийся у данного атома водород может быть замещен атомом металла. Если тройная связь спрятана внутри молекулы, то образование солей невозможно. Реакция аммиачного раствора серебра и ацетилена — качественная реакция, в ходе которой выпадает осадок ацетиленида серебра. © Беллевич Юрий Сергеевич 2018-2022 Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию. источники: http://acetyl.ru/o/a21d2d.php http://studarium.ru/article/185 |