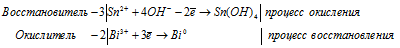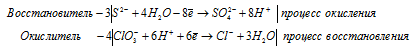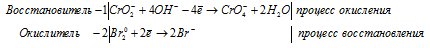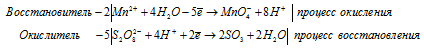Составление уравнений окислительно-восстановительного процесса в молекулярной и ионной форме
Задача 640.
Закончить уравнения реакций, записать их в ионно-молекулярной форме:
а) BiCl3 + SnCl2 + KOH → Bi +
б) NaClO3 + H2S → H2SO4 +
в) KCrO2 + Br2 + KOH →
г) MnSO4 + (NH4)2S2O8 + H2SO4 → HMnO4 +
Решение:
а) BiCl3 + SnCl2 + KOH → Bi +
Ионно-молекулярная форма процесса:
2Bi 3+ + 3Sn 2+ + 12OH — = 3Sn(OH)4 + 2Bi 0
Молекулярная форма будет иметь вид:
2BiCl3 + 3SnCl2 +12KOH = Bi + 3Sn(OH)4 + 12KCl.
2Bi 3+ + 3Sn 2+ + 12OH — + 12Cl — + 12K + = 3Sn(OH)4 + 2Bi 0 + 12K + + 12Cl — .
Сокращенная ионно-молекулярная форма процесса:
2Bi 3+ + 3Sn 2+ + 12OH — = 3Sn(OH)4 + 2Bi 0 .
Ионно-молекулярная форма процесса:
3S 2- + 4ClO3 — + 12H2O + 24H + = 4Cl — + 3SO4 2- + 12H2O + 24H +
После приведения членов в обеих частях равенства получим молекулярную форму:
4Na + + 4ClO3 — + 6H + + 3S 2- = 6H + + 3SO4 2- + 4Na + + 4Cl — .
Сокращённая ионно-молекулярная форма:
в) KCrO2 + Br2 + KOH →
Ионно-молекулярная форма процесса:
Молекулярная форма процесса:
5K + + CrO2 — + 2Br2 0 + 4OH — = 5K + + 4Br — + CrO4 — + 2H2O.
Сокращённая ионно-молекулярная форма:
Ионно-молекулярная форма процесса:
После приведения членов в обеих частях равенства получим:
Молекулярная форма процесса:
Для уравнивания атомов водорода и группы SO4 добавим в левую часть равенства одну молекулу H2SO4, получим:
bi(no3)3+sncl2+koh=k2[sn(oh)6]+bi+kno3+kkl Электронно ионный баланс
2 Bi(NO3)3 + 3 SnCl2 + 18 KOH = 3 K2[Sn(OH)6] + 6 KNO3 + 6 KCl + 2 Bi
2Bi(NO3)3+3SnCl2+18KOH=3K2[Sn(OH)6]+2Bi+6KNO3+6KCl
Электронно-ионный баланс (метод «полуреакций»):
Bi(3+) + 3e = Bi(0)—————————x2 восстановление, окислитель
Sn(2+) + 6OH(-) — 2e = [Sn(OH)6](2+)—!x3 окисление, восстановитель
Подобрать коэффициенты электронно-ионным методом (методом полуреакций) и рассчитать молярные массы эквивалентов в следующих реакциях: SnCl2 + BiCl3 + KOH → K2SnО3 + KCl + H2О + Bi






Чтобы получить решение , напишите мне в WhatsApp , оплатите, и я Вам вышлю файлы.
Кстати, если эта работа не по вашей теме или не по вашим данным , не расстраивайтесь, напишите мне в WhatsApp и закажите у меня новую работу , я смогу выполнить её в срок 1-3 дня!
Описание и исходные данные задания, 50% решения + фотография:
Подобрать коэффициенты электронно-ионным методом (методом полуреакций) и рассчитать молярные массы эквивалентов окислителя и восстановителя в следующих реакциях:
Решение :
3| Sn 2+ + OH — -2 e = SnO 3 2- + H 2 O
| Если вам нужно решить химию, тогда нажмите ➔ заказать контрольную работу по химии. |
| Похожие готовые решения: |
- Какой тип гибридизации орбиталей центрального атома наиболее вероятен для молекул NH3, CH4, H2O, BH3, BeH2?
- Вычислить концентрацию ионов Ni2+ в 0,1 М растворе K2[Ni(CN)4]. Kнест.([Ni(CN)4] 2– )=1•10–22 .
- Определить концентрацию иодид-ионов в насыщенном растворе PbI2. ПР (PbI2) см. в приложении.
- Используя справочные материалы, составить уравнения окислительно-восстановительных реакций: KMnO4 + K4[Fe(CN)6] + H2SO4 →
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.
http://sprashivalka.com/tqa/q/27866162
http://natalibrilenova.ru/podobrat-koeffitsientyi-elektronno-ionnyim-metodom-metodom-polureaktsij-i-rasschitat-molyarnyie-massyi-ekvivalentov-v-sleduyuschih-reaktsiyah-sncl2—bicl3—koh—k2sno3—kcl—h2o—bi-/