БИОСИНТЕЗ НАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ
В настоящее время в достаточной степени изучен механизм биосинтеза жирных кислот в организме животных и человека, а также катализирующие этот процесс ферментные системы. Синтез жирных кислот протекает в цитоплазме клетки. В митохондриях в основном происходит удлинение существующих цепей жирных кислот. Установлено, что в цитоплазме печеночных клеток синтезируется пальмитиновая кислота (16 углеродных атомов), а в митохондриях этих клеток из уже синтезированной в цитоплазме клетки пальмитиновой кислоты или из жирных кислот экзогенного происхождения, т.е. поступающих из кишечника, образуются жирные кислоты, содержащие 18, 20 и 22 углеродных атома.
Иными словами, митохондриальная система биосинтеза жирных кислот, включающая несколько модифицированную последовательность реакций β-окисления, осуществляет только удлинение существующих в организме среднецепочечных жирных кислот, в то время как полный биосинтез пальмитиновой кислоты из ацетил-КоА активно протекает в цитозоле, т.е. вне митохондрий, по совершенно другому пути.
Внемитохондриальная система биосинтеза de novo жирных кислот (ли-погенез). Эта система находится в растворимой (цитозольной) фракции клеток многих органов, в частности печени, почек, мозга, легких, молочной железы, а также в жировой ткани. Биосинтез жирных кислот протекает с участием НАДФН, АТФ, Мn 2+ и НСО3 – (в качестве источника СО2); субстратом является ацетил-КоА, конечным продуктом – пальмитиновая кислота. Потребности в кофакторах процессов биосинтеза и β-окисления жирных кислот значительно различаются.
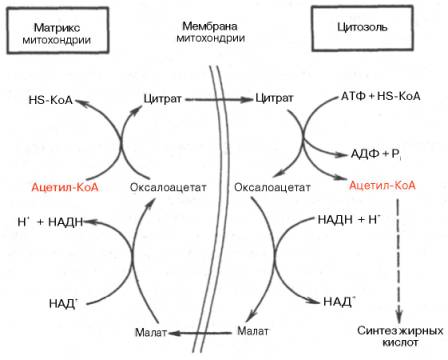
Как отмечалось, строительным блоком для синтеза жирных кислот в цитозоле клетки служит ацетил-КоА, который в основном поступает из митохондрий. Было выявлено, что цитрат стимулирует синтез жирных кислот в цитозоле клетки. Известно также, что образующийся в митохондриях в процессе окислительного декарбоксилирования пирувата и окисления жирных кислот ацетил-КоА не может диффундировать в цитозоль клетки, так как митохондриальная мембрана непроницаема для данного субстрата. Поэтому вначале внутримитохондриальный ацетил-КоА взаимодействует с оксалоацетатом, в результате чего образуется цитрат. Реакция катализируется ферментом цитрат-синтазой. Образовавшийся цитрат переносится через мембрану митохондрий в цитозоль при помощи специальной трикарбоксилаттранспортирующей системы.
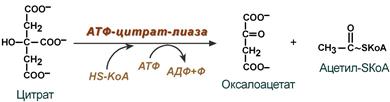
В цитозоле цитрат реагирует с HS-KoA и АТФ, вновь распадаясь на ацетил-КоА и оксалоацетат. Эта реакция катализируется АТФ-цитратлиазой. Уже в цитозоле оксалоацетат при участии цитозольной малатдегидрогеназы восстанавливается до малата. Последний при помощи дикарбокси-латтранспортирующей системы возвращается в митохондриальный матрикс, где окисляется до оксалоацетата, завершая тем самым так называемый челночный цикл:
Существует еще один путь переноса внутримитохондриального аце-тил-КоА в цитозоль клетки – с участием карнитина. Как отмечалось, кар-нитин играет роль переносчика ацильных групп из цитозоля в митохондрии при окислении жирных кислот. По-видимому, он может выполнять эту роль и в обратном процессе, т.е. в переносе ацильных радикалов, в том числе ацетильного радикала, из митохондрий в цитозоль клетки. Однако, когда речь идет о синтезе жирных кислот, данный путь переноса ацетил-КоА не является главным.
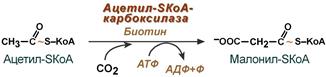
Образование малонил-КоА. Первой реакцией биосинтеза жирных кислот является карбоксилирование ацетил-КоА, для чего требуются бикарбонат, АТФ, ионы марганца. Катализирует эту реакцию фермент ацетил-КоА-карбоксилаза. Фермент содержит в качестве простетической группы биотин. Авидин – ингибитор биотина угнетает эту реакцию, как и синтез жирных кислот в целом.
Установлено, что ацетил-КоА-карбоксилаза состоит из переменного числа одинаковых субъединиц, каждая из которых содержит биотин, биотинкарбоксилазу, карбоксибиотинпереносящий белок, транскарбоксилазу, а также регуляторный ал-лостерический центр, т.е. представляет собой полиферментный комплекс.
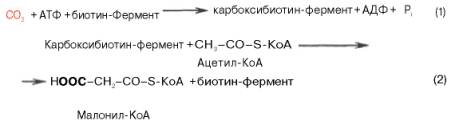
Реакция протекает в два этапа: I – карбоксилирование биотина с участием АТФ и II – перенос карбоксильной группы на ацетил-КоА, в результате чего образуется малонил-КоА:
Малонил-КоА представляет собой первый специфический продукт биосинтеза жирных кислот. В присутствии соответствующей ферментной системы малонил-КоА быстро превращается в жирные кислоты.
Энзиматические системы, осуществляющие синтез жирных кислот, называются жирно-кислотными синтетазами. Они широко встречаются в природе и могут быть изолированы из различных одноклеточных организмов, растений и животных тканей.
Жирно-кислотные синтетазы делятся на 2 группы. К первой группе относятся полиэнзимные, не поддающиеся фракционированию комплексы с мол. м. порядка 500000, в которых все индивидуальные энзимы собраны в компактную структуру. В частности, в эту группу входят жирно-кислотные синтетазы животных тканей и дрожжей.
Вторая группа включает жирно-кислотные синтетазы, из которых отдельные энзимы могут быть выделены методами белкового фракционирования. Такие синтетазы встречаются у ряда микроорганизмов (в частности, у E.coli) и растений. Иными словами, в этих случаях все индивидуальные ферменты синтетазной системы находятся в виде автономных полипептидов.
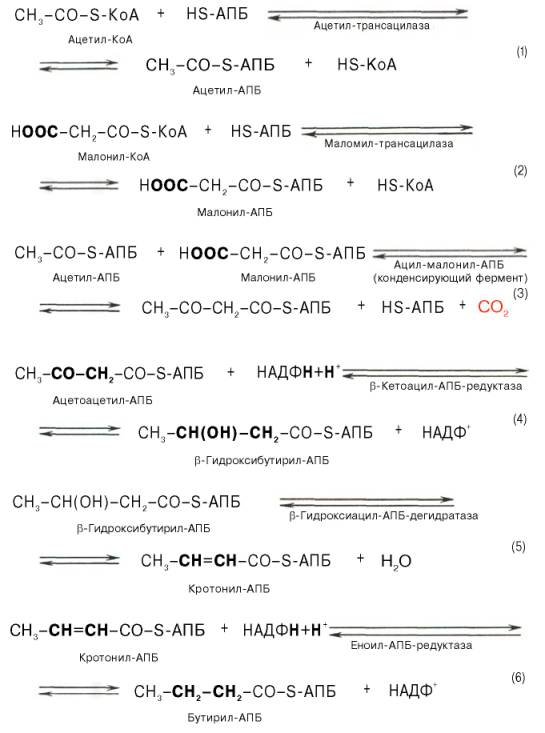
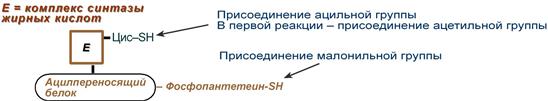
Мультиферментный комплекс, называемый синтетазой (синтазой) жирных кислот, состоит из 6 ферментов, связанных с так называемым ацилпереносящим белком (АПБ). Этот белок относительно термостабилен, имеет две свободные HS-группы (цистеина и фосфопантетеинового остатка, присоединенного к ОН-группе серина) и вовлекается в процесс синтеза высших жирных кислот практически на всех его этапах. Мол. масса АПБ составляет около 10000. Данный белок в синтетазной системе выполняет роль КоА. Заметим, что в животных тканях не удалось обнаружить свободного АПБ, подобного микробному. Из печени выделен полиэнзимный комплекс, содержащий все энзимы, необходимые для синтеза жирных кислот. Энзимы комплекса настолько прочно связаны друг с другом, что все попытки изолировать их в индивидуальном виде не увенчались успехом. Приводим последовательность реакций, происходящих при синтезе жирных кислот:
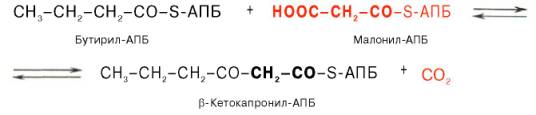
Далее цикл реакций повторяется. Допустим, что идет синтез пальмитиновой кислоты (С16). В этом случае образованием бутирил-АПБ завершается лишь первый из 7 циклов, в каждом из которых началом является присоединение молекулы малонил-АПБ к карбоксильному концу растущей цепи жирной кислоты. При этом отщепляется дистальная карбоксильная группа малонил-АПБ в виде СО2. Например, образовавшийся в первом цикле бутирил-АПБ взаимодействует с малонил-АПБ:
Завершается синтез жирной кислоты отщеплением HS-АПБ от ацил-АПБ под влиянием фермента деацилазы. Например:
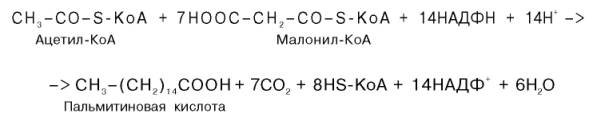
Суммарное уравнение синтеза пальмитиновой кислоты можно записать так:
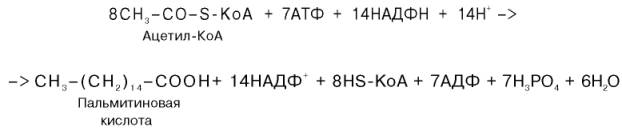
Или, учитывая, что на образование одной молекулы малонил-КоА из ацетил-КоА расходуются одна молекула АТФ и одна молекула СО2, которая затем отщепляется, суммарное уравнение можно представить в следующем виде:
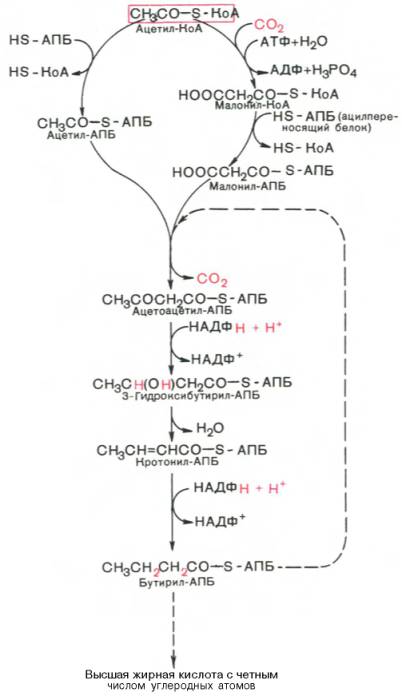
Основные этапы биосинтеза жирных кислот можно представить в виде схемы:
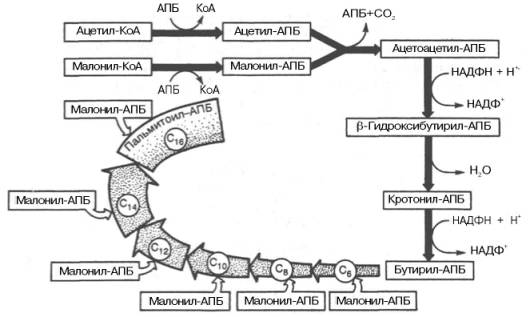
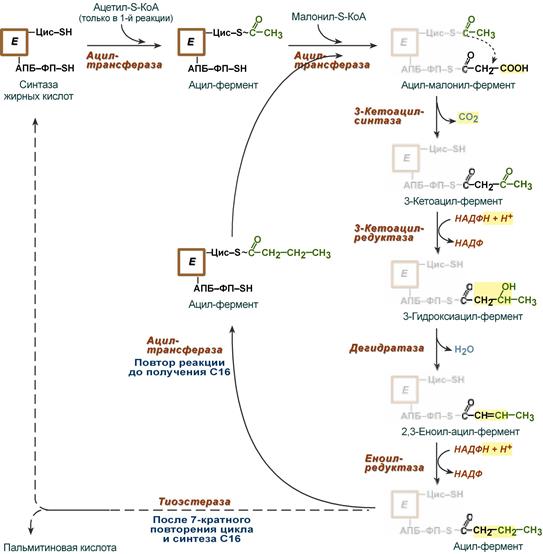
В общем виде синтез жирных кислот у кишечной палочки представлен на рис. 11.4. Последовательность и характер реакций в синтезе жирных кислот, начиная с образования β-кетоацил-АПБ (на рис. 11.4 – ацетоацетил-АПБ) и кончая завершением одного цикла удлинения цепи на два углеродных атома, являются как бы обратными реакциями окисления жирных кислот. На самом деле пути синтеза и окисления жирных кислот не пересекаются даже частично. Это становится очевидным, если принять во внимание некоторые особенности синтеза и окисления жирных кислот.
Рис. 11.4. Синтез пальмитиновой кислоты у кишечной палочки при участии одной молекулы ацетил-КоА и 7 молекул малонил-КоА. Подробно представлен первый цикл синтеза — образование бутирил-АПБ. Остальные 6 циклов аналогичны первому.
По сравнению с β-окислением биосинтез жирных кислот имеет ряд характерных особенностей: синтез жирных кислот в основном осуществляется в цитозоле клетки, а окисление – в митохондриях; участие в процессе биосинтеза жирных кислот малонил-КоА, который образуется путем связывания СО2 (в присутствии биотин-фермента и АТФ) с ацетил-КоА; на всех этапах синтеза жирных кислот принимает участие ацилпереносящий белок (HS-АПБ); при биосинтезе образуется D(–)-изомер 3-гидроксикис-лоты, а не L(+)-изомер, как это имеет место при β-окислении жирных кислот; необходимость для синтеза жирных кислот кофермента НАДФН. Последний в организме частично (на 50%) образуется в реакциях пен-тозофосфатного цикла, частично – в других реакциях, в частности в реакциях:
Малат + НАДФ + -> Пируват + С02 + НАДФН + Н + Изоцитрат + НАДФ + -> α-Кетоглутарат + С02 + НАДФН + Н + .
Образование ненасыщенных жирных кислот. Элонгация жирных кислот. В отличие от растительных тканей ткани животных обладают весьма ограниченной способностью превращать насыщенные жирные кислоты в ненасыщенные.
Установлено, что две наиболее распространенные мононенасыщенные жирные кислоты – пальмитоолеиновая и олеиновая – синтезируются из пальмитиновой и стеариновой кислот.
Эти превращения протекают в микросомах клеток печени и жировой ткани при участии молекулярного кислорода, восстановленной системы пиридиновых нуклеотидов и цитохрома b5. Превращению подвергаются только активированные формы пальмитиновой и стеариновой кислот. Ферменты, участвующие в этих превращениях, получили название деса-тураз.
Наряду с десатурацией жирных кислот (образование двойных связей) в микросомах происходит и их удлинение (элонгация), причем оба эти процесса могут сочетаться и повторяться. Удлинение цепи жирной кислоты происходит путем последовательного присоединения к соответствующему ацил-КоА двууглеродных фрагментов при участии малонил-КоА и НАДФН. Энзиматическая система, катализирующая удлинение жирных кислот, получила название элонгазы. На схеме представлены пути превращения пальмитиновой кислоты в реакциях десатурации и элонгации.
Путь синтеза жирных кислот длиннее, чем их окисление
Биосинтез жирных кислот наиболее активно происходит в цитозоле клеток печени, кишечника, жировой ткани в состоянии покоя или после еды.
Условно можно выделить 4 этапа биосинтеза:
1. Образование ацетил-SКоА из глюкозы, других моносахаров или кетогенных аминокислот.
2. Перенос ацетил-SКоА из митохондрий в цитозоль :
- может быть в комплексе с карнитином, подобно тому как переносятся внутрь митохондрии высшие жирные кислоты, но здесь транспорт идет в другом направлении,
- обычно в составе лимонной кислоты , образующейся в первой реакции ЦТК.
Поступающий из митохондрий цитрат в цитозоле расщепляется АТФ-цитрат-лиазой до оксалоацетата и ацетил-SКоА.
Образование ацетил-SКоА из лимонной кислоты
Оксалоацетат в дальнейшем восстанавливается до малата, и последний либо переходит в митохондрии (малат-аспартатный челнок), либо декарбоксилируется в пируват малик-ферментом («яблочный» фермент).
3. Образование малонил-SКоА из ацетил-SКоА.
Карбоксилирование ацетил-SКоА катализируется ацетил-SКоА-карбоксилазой , мульферментным комплексом из трех ферментов.
Образование малонил-SКоА из ацетил-SКоА
4. Синтез пальмитиновой кислоты.
Осуществляется мультиферментным комплексом » синтаза жирных кислот » (синоним пальмитатсинтаза ) в состав которого входит 6 ферментов и ацил-переносящий белок (АПБ).
Ацил-переносящий белок включает производное пантотеновой кислоты – 6-фосфопантетеин (ФП), имеющий HS-группу, подобно HS-КоА. Один их ферментов комплекса, 3-кетоацил-синтаза, также имеет HS-группу в составе цистеина. Взаимодействие этих групп обусловливает начало и продолжение биосинтеза жирной кислоты, а именно пальмитиновой кислоты. Для реакций синтеза необходим НАДФН.
Активные группы синтазы жирных кислот
В первых двух трансферазных реакциях последовательно присоединяются малонил-SКоА к фосфопантетеину ацил-переносящего белка и ацетил-SКоА к цистеину 3-кетоацилсинтазы.
3-Кетоацилсинтаза катализирует третью реакцию – перенос ацетильной группы на С 2 малонила с отщеплением карбоксильной группы в виде CO2.
Далее 3-кетогруппа в реакциях восстановления ( 3-кетоацил-редуктаза ), дегидратации ( дегидратаза ) и опять восстановления (еноил-редуктаза ) превращается в метиленовую с образованием насыщенного ацила, связанного с фосфопантетеином.
Ацилтрансфераза переносит полученный ацил на цистеин 3-кетоацил-синтазы, к фосфопантетеину АПБ присоединяется малонил-SКоА и цикл повторяется 7 раз. В первом цикле синтеза получается 4-углеродная (масляная) кислота, во втором — 6-углеродная (капроновая), и так далее до образования остатка пальмитиновой кислоты C16. После этого пальмитиновая кислота отщепляется шестым ферментом комплекса тиоэстеразой .
Реакции синтеза жирных кислот
Удлинение цепи жирных кислот
Синтезированная пальмитиновая кислота при необходимости поступает в эндоплазматический ретикулум. Здесь с участием малонил-S-КоА и НАДФН цепь удлиняется до С18 или С20. Присоединение углеродов идет по карбоксильной группе (С 1 ).
Удлиняться могут и ненасыщенные жирные кислоты (олеиновая, линолевая, линоленовая) с образованием производных эйкозановой кислоты (С20). Но двойная связь животными клетками вводится не далее 9 атома углерода, поэтому ω3- и ω6-полиненасыщенные жирные кислоты синтезируются только из соответствующих предшественников. Например, арахидоновая кислота может образоваться в клетке только при наличии γ-линоленовой или линолевой кислот. При этом линолевая кислота (18:2, Δ9,12) дегидрируется до γ-линоленовой (18:3, Δ6,9,12) и удлиняется до эйкозотриеновой кислоты (20:3, Δ8,11,14), последняя далее вновь дегидрируется до арахидоновой кислоты (20:4, Δ5,8,11,14). Так формируются жирные кислоты ω6-ряда.
Для образования жирных кислот ω3-ряда, например, тимнодоновой, необходимо наличие α-линоленовой кислоты (18:3, Δ9,12,15), которая дегидрируется (18:4, Δ6,9,12,15), удлиняется (20:4, Δ8,11,14,17) и опять дегидрируется с получением тимнодоновой кислоты (20:5, Δ5,8,11,14,17).
Параграф 46 синтез жирных кислот
Автор текстов Анисимова Елена Сергеевна.
Авторские права защищены. Продавать текст нельзя.
Курсив не зубрить.
Замечания присылать по электронной почте exam_bch@mail.ru
https://vk.com/bch_5
ПАРАГРАФ 46:
«СИНТЕЗ ЖИРНЫХ КИСЛОТ».
См. формулы в файле «46 формулы».
46.1. ЗНАЧЕНИЕ синтеза жирных кислот для организма –
этот процесс является источником жирных кислот для нужд клеток.
Основной путь использования жирных кислот в организме –
использование жирных кислот для синтеза жира (в основном в качестве «резерва энергии» на случай голода),
а также для синтеза липоидов, в том числе для синтеза МЕМБРАННЫХ липидов,
что нужно для образования новых клеток (для деления) и для «ремонта» мембран – то есть для замены молекул мембран новыми неповреждёнными молекулами (иначе мембраны быстрее разрушались бы, что приводило бы к гибели клеток).
Подробнее о том, зачем нужны жир и липоиды – см. п.47 и …
Снижение синтеза жирных кислот может привести к дефициту в организме липоидов, что в свою очередь может привести к дерматитам и другим проявлениям снижения пролиферативных процессов (деления клеток).
При снижении синтеза жирных кислот остаётся такой источник жирных кислот, как поступление жирных кислот с пищей в составе жира (точнее, в виде ацилов в составе пищевых липидов).
ГДЕ синтезируется пальмитиновая кислота.
Основное место синтеза пальмитиновой кислоты – печень. Не жировая ткань, не адипоциты, а печень.
После синтеза в печени пальмитиновая кислота используется для синтеза молекул жира (см. …) и липоидов, которые включаются в состав липопротеинов очень низкой плотности (ЛПОНП), которые поступают в кровь для доставки липидов в ткани. Подробности обмена ЛПОНП смотрите в п. … В итоге синтезированные в печени жирные кислоты оказываются в жировой ткани в составе жира – в качестве резерва энергии на случай голода.
46.2. Какие жирные кислоты синтезируются в организме человека.
В основном в организме синтезируется пальмитиновая кислота (её соли и анионы называются пальмитатами) с 16-тью атомами углерода и формулой С16Н31СООН (обозначение – С16:0).
Из неё может синтезироваться стеариновая кислота (С18:0), а из стеариновой – олеиновая (С18:1) и эйкозановая (С20:0).
Из линолевой кислоты может синтезироваться арахидоновая кислота (АрК).
Из линоленовой кислоты может синтезироваться эйкозапентаеновая (ЭПЕ) а из неё – докозагексаеновая (ДГЕ).
При этих реакциях происходит удлинение углеродной цепочки жирных кислот, которое называется элонгацией.
При образовании олеиновой кислоты из стеариновой, а также АрК из линолевой и ЭПЕ из линоленовой, ДГЕ из ЭПЕ происходит образование новых двойных связей, которое называется десатурацией и катализируется ферментами десатуразами.
Линолевая и линоленовая кислоты не могут синтезироваться в организме, должны поступать с пищей и поэтому называются незаменимыми жирными кислотами – аналогично тому как есть незаменимые аминокислоты.
Незаменимые жирные кислоты поступают в организм благодаря присутствию в пище растительных масел.
АрК, ЭПЕ и ДГЕ кислоты не считаются незаменимыми жирными кислотами, но лучше, если они поступают в организм с пищей (морепродукты).
При отсутствии в пище растительных масел и морепродуктов организм не получает незаменимы жирных кислот, что приводит к снижению синтеза мембранных липидов и деления клеток.
46.3. Регуляция синтеза жирных кислот.
Регуляция гормонами. Синтез жирных кислот происходит в состоянии сытости и покоя под влиянием инсулина (количество которого в крови увеличивается в этом состоянии).
В состоянии голода синтез жирных кислот снижается (по поговорке «не до жиру – быть бы живу») под влиянием гормона голода глюкагона.
В состоянии стресса и при работе синтез жирных кислот также снижается – под влиянием гормонов стресса катехоламинов (адреналина и норадреналина).
Дополнительно. – Синтез жирных кислот усиливается женскими половыми гормонами эстрогенами.
Регуляция метаболитами. Как обычно, продукты процесса и их метаболиты замедляют процесс, а субстраты усиливают (ацетилКоА).
46.4. Реакции синтеза пальмитиновой кислоты.
Синтез пальмитиновой кислоты осуществляется комплексом ферментов, который называется синтазой жирных кислот.
Из чего синтезируется молекула пальмитиновой кислоты – из молекул ацетилКоА. Источник ацетилКоА для синтеза жирных кислот – образование ацетилКоА из глюкозы (в ходе гликолиза и ПДГ – см. …). Именно поэтому сладости, мучное и картофель способствуют набору веса.
Для синтеза одной молекулы пальмитиновой кислоты (16 атомов углерода) нужно 8 молекул ацетилКоА (одна молекула ацетилКоА – это 2 атома углерода), атомы углерода которых нужно соединить в «цепочку».
Присоединение атома углерода каждого очередного ацетила происходит по очереди. К первому ацетилу присоединяется второй ацетил и т.д., пока не соединятся все 8 молекул, образовав молекулы пальмитиновой кислоты.
Далее идёт описание реакций. Формулы веществ и реакции смотрите в таблице к 46-му параграфу. Здесь только словесное описание формул и реакций таблицы. Без иллюстрации в таблице не поймёте.
1. «МалонилКоА». Семь молекул ацетилКоА из восьми превращаются в малонилКоА за счёт реакции с СО2 (точнее, с бикарбонатом – НСО3 – , который образуется из СО2), при которой образуется карбоксильная группа (из-за чего реакция называется карбоксилированием ацетилаКоА, а фермент, катализирующий эту реакцию, называется карбоксилазой ацетила КоА или ацетилКоА/карбоксилазой).
Для этой реакции необходим витамин Н (БИОТИН), поэтому при отсутствии биотина синтез жирных кислот не происходит, а дефицит биотина проявляется дерматитами (причиной дефицита биотина может быть дисбактериоз).
СО2 присоединяется ко второму атому углерода ацетилКоА.
Реакция происходит с затратой АТФ – АТФ расщепляется на АДФ и фосфат для выделения энергии.
По одной АТФ на синтез каждой молекулы малонилКоА, то есть всего тратится 7 молекул АТФ.
Сравните реакцию с карбоксилированием пирувата – много похожего.
Синтез жирных кислот – пример анаболического процесса, требующего затрат энергии.
2. «Замена КоА на АПБ, перенос с КоА на АПБ».
Первая молекула ацетилКоА и 7 молекул малонилКоА вступают в реакцию с АПБ (ацилпереносящим белком) для того, чтобы отсоединиться от КоА и присоединиться к АПБ. В результате образуются: 1 молекула ацетилАПБ и 7 молекул малонилАПБ.
3. Первая молекула ацетилАПБ вступает в реакцию с первой (с одной из семи) молекул малонилАПБ.
При этом соединяются первый атом углерода ацетилАПБ и ВТОРОЙ атом углерода малонил АПБ,
образуя молекулу из 4 атомов углерода с кетогруппой в третьем (;) положении, которая называется ;-кето/бутирилАПБ.
В реакции первый атом углерода ацетилАПБ отсоединяется от АПБ, а –СООН (карбоксильная группа) отсоединяется от второго атома углерода малонилаКоА и выделяется в реакции в виде СО2. (Таким образом, СО2 на синтез не тратится).
Бутирил – это остаток (ацил) 4-хуглеродной жирной кислоты (бутановой).
Далее все остатки любой длины называются просто ацилами.
У ;-кетобутирилАПБ есть кетогруппа. Нужно сделать так, чтобы на её месте в ;-положении была –СН2– группа (метиленовая), то есть нужно восстановить кетогруппу по метиленовой. Это происходит благодаря трём реакциям, «противоположным» реакциям ;-окисления.
4.1. Кетогруппа ;-кетобутирилаАПБ превращается в гидроксильную, в результате чего ;-КЕТОбутирилАПБ превращается в ;-ГИДРОКСИбутирилАПБ.
При этом происходит присоединение двух атомов водорода, источником которых является, как обычно, НАДФН, Н+, для образования которого клеткам нужен витамин РР. Катализируют реакции такого типа (перенос водорода от НАДФН на субстрат) РЕДУКТАЗЫ. Редуктаза данной реакции называется редуктазой ;-кетобутирилаАПБ или ;-кетобутирилАПБ/редуктазой.
Источником НАДФН, Н+ являются реакции ПЕНТОЗОФОСФАТНОГО пути (ПФП; вариант «пентозный цикл» в данном случае) – см. … , для протекания которого нужны ГЛЮКОЗА в качестве субстрата и ИНСУЛИН в качестве гормона, стимулирующего ПФП, а также витамины РР и В1.
4.2. ;-ГИДРОКСИбутирилАПБ теряет молекулу воды (НОН), при этом ОН отщепляется от 3-го атома углерода, а атом водорода (Н) – от второго. В итоге образуется вещество с двойной связью между 2-м и 3-и атомами углерода (; и ;), которое называется ЕНоилАПБ. (ЕН означает двойную связь).
Процесс отщепления Н и ОН и виде воды называется дегидратаций (не путать с дегидрированием), а фермент, который катализирует дегидратацию, называется дегидратазой, дегидратаза гидрокси/бутирилаАПБ называется гидрокси/бутирилАПБ/дегидратазой.
4.3. К еноилуАПБ по двойной связи присоединяются 2 атома водорода, в результате чего образуется бутирилАПБ.
Источником 2 атомов водорода является, как обычно, НАДФН, Н+. Катализируют реакции такого типа (перенос водорода от НАДФН на субстрат) РЕДУКТАЗЫ. Редуктаза данной реакции называется редуктазой еноилаАПБ или еноилАПБ/редуктазой.
БутирилАПБ является ацилом с 4 атомами углерода. Далее он вступает в реакцию с очередной (второй из семи исходных и из шести оставшихся) молекулой малонилАПБ так же, как вступал ацетилАПБ. – То есть первый атом углерода бутирилАПБ соединяется со вторым атомом углерода малонилаАПБ, АПБ и СО2 «уходят», образуется соединение с 6 атомами углерода и кетогруппой в ;-положении. Далее происходят реакции, аналогичные реакциям 4.1-4.3, в результате которых образуется ацилАПБ с шестью атомами углерода. То есть углеродная цепочка бутирила удлиняется ещё на 2 атома углерода.
АцилАПБ с шестью атомами углерода вступает в реакцию с очередной (то есть третьей из исходных семи) молекул малонилАПБ и т.д.
И так до тех пор, пока не будут использованы все 7 молекул малонилАПБ.
В результате образуется ацил из 16 атомов углерода – пальмитоилАПБ.
После этого остаётся отщепить пальмитоил от АПБ и превратить его в пальмитиновую кислоту.
5. ПальмитоилАПБ превращается в пальмитиновую кислоту за счёт расщепления связи между пальмитоилом и АПБ путём гидролиза (то есть с присоединением воды «по местам расщепления связи»).
46.4
Синтез жирных кислот – пример типичного анаболического процесса. (То есть процесса синтеза).
При этих процессах из простых веществ образуются более сложные – в данном случае 16-тиуглеродная цепочка из двухуглеродных молекул ацетилКоА.
Анаболические процессы протекают с затратой АТФ (7 молекул на одну молекулу пальмитиновой кислоты) и НАДФН (7*2= 14 молекул на одну молекулу пальмитиновой), поставляемого пентозофосфатным путём.
46.5
Сравнение синтеза жирных кислот и ;-окисления –
1. Синтез – процесс анаболический, а ;-окисление – катаболический.
2. АТФ: при синтезе АТФ тратится (7), а при ;-окислении образуется (108 АТФ за счёт одного пальмитата).
3. Коферменты: при синтезе НАДФН (образующийся в ПФП) превращается в НАДФ+ (который снова превращается в НАДФН в ПФП),
а при ;-окислении – НАД+ и ФАД и превращаются в НАДН и ФАДН2, поступающие в дыхательную цепь для выработки энергии.
4. Витамины: для синтеза нужны биотин и РР, а для ;-окисления – РР и В2. В составе коферментов.
5. Переносчики ацилов: при синтезе кофермент А (КоА) и АПБ (ацилпереносящий белок), а при ;-окислении – только кофермент А.
6. Локализация – синтез в печени, а ;-окисление – во всех клетках, кроме эритроцитов и нейронов.
7. В каких условиях протекают: синтез при сытости и покое под влиянием инсулина,
а ;-окисление – при стрессе под влиянием катехоламинов адреналина и норадреналина и при голоде под влиянием гормона голода глюкагона.
8. Какими гормонами стимулируются: синтез – инсулином и эстрогенами, а ;-окисление – катехоламинами и глюкагоном.
9. Какими гормонами тормозятся: синтез – катехоламинами при стрессе и глюкагоном при голоде, а ;-окисление – глюкагоном при голоде.
http://biokhimija.ru/lipidy/sintez-zhirnyh-kislot.html
http://proza.ru/2017/06/07/1247