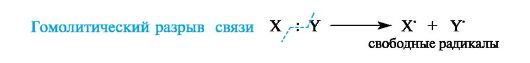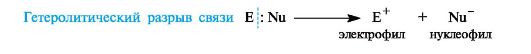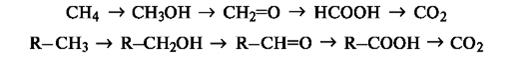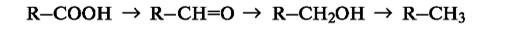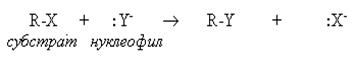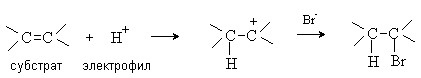Понятия – субстрат, реагент, реакционный центр, продукт реакции, энергия активации, скорость реакции, механизм.
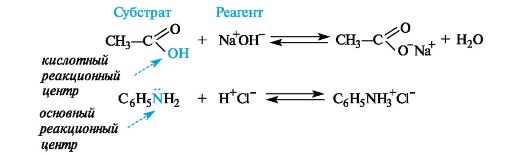
Субстрат —химическое вещество, подвергающееся превращению под действием фермента.
Реагент —это вещества, которые принимают участие в химической реакции, но при этом сами не являются объектом обработки.
реакционный центр —атом, у которого происходит разрыв или образование связей.
Продукт реакции– образующиеся в ходе реакции вещество.
Энергия активации —минимальное количество энергии, которое требуется сообщить системе (выражается в джоулях на моль), чтобы произошла реакция.
Скорость реакции —изменение количества одного из реагирующих веществ за единицу времени в единице реакционного пространства.
Механизм реакции —это детальное описание всех стадий химического процесса.
Типы реагентов: радикальные, кислотные, основные, электрофильные, нуклеофильные. Способы разрыва ковалентной связи в органических соединениях и образующиеся при этом частицы: свободные радикалы (гомолитический разрыв), карбкатионы и карбанионы (гетеролитический разрыв). Электронное и пространственное строение этих частиц и факторы, обусловливающие их относительную устойчивость.
Типы реагентов:
Радикальные реагенты(радикалы) — свободные атомы или частицы с неспаренным электроном. Примеры радикальных реагентов: гидроксильные НОˑ, гидропероксильные HOOˑ, алкильные Rˑ радикалы, атомы галогенов Сˑ, Brˑ.
Электрофильные реагенты(электрофилы) — частицы, образующие новую ковалентную связь за счет электронной пары реакционного партнера. Электрофильные частицы обозначаются символом Е + или Е. Они могут нести положительный заряд — протон Н + , карбокатионы R3C + , ацилий-катионы R-C=O — или быть электронейтральными, например триоксид серы SO3.
Кислотные реагенты(кислоты) — полностью или частично ионизированные в водных растворах нейтральные молекулы (CH3COOH, HCl) либо положительно заряженные частицы (катионы аммония NH4 + , гидроксония H3O + ), способные быть донором протона для реакционного партнера.
Нуклеофильные реагенты(нуклеофилы) — частицы, образующие новую ковалентную связь с реакционным партнером, предоставляя для этого свою электронную пару. Нуклеофильные частицы обозначаются символами Nu или Nu и могут быть отрицательно заряженными — гидрид-ион Н — , гидроксид-ион НО — , алкоксид-ион RO — , карбанион R3C — , хлорид-ион Cl — или быть электронейтральными. В этом случае их нуклеофильность обусловлена р- или π-электронами (NH3, H2O, CH2=CH2, C6H6).
Термин «нуклеофил» применяется к частице, реагирующей с любым электрофильным реакционным партнером за исключением протона Н + .
Основные реагенты(основания) — отрицательно заряженные частицы (НО — , RO — ) или нейтральные молекулы (NH3, H2O), способные оторвать протон от кислотного реакционного центра. Основные реагенты обозначаются символами B — или B.
В соответствии с характером разрыва связи в субстрате и природой реагента различают реакции радикальные и ионные.
В радикальных, или гомолитических, реакциях(символ R) участвуют радикальные реагенты и происходит гомолитический разрыв ковалентной связи в субстрате. При гомолитическом, или свободнорадикальном, разрыве ковалентной связи (гомолизе)у каждого из ранее связанных атомов остается по одному электрону. В результате в качестве промежуточных частиц образуются радикальные реагенты, как показано ниже для молекулы X-Y (где X и Y обозначают ковалентно связанные атомы или группы атомов).
Ионные(гетеролитические) реакциисопровождаются гетеролитическим разрывом связи в субстрате. При таком разрыве (гетеролизе) ковалентной связи электронная пара, связывающая атомы, остается с одним из партнеров по связи. При этом образуются электрофильная и нуклеофильная частицы.
В качестве промежуточных частиц в гетеролитических реакциях принимают участие карбокатионы R3C + и карбанионы R3C — .
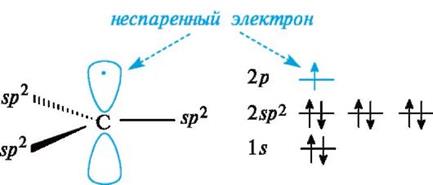
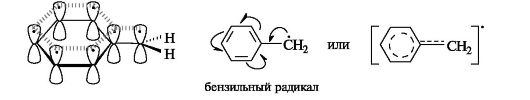
Свободные радикалы.Входящий в состав свободнорадикальных частиц атом углерода с неспаренным электроном находится в состоянии sр 2 -гибридизации и три его валентные связи лежат в одной плоскости. Неспаренный электрон занимает негибридизованную р-АО, расположенную перпендикулярно плоскости σ-связей (рис. 6).
Рис. 6.Распределение электронов по орбиталям в свободном радикале
Высокая реакционная способность свободных радикалов объясняется их стремлением достроить внешний электронный уровень до устойчивого октета. Алкильные радикалы — короткоживущие частицы. Их относительная устойчивость соответствует ряду: третичный > вторичный > первичный.
Это связывают с энергией разрыва соответствующей связи С-Н, которая составляет 414 кДж/моль в этане, 396 кДж/моль для группы в пропане и 376 кДж/моль для группы СН в 2-метилпропане.
Стабильность свободных радикалов существенно возрастает, когда имеется возможность делокализации неспаренного электрона за счет участия π-электронов соседней двойной связи или бензольного кольца. Для систем с открытой цепью сопряжения наиболее типичным примером является аллильный радикал, а для систем с ароматическим циклом — бензильный радикал (одноэлектронные смещения обозначены стрелкой с одним острием).
8. Классификация органических реакций по результату (замещения, присоединения, элиминирования, перегруппировки, окислительно-восстановительные) и по механизму – радикальные, ионные (электрофильные, нуклеофильные), согласованные.
По направлению (конечному результату) органические реакции делят на несколько основных типов:
В случае реакций замещения в молекуле один атом (или группа атомов) замещается другим атомом (или группой атомов), в результате чего образуются новые соединения:
При протекании реакций присоединенияиз двух (или нескольких) молекул образуется одно новое вещество:
В результате реакции отщепления (элиминирования) образуется новое органическое вещество, содержащее кратную связь:
Реакции разложения приводят к образованию из одного вещества двух или более веществ более простого строения:
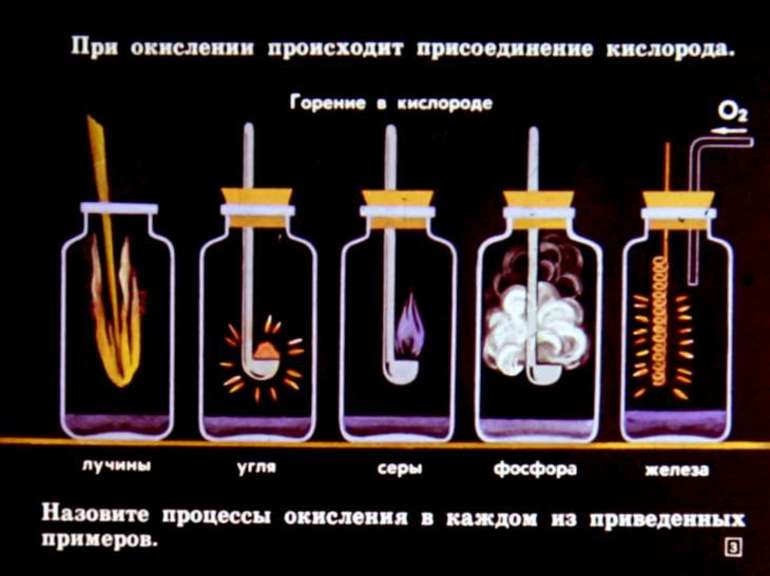
окислительно-восстановительные реакции. Процесс окисления включает переход электронов от органического субстрата к реагенту-окислителю, а процесс восстановления — передачу электронов от реагента к органическому субстрату. В органической химии более распространен иной подход к трактовке реакций окисления и восстановления. Под окислением понимают введение атома кислорода в молекулу субстрата или удаление двух атомов водорода, как, например, в следующих рядах:
При таком подходе восстановление представляет собой обратный процесс, т.е. удаление атома кислорода или введение двух атомов водорода:
В окислительно-восстановительных реакциях органических соединений, безусловно, меняется степень окисления атома углерода, являющегося реакционным центром. Учет изменения степени окисления, однако, может потребоваться только при необходимости расстановки коэффициентов в уравнении реакции. В то же время многие процессы, протекающие с изменением степени окисления атома углерода, такие, как дегидрирование (-СН2СН2—→ -СН=СН-) или галогенирование (-СН3— →СН2О), классифицируются не как реакции окисления.
Реакция перегруппировки (молекулярная перегруппировка) — химическая реакция, в результате которых происходит изменение взаимного расположения атомов в молекуле, места кратных связей и их кратности; могут осуществляться с сохранением атомного состава молекулы (изомеризация) или с его изменением.
Классификация органических реакций по механизму:
В радикальных реакциях реагент имеет неспаренный электрон и является свободным радикалом (Cl , R и др.). В ходе радикальных реакций связь в субстрате разрывается гомолитически, а новая связь образуется за счет неспаренного электрона свободного радикала и одного из электронов старой связи. Примером радикальных реакций может служить радикальное замещение (символ SR) в алканах:
R• + Cl-Cl → R-Cl + Cl•
В ионных реакциях происходит гетеролитический разрыв связей в субстрате под действием электрофильного или нуклеофильного реагентов.
В нуклеофильных реакциях реагент (нуклеофил) имеет на одном из атомовсвободную пару электронов и является нейтральной молекулой или анионом (Hal — , OH — , RO — , RS — , RCOO — , R — , CN — , H2O, ROH, NH3, RNH2 и др.). Все нуклеофилы – основания Льюиса. Нуклеофил атакует в субстрате атом с наименьшей электронной плотностью (т.е. с частичным или полным положительным зарядом). При этом новая связь образуется за счет электронной пары нуклеофила, а старая претерпевает гетеролитический разрыв. Примером нуклеофильной реакции может служить нуклеофильное замещение (символ SN) у насыщенного атома углерода:
В электрофильных реакциях атакующий реагент (электрофил) имеет вакантную орбиталь и является нейтральной молекулой или катионом (Cl2, SO3, BF3, H + , Br + , R + , NO2 + , и др.). Все электрофилы – кислоты Льюиса. Электрофил атакует в субстрате атом с наибольшей электронной плотностью, причем старая связь претерпевает гетеролитический распад, а образование новой связи происходит за счет пары электронов субстрата. Пример электрофильной реакции – электрофильное присоединение (символ AdE) к С=С связи:
В согласованных реакциях разрыв старых и образование новых связей происходит одновременно.
Кислотность и основность органических соединений: теория Бренстеда. Классификация кислот и оснований Бренстеда. Общие закономерности в изменении кислотных и основных свойств во взаимосвязи с электронными эффектами заместителей.
Основные правила составления названий по номенклатуре ИЮПАК для органических соединений; заместительная и радикально-функциональная номенклатура. Родоначальная структура, заместители, характеристические группы.
В настоящее время общепринята систематическая номенклатура ИЮПАК (IUPAC — Международный союз теоретической и прикладной химии).
Для использования систематической номенклатуры ИЮПАК необходимо знать содержание следующих номенклатурных терминов:
Органический радикал— остаток молекулы, из которой удаляются один или несколько атомов водорода и при этом остаются свободными одна или несколько валентностей.
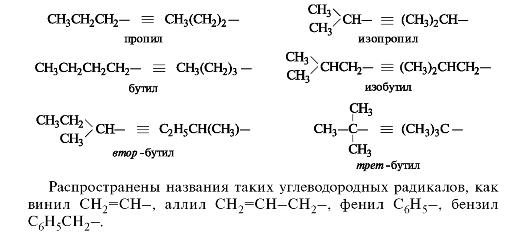
Углеводородные радикалы алифатического ряда имеют общее название — алкилы (в общих формулах обозначаются R), радикалы ароматического ряда — арилы (Ar). Два первых представителя алканов — метан и этан — образуют одновалентные радикалы метил СН3— и этил СН3СН2-. Названия одновалентных радикалов обычно образуются при замене суффикса -ан суффиксом -ил.
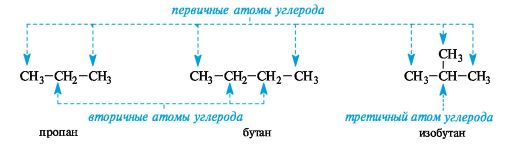
Атом углерода, связанный только с одним атомом углерода (т. е. концевой), называют первичным, с двумя — вторичным, с тремя — третичным, с четырьмя — четвертичным.
Каждый последующий гомолог из-за неравноценности атомов углерода образует несколько радикалов. При удалении атома водорода от концевого атома углерода пропана получают радикал н-пропил (нормальный пропил), а от вторичного атома углерода — радикал изопропил. Бутан и изобутан каждый образуют по два радикала. Буква н-(которую разрешается опускать) перед названием радикала указывает, что свободная валентность находится на конце неразветвленной цепи. Префикс втор- (вторичный) означает, что свободная валентность находится у вторичного атома углерода, а префикс трет- (третичный) — у третичного.
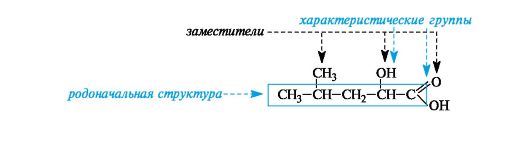
Родоначальная структура— химическая структура, составляющая основу называемого соединения. В ациклических соединениях в качестве родоначальной структуры рассматривается главная цепь атомов углерода, в карбоциклических и гетероциклических соединениях — цикл.
Характеристическая группа— функциональная группа, связанная с родоначальной структурой или частично входящая в ее состав.
Заместитель— любой атом или группа атомов, замещающие в органическом соединении атом водорода.
Локант(от лат. locus — место) цифра или буква, указывающая положение заместителя или кратной связи.
Наиболее широко применяются два вида номенклатуры: заместительная и радикально-функциональная.
Что такое реагенты вещества в уравнении
ХИМИЯ – это область чудес, в ней скрыто счастье человечества,
величайшие завоевания разума будут сделаны
именно в этой области.(М. ГОРЬКИЙ)
Таблица
Менделеева
Универсальная таблица растворимости
Коллекция таблиц к урокам по химии
Составление уравнений химических реакций
Урок посвящен изучению алгоритма составления уравнения химической реакции. В ходе урока вы научитесь составлять схему и уравнение химической реакции, зная формулы исходных веществ и продуктов реакции.
I. Схема химической реакции
Сущность химической реакции с позиции атомно-молекулярной теории заключается в том, что продукты реакции образуются из тех же атомов, которые входили в состав исходных веществ.
Пример 1. При разложении воды образуются простые вещества – водород и кислород (Рис.1.).
Рис. 1. Разложение воды под действие электрического тока
Запишем формулу исходного вещества воды слева, а формулы продуктов реакции — водорода и кислорода – справа. Между ними поставим стрелку:
Эта запись является схемой реакции.
Схема реакции показывает только состав исходных веществ и продуктов реакции, но не может полностью отражать сущность реакции. В состав молекулы воды входит один атом кислорода, а в состав простого вещества кислорода входят два атома. Это значит, что не выполняется закон сохранения массы веществ.
II. Химические уравнения реакций
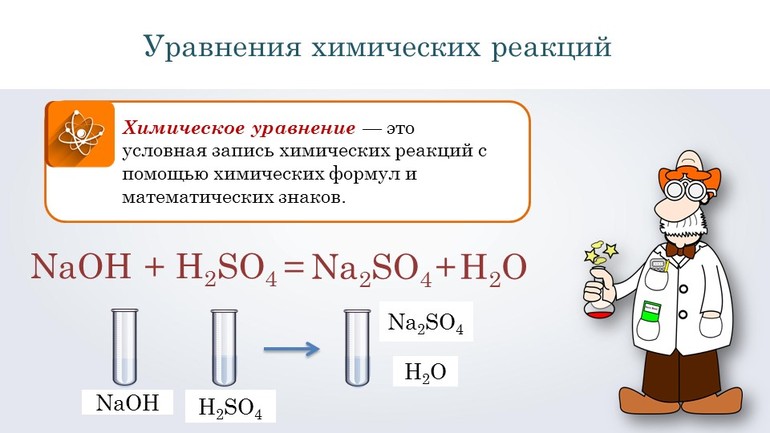
Химическое уравнение – это условная запись химической реакции посредством химических формул и коэффициентов.
В результате химического взаимодействия серы и железа получено вещество – сульфид железа (II) – оно отличается от исходной смеси. Ни железо, ни сера не могут быть визуально обнаружены в нем. Невозможно их разделить и с помощью магнита. Произошло химическое превращение.
Запишем протекающую реакцию в виде уравнения химической реакции:
Рассмотрим еще один пример: 2Н2О = 2Н2 + О2
Чтобы не было противоречий с законом сохранения массы веществ, нужно уравнять число атомов каждого химического элемента слева и справа от стрелки.
Чтобы образовалась одна молекула кислорода, в реакцию должны вступить две молекулы воды. Поставив коэффициент «2» перед формулой воды. Теперь уравняем количество атомов водорода, поставив коэффициент «2» перед формулой Н2, вместо стрелки поставим знак равенства:
Эта запись является уравнением химической реакции. В отличие от схемы реакции, уравнение учитывает, что число атомов каждого химического элемента в реакции не меняется.
Цифры, стоящие перед формулой вещества, называются коэффициентами. Коэффициент показывает количество молекул вещества.
Прочитать записанное уравнение можно так: «Из двух молекул воды образуется две молекулы водорода и 1 молекула кислорода».
Составим уравнение химической реакции взаимодействия фосфора и кислорода
1. В левой части уравнения записываем химические формулы реагентов (веществ, вступающих в реакцию). Помните! Молекулы большинства простых газообразных веществ двухатомны – H2; N2; O2; F2; Cl2; Br2; I2. Между реагентами ставим знак «+», а затем стрелку:
2. В правой части (после стрелки) пишем химическую формулу продукта (вещества, образующегося при взаимодействии). Помните! Химические формулы необходимо составлять, используя валентности атомов химических элементов:
3. Согласно закону сохранения массы веществ число атомов до и после реакции должно быть одинаковым. Это достигается путём расстановки коэффициентов перед химическими формулами реагентов и продуктов химической реакции.
- Вначале уравнивают число атомов, которых в реагирующих веществах (продуктах) содержится больше.
- В данном случае это атомы кислорода.
- Находим наименьшее общее кратное чисел атомов кислорода в левой и правой частях уравнения. Наименьшее кратное для атомов натрия –10:
Как решать химические уравнения — схемы и примеры решения для разных реакций
Основные термины и понятия
Составление уравнений химических реакций невозможно без знания определённых обозначений, показывающих, как проходит реакция. Объединение атомов, имеющих одинаковый ядерный заряд, называют химическим элементом. Ядро атома состоит из протонов и нейтронов. Первые совпадают с числом атомного номера элемента, а значение вторых может варьироваться. Простейшими веществами называют элементы, состоящие из однотипных атомов.
Любой химический элемент описывается с помощью символов, условно обозначающих структуру веществ. Формулы являются неотъемлемой частью языка науки. Именно на их основе составляют уравнения и схемы. По своей сути они отражают количественный и качественный состав элементов. Например, запись HNO3 сообщает, что в соединении содержится одна молекула азотной кислоты, а оно само состоит из водорода, азота и кислорода. При этом в состав одного моля азотной кислоты входит по одному атому водорода и азота и 3 кислорода.
Символика элементов, условное обозначение, представляет собой химический язык. В значке содержится информация о названии, массовом числе и порядковом номере. Международное обозначение принято, согласно периодической таблице Менделеева, разработанной в начале 1870 года.
Взаимодействующие между собой вещества называются реагентами, а образующиеся в процессе реакции — продуктами. Составление и решение химических уравнений фактически сводится к определению результатов реакций, поэтому просто знать формулы веществ мало, нужно ещё уметь подбирать коэффициенты. Располагаются они перед формулой и указывают на количество молекул или атомов, принимающих участие в процессе. С правой стороны от химического вещества ставится индекс, указывающий место элемента в системе.
Записывают уравнения в виде цепочки, в которой указываются все стадии превращения вещества начиная с левой части. Вначале пишут формулы элементов в исходном состоянии, а затем последовательно их преобразование.
Виды химических реакций
Химические явления характеризуются тем, что из двух и более элементов образуются новые вещества. Уравнения описывают эти процессы. Впервые с объяснениями протекания реакций знакомят в восьмом классе средней образовательной школы на уроках неорганической химии. Ученикам демонстрируют опыты, в которых явно наблюдаются различия в протекании реакций.
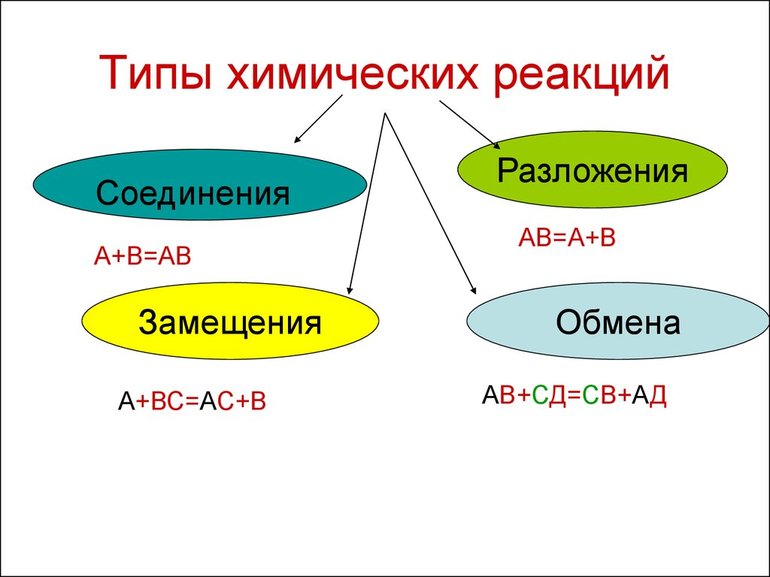
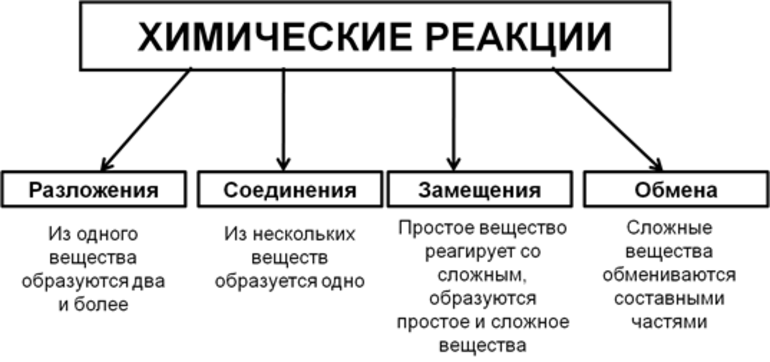
Всего существует 4 типа химического взаимодействия веществ:
- Соединение. В реакцию могут вступать 2 простых вещества: металл и неметалл или неметалл и неметалл. Например, алюминий с серой образуют сульфид алюминия. Кислород, взаимодействуя с водородом, превращается в воду. Объединятся могут 2 оксида с растворимым основанием, как оксид кальция с водой: CaO + H2O = Ca (OH)2 или основной оксид с кислотным: CaO + SO3 = CaSO4.
- Разложение. Это процесс обратный реакции соединения: было одно вещество, а стало несколько. Например, при пропускании электрического тока через воду получается водород и кислород, а при нагревании известняка 2 оксида: CaCO3 = CaO + CO2.
- Замещение. В реакцию вступают 2 элемента. Один из них простой, а второй сложный. В итоге образуются 2 новых соединения, при котором атом простого вещества заменяет сложный, как бы вытесняя его. Условие протекания процесса: простое вещество должно быть более активным, чем сложное. Например, Zn + 2HCl = ZnCl2 + H2. Величину активности можно узнать из таблицы ряда электрохимических напряжений.
- Обмен. В этом случае между собой реагируют 2 сложных элемента, обменивающиеся своими составными частями. Условием осуществления такого типа реакции является обязательное образование воды, газа или осадка. Например, CuO + 2HCl = CuCl2 + H2O. Чтобы узнать, смогут ли вещества прореагировать, используют таблицу растворимости.
Основными признаками химических реакций является изменение цвета, выделение газа или образование осадка. Различают их по числу веществ, вступивших в реакцию и образовавшихся продуктов. Правильное определение типа реакции особо важно при составлении химических уравнений, а также определения свойств и возможностей веществ.
Окислительно-восстановительный процесс
Составление большинства реакций сводится к подбору коэффициентов. Но при этом могут возникнуть трудности с установлением равновесия, согласно закону сохранения массы веществ. Чаще всего такая ситуация возникает при решении заданий, связанных с расстановкой количества атомов в уравнениях окислительно-восстановительных процессов.
Под ними принято понимать превращения, протекающие с изменением степени окисления элементов. При окислении происходит процесс передачи атомом электронов, сопровождающийся приобретением им положительного заряда или ионом, после чего он становится нейтральным. При этом также происходит процесс восстановления, связанный с присоединением элементарных частиц атомом.
Для составления уравнений необходимо определить восстановитель, окислитель и число участвующих в реакции электронов. Коэффициенты же подбирают с помощью метода электронно-ионного баланса (полуреакций). Его суть состоит в установлении равенства путём уравнивания количества электронов, отдаваемых одним элементом и принимаемым другим.
Классический алгоритм
В основе решения задач этим методом — закон сохранения массы. Согласно ему, совокупная масса элементов до реакции и после остаётся неизменной. Другими словами, происходит перегруппировка частиц. Если рассматривать решение химического уравнения поэтапно, оно будет состоять из трёх шагов:
- Написания формул элементов, вступающих в реакцию с левой стороны.
- Указания справа формулы образующихся веществ.
- Уравнивания числа атомов с добавлением коэффициентов.
Перед тем как переходить к сложным соединениям, лучше всего потренироваться на простых. Например, нужно составить уравнение, описывающее взаимодействие двух сложных веществ: гидроксида натрия и серной кислоты. При таком соединении образуется сульфат натрия и вода.
Согласно алгоритму, в левой части уравнения необходимо записать реагенты, а в правой продукты реакции: NaOH + H2SO 4 → Na 2SO4 + H2O. Теперь следует уравнять коэффициенты. Начинают с первого элемента. В примере это натрий. В правой части содержится 2 его атома, а в левой один, поэтому необходимо возле реагента поставить цифру 2. Затем нужно уровнять водород. В результате получится выражение: 2 NaOH + H2SO 4 → Na2 SO4 +2H2O.
Ещё одним наглядным примером является процесс реакции тринитротолуола с кислородом. При их взаимодействии образуется: C7H5N3O6 + O2 → CO2 + H2O + N2. Исходя из того, что слева находится нечётное число атомов H и N, а справа чётное, нужно их уравнять: 2C7H5N3O6 + O2 → CO2 + H2O + N2.
Теперь становится понятным, что 14 и 10 атомов углерода и водорода должны образовать 14 долей диоксида и 5 молекул воды. При этом 6 атомов азота превратятся в 3. Итоговое уравнение будет выглядеть как 2C7H5N3O6 + 10,5O2 → 14CO2 + 5H2O + 3N2.
Перед тем как начинать тренировку по составлению уравнений, следует научиться расставлять валентность. Это параметр, равный числу соединившихся атомов каждого элемента. Фактически это способность к соединению. Например, в формуле NH3 валентность атома азота равна 3, а водорода 1.
Решение методом полуреакций
Алгоритм для решения примеров химических уравнений проще рассмотреть на конкретном задании. Пускай необходимо описать процесс окисления пирита азотной кислоты с малой концентрацией: FeS2 + HNO3. Решать этот пример необходимо в следующей последовательности:
- Определить продукты реакции. Так как кислота является сильным окислителем, сера получит максимальную степень оксидации S6+, а железо Fe3+. HNO3 может восстановиться до одного из двух состояний NO2 или NO.
- Исходя из состава ионов и правила, что вещества, переходящие в газовую форму или плохо растворимые, записываются в молекулярном виде, верным будет записать: FeS2 — Fe3+ + 2SO2−4. Гидролизом можно пренебречь.
- В записи уравнивают кислород. Для этого в левую часть добавляют 8 молекул воды, а в правую 16 ионов водорода: FeS2 + 8H20 — Fe3+ + 2SO2−4 + 16H+. Так как заряда в левой части нет, а в правой он равный +15, то серное железо должно будет отдать 15 электронов. Значит, уравнение примет вид: FeS2 + 8H20 — 15e → Fe3+ + 2SO2−4 + 16H+.
- Теперь переходят к реакции восстановления нитрата иона: NO-3 →NO. Для её составления нужно отнять у оксида азота 2 атома кислорода. Делают это путём прибавления к левой части 4 ионов водорода, а правой — 2 молекул воды. В итоге получится: NO-3 + 4H+ → NO + 2H2O.
- Полученную формулу уравнивают добавлением к левой части 3 электронов: NO-3 + 4H+ 3e → NO + 2H2O.
- Объединяют найденные выражения и записывают результат: FeS2 + 8H20 + 5NO-3 + 20H+ → Fe3+ + 2SO2−4 + 16H+ + 5NO + 10H2O.
Уравнение можно сократить на 16H + и 8H2O. В итоге получится сокращённое выражение окислительно-восстановительной реакции: FeS2 + 5NO — 3 + 4 H + = Fe3 + + 2SO 2- 4 + 5NO + 2H2O.
Такой алгоритм считается классическим, но для упрощения понимания лучше использовать способ электронного баланса. Процесс восстановления переписывают как N5+ + 3e → N2+. Степень же окисления составить сложнее. Сере нужно приписать степень 2+ и учесть, что на 1 атом железа приходится 2 атома серы: FeS2 → Fe3++ 2S6+. Запись общего баланса будет выглядеть: FeS2 + 5N5+ = Fe3+ + 2S6+ + 5N2+.
Пять молекул потратятся на окисление серного железа, а ещё 3 на образование Fe (NO3)3. После уравнения двух сторон запись реакции примет вид, аналогичный полученному с использованием предыдущего метода.
Использование онлайн-расчёта
Простые уравнения решать самостоятельно довольно просто. Но состоящие из сложных веществ могут вызвать трудности даже у опытных химиков. Чтобы получить точную формулу и не подбирать вручную коэффициенты, можно воспользоваться онлайн-калькуляторами. При этом их использовать сможет даже пользователь, не особо разбирающийся в науке.
Чтобы расстановка коэффициентов в химических уравнениях онлайн происходила автоматически, нужно лишь подключение к интернету и исходные данные. Система самостоятельно вычислит продукты реакции и уравняет обе стороны формулы. Интересной особенностью таких сайтов является не только быстрый и правильный расчёт, но и описание правил с алгоритмами, по которому выполняются действия.
После загрузки калькулятора в веб-обозревателе единственное, что требуется от пользователя — правильно ввести реагенты в специальные формы латинскими буквами и нажать кнопку «Уравнять». Иногда возникает ситуация, когда запись сделана верно, но коэффициенты не расставляются. Это происходит, если суммы в уравнении могут быть подсчитаны разными способами. Характерно это для реакций окисления. В таком случае нужно заменить фрагменты молекул на любой произвольный символ. Таким способом можно не только рассчитать непонятное уравнение, но и выполнить проверку своих вычислений.
http://kardaeva.ru/88-dlya-uchenika/8-klass/124-sostavlenie-uravnenij-khimicheskikh-reaktsij
http://nauka.club/khimiya/khimicheskie-uravneniya.html