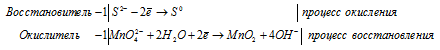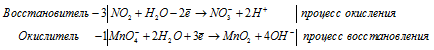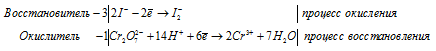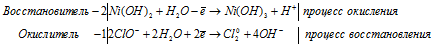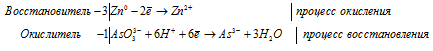Оксид хрома (III)
Оксид хрома (III)
Способы получения
Оксид хрома (III) можно получить различными методами :
1. Термическим разложением гидроксида хрома (III):
2. Разложением дихромата аммония:
3. Восстановлением дихромата калия углеродом (коксом) или серой:
Химические свойства
Оксид хрома (III) – типичный амфотерный оксид . При этом оксид химически довольно инертен. В высокодисперсном состоянии с трудом взаимодействует с кислотами и щелочами.
1. При сплавлении оксида хрома (III) с основными оксидами активных металлов образуются соли-хромиты.
Например , оксид хрома (III) взаимодействует с оксидом натрия:
2. Оксид хрома (III) взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—хромиты, а в растворе реакция практически не идет . При этом оксид хрома (III) проявляет кислотные свойства.
Например , оксид хрома (III) взаимодействует с гидроксидом натрия в расплаве с образованием хромита натрия и воды:
3. Оксид хрома (III) не взаимодействует с водой.
4. Оксид хрома (III) проявляет слабые восстановительные свойства . В щелочных расплавах окислителей окисляется до соединений хрома (VI).
Например , оксид хрома (III) взаимодействует с нитратом калия в щелочной среде:
Оксид хрома (III) окисляется бромом в присутствии гидроксида натрия:
Озоном или кислородом:
Нитраты и хлораты в расплаве щелочи также окисляют оксид хрома (III):
5. Оксид хрома (III) в высокодисперсном состоянии при сильном нагревании взаимодействует с сильными кислотами .
Например , оксид хрома (III) реагирует с серной кислотой:
6. Оксид хрома (III) проявляет слабые окислительные свойства при взаимодействии с более активными металлами.
Например , оксид хрома (III) реагирует с алюминием (термит):
Реакция очень экзотермическая, сопровождается выделением большого количества света:

Если сжечь большой объем термита в тигле, то можно получить металлический хром:

7. Оксид хрома (III) – твердый, нелетучий. А следовательно, он вытесняет более летучие оксиды (как правило, углекислый газ) из солей при сплавлении.
Например , из карбоната калия:
Оксид хрома CrO(II)
Низший оксид для элементов 6-й группы состава MeO получен только для хрома.
Физические свойства CrO(II):
- тугоплавкий порошок черного цвета;
- нерастворим в воде;
- устойчив на воздухе.
Химические свойства CrO(II):
- типичный основной оксид;
- реагирует с кислотами:
CrO+2HCl = CrCl2+H2O; - является сильным восстановителем;
- воспламеняется при нагревании или растирании на воздухе, сгорая до Cr2O3;
- при высокой температуре (1000°C) «забирает» кислород у углекислого газа:
- 2CrO+CO2 → Cr2O3+CO;
- в инертной атмосфере нагревание CrO (700°C) приводит к диспропорционированию:
3CrO → Cr2O3+Cr - CrO(II) получают путем воздействия на амальгаму хрома кислородом воздуха:
2Cr+O2 = 2CrO
Гидроксид хрома Cr(OH)2(II)
Физические свойства Cr(OH)2(II):
- вещество коричнево-желтого цвета;
- нерастворим в воде;
- быстро окисляется на воздухе.
Химические свойства Cr(OH)2(II):
- проявляет оснОвные свойства;
- реагирует с кислотами:
Cr(OH)2+H2SO4 = CrSO4+2H2O - Cr(OH)2(II) получают, как продукт реакции солей хрома с щелочью в отсутствии кислорода:
CrCl2+2NaOH = Cr(OH)2↓+2NaCl
Соединения хрома со степенью окисления +2 являются неустойчивыми, легко окисляются кислородом воздуха в более устойчивые соединения хрома со степенью окисления +3:
4Cr(OH)2+O2+2H2O = 4Cr(OH)3
Оксид хрома Cr2O3(III) — хромовая охра
Cr2O3 в мелкоизмельченном состоянии применяют в качестве абразивного материала (паста ГОИ), зеленого пигмента, катализатора в органическом синтезе. Оксид хрома (III) является основной добавкой к корунду при выращивании искусственных рубинов, используемых в ювелирной промышленности и часовом деле, а также в качестве лазерного материала в оптоэлектронике.
Физические свойства Cr2O3(III):
- тугоплавкий порошок серо-зеленого цвета, имеющий структуру корунда (α-Al2O3);
- нерастворим в воде;
- обладает высокой твердостью;
- меняет свой цвет от светло-зеленого до черного в зависимости от размеров кристаллов;
- при н.у. является полупроводником;
- при нагревании порошок приобретает коричневый цвет, при охлаждении зеленая окраска возвращается;
- Cr2O3 с корундом образует твердые растворы, в которых катионы хрома и алюминия заполняют пустоты анионной решетки, такие твердые растворы с содержанием Cr2O3 до 10% имеют красный цвет, и в природе известны под названием рубин, который является драгоценным камнем-минералом. Твердые растворы в которых содержание оксида хрома превышает 10%, имеют зеленый цвет (окраска твердого раствора зависит от расстояния связи металл-кислород).
Химические свойства Cr2O3(III):
- Cr2O3 амфотерный оксид — самое устойчивое соединение хрома;
- при н.у. плохо растворим в кислотах и щелочах;
- при сплавлении с щелочами (карбонатами щелочных металлов) образует метахромиты:
Cr2O3+2KOH = 2KCrO2+H2O
Cr2O3+Na2CO3 = 2NaCrO2+CO2↑ - с кислотами образует соли:
Cr2O3+6HCl = 2CrCl3+3H2O - с щелочами образует комплексные соединения хрома:
Cr2O3+6KOH+3H2O = 2K2[Cr(OH)6] - в промышленности Cr2O3 получают восстановлением дихромата калия серой или коксом:
K2Cr2O7+S = Cr2O3+K2SO4 - Cr2O3 также можно получить разложением дихромата аммония или прокаливанием гидроксида хрома:
(NH4)Cr2O7 = Cr2O3+N2+4H2O
2Cr(OH)3 = Cr2O3+3H2O
Гидроксид хрома Cr(OH)3(III)
Физические свойства Cr(OH)3(III):
- амфотерный малоустойчивый гидроксид различной окраски (голубой, фиолетовой, зеленой), которая зависит от условий получения;
- имеет различную химическую активность;
- плохо растворим в воде.
Химические свойства Cr(OH)3(III):
- реагирует с кислотами с образованием солей:
Cr(OH)3+3H2SO4 = Cr2(SO4)3+6H2O - реагирует с щелочами с образованием комплексных соединений хрома:
Cr(OH)3+NaOH = Na[Cr(OH)4] - осаждается при действии щелочей на соли хрома:
Cr(OH)3+3NaOH = Cr(OH)3↓+3NaCl - выпавший в осадок гидрооксид хрома растворим в кислотах:
Cr(OH)3+3HCl = CrCl3+3H2O - и в избытке щелочей:
Cr(OH)3+3NaOH = Na3[Cr(OH)6]
Оксид хрома CrO2(IV) (диоксид хрома)
Диоксид хрома применяется в производстве элементов памяти для компьютеров.
- все диоксиды элементов 6-й группы (Cr, Mo, W) имеют структуру рутила;
- не реагируют с водой и щелочами;
- диоксид хрома имеет черную окраску, обладает металлической проводимостью, является ферромагнетиком;
- диоксиды, как промежуточный прдукт реакции, получают при разложении или восстановлении высших оксидов (VI) соответствующих металлов, при темературах 250°(Cr), 450°C(Mo), 600°C(W):
3(NH4)Cr2O7 → 6CrO2+2N2+9H2O+2NH3
MoO3+H2 → MoO2+H2O
WO3+H2 → WO2+H2O - диоксид хрома получают нагреванием Cr2O3 в кислороде при 300°C и высоком давлении;
- устойчивость диоксида возрастает в ряду от хрома к вольфраму.
Оксид хрома CrO3(VI) (хромовый ангидрид)
Физические свойства CrO3(VI):
- кристаллы красно-фиолетового цвета;
- разлагаются при комнатной температуре;
- расплывается на воздухе по причине высокой гигроскопичности;
- хорошо растворим в воде.
Химические свойства CrO3(VI):
- CrO3(VI) является кислотным оксидом;
- растворяясь в воде, образует хромовые кислоты:
- хромовая кислота: CrO3+H2O(изб) = H2CrO4
- дихромовая кислота: 2CrO3+H2O(нед) = H2Cr2O7
- реагирует с основаниями:
CrO3+2KOH = K2CrO4+H2O - CrO3 окисляет углерод, серу, фосфор, йод, образуя оксид хрома (III):
4CrO3+3S = 3SO2+2Cr2O3 - нагретый до температуры выше 250°C, триоксид хрома разлагается на молекулярный кислород и оксид хрома (III):
4CrO3 = 2Cr2O3+3O2
Триоксид хрома получают действием концентрированной серной кислоты на концентрированные растворы хроматов/дихроматов калия/натрия:
K2Cr2O7+H2SO4 = 2CrO3↓+K2SO4+H2O
Гидроксиды хрома
К гидроксидам хрома относятся две кислоты — хромовая и дихромовая, существующие только в водных растворах, но образующие очень устойчивые соли — хроматы и дихроматы соответственно. Хроматы окрашивают раствор в желтый цвет; дихроматы — в оранжевый.
Кислоты образуются в результате взаимодействия с водой триоксида хрома — если вода присутствует в избытке, образуется хромовая кислота, если в недостатке — дихромовая:
CrO3+H2O(изб) = H2CrO4
2CrO3+H2O(нед) = H2Cr2O7
Примечательно, что хромат-ионы и дихромат-ионы при изменении среды растворов без проблем переходят друг в друга, меняя при этом окраску раствора:
- в кислой среде хроматы переходят в дихроматы, меняя желтый цвет раствора на оранжевый:
2CrO4 2- +2H + ↔ Cr2O7 2- +H2O
2K2CrO4+H2SO4 ↔ K2Cr2O7+K2SO4+H2O - в щелочной среде все происходит наоборот — дихроматы переходят в хроматы, а оранжевый цвет раствора меняется на желтый:
Cr2O7 2- +2OH — ↔ 2CrO4 2- +H2O
K2Cr2O7+2KOH = 2K2CrO4+H2O
Хроматы получают сплавлением хромистого железняка или оксида хрома (III) с карбонатами в присутствии кислорода (t=1000°C):
4Fe(CrO2)2+8Na2CO3+7O2 = 8Na2CrO4+2Fe2O3+8CO2
Дихроматы получают из растворов хроматов, подкисляя их.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Составление уравнений в ионно-молекулярной форме
S 2 — + MnO4 2- + 2H2O = MnO2 + S 0 + 4OH —
После приведения членов обеих частей уравнения, получим:
Уравнение в ионно-молекулярной форме:
4K + + S 2- + MnO4 2- + 2H2O = S + MnO2 + 4K + + 4OH — .
После приведения членов обеих частей уравнения, получим:
Уравнение в ионно-молекулярной форме:
После приведения членов обеих частей уравнения, получим:
Для уравнивания добавим в уравнение 1 моль K2SO4, получим:
Уравнение в ионно-молекулярной форме:
После приведения членов обеих частей уравнения, получим:
Уравнение в ионно-молекулярной форме:
3Zn 0 + AsO3 3- + 6H + = 3Zn 2+ + As 3- + 3H2O.
После приведения членов обеих частей уравнения, получим:
http://prosto-o-slognom.ru/chimia/516_oksidy_hroma.html
http://buzani.ru/zadachi/khimiya-glinka/1213-uravneniya-v-ionno-molekulyarnoj-forme-zadachi-631-632