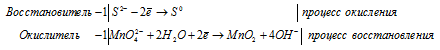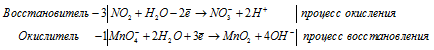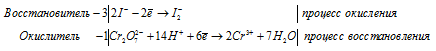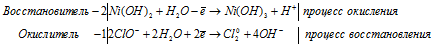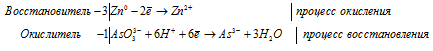Занятие элективного курса «Хром и его соединения»
Разделы: Химия
Цель: углубить знания учащихся по теме занятия.
- дать характеристику хрома как простого вещества;
- познакомить учащихся с соединениями хрома разной степени окисления;
- показать зависимость свойств соединений от степени окисления;
- показать окислительно – восстановительные свойства соединений хрома;
- продолжить формирование умений учащихся записывать уравнения химических реакций в молекулярном и ионном виде, составлять электронный баланс;
- продолжить формирование умений наблюдать химический эксперимент.
Форма занятия: лекция с элементами самостоятельной работы учащихся и наблюдением за химическим экспериментом.
I. Повторение материала предыдущего занятия.
1. Ответить на вопросы и выполнить задания:
— Какие элементы относятся к подгруппе хрома?
— Написать электронные формулы атомов
— К какому типу элементов относятся?
— Какие степени окисления проявляют в соединениях?
— Как изменяется радиус атомов и энергия ионизации от хрома к вольфраму?
Можно предложить заполнить учащимся заполнить таблицу, используя табличные величины радиусов атомов, энергии ионизации и сделать выводы.
| Элемент | Электронные формулы | Радиус атома нм | Энергия ионизации эВ | Степень окисления |
| хром | …3s 2 3p 6 3d 5 4s 1 | 0,125 | 6,76 | +2,+3,+6 |
| молибден | …4s 2 4p 6 4d 5 5s 1 | 0,136 | 7,10 | +3,+4,+5,+6 |
| вольфрам | …5s 2 5p 6 5d 4 6s 2 | 0,140 | 7,98 | +3,+4,+5,+6 |
2. Заслушать сообщение учащегося по теме «Элементы подгруппы хрома в природе, получение и применение».
- Хром.
- Соединения хрома. (2)
- Оксид хрома; (2)
- Гидроксид хрома. (2)
- Соединения хрома. (3)
- Оксид хрома; (3)
- Гидроксид хрома. (3)
- Соединения хрома (6)
- Оксид хрома; (6)
- Хромовая и дихромовая кислоты.
- Зависимость свойств соединений хрома от степени окисления.
- Окислительно – восстановительные свойства соединений хрома.
Хром – это белый с голубоватым отливом блестящий металл, очень твердый (плотность 7, 2 г/см 3 ), температура плавления 1890˚С.
Химические свойства: хром при обычных условиях неактивный металл. Это объясняется тем, что его поверхность покрыта оксидной пленкой (Сr2О3). При нагревании оксидная пленка разрушается, и хром реагирует с простыми веществами при высокой температуре:
Задание: составить уравнения реакций хрома с азотом, фосфором, углеродом и кремнием; к одному из уравнений составить электронный баланс, указать окислитель и восстановитель.
Взаимодействие хрома со сложными веществами:
При очень высокой температуре хром реагирует с водой:
Задание: составить электронный баланс, указать окислитель и восстановитель.
Хром реагирует с разбавленной серной и соляной кислотами:
Задание: составить электронный баланс, указать окислитель и восстановитель.
Концентрированные серная соляная и азотная кислоты пассивируют хром.
2. Соединения хрома. (2)
1. Оксид хрома (2) — СrО – твердое ярко – красное вещество, типичный основной оксид (ему соответствует гидроксид хрома (2) — Сr(ОН)2), не растворяется в воде, но растворяется в кислотах:
Задание: составить уравнение реакции в молекулярном и ионном виде взаимодействия оксида хрома (2) с серной кислотой.
Оксид хрома (2) легко окисляется на воздухе:
Задание: составить электронный баланс, указать окислитель и восстановитель.
Оксид хрома (2) образуется при окислении амальгамы хрома кислородом воздуха:
2Сr (амальгама) + О2 = 2СrО
2. Гидроксид хрома (2) — Сr(ОН)2 – вещество желтого цвета, плохо растворимо в воде, с ярко выраженным основным характером, поэтому взаимодействует с кислотами:
Задание: составить уравнения реакций в молекулярном и ионном виде взаимодействия оксида хрома (2) с соляной кислотой.
Как и оксид хрома (2), гидроксид хрома (2) окисляется:
Задание: составить электронный баланс, указать окислитель и восстановитель.
Получить гидроксид хрома (2) можно при действии щелочей на соли хрома (2):
Задание: составить ионные уравнения.
3. Соединения хрома. (3)
1. Оксид хрома (3) — Сr2О3 – порошок темно – зеленого цвета, нерастворим в воде, тугоплавкий, по твёрдости близок к корунду (ему соответствует гидроксид хрома (3) – Сr(ОН)3). Оксид хрома (3) имеет амфотерный характер, однако в кислотах и щелочах растворяется плохо. Реакции со щелочами идут при сплавлении:
Задание: составить уравнение реакции в молекулярном и ионном виде взаимодействия оксида хрома (3) с гидроксидом лития.
С концентрированными растворами кислот и щелочей взаимодействует с трудом:
Задание: составить уравнения реакций в молекулярном и ионном виде взаимодействия оксида хрома (3) с конценрированной серной кислотой и концентрированным раствором гидроксида натрия.
Оксид хрома (3) может быть получен при разложении дихромата аммония:
2. Гидроксид хрома (3) Сr(ОН)3 получают при действии щелочей на на растворы солей хрома (3):
Задание: составить ионные уравнения
Гидроксид хрома (3) представляет собой осадок серо – зеленого цвета, при получении которого, щелочь надо брать в недостатке. Полученный таким образом гидроксид хрома (3), в отличие от соответствующего оксида легко взаимодействует с кислотами и щелочами, т.е. проявляет амфотерные свойства:
Задание: составить уравнения реакций в молекулярном и ионном виде взаимодействия гидроксида хрома (3) с соляной кислотой и гидроксидом натрия.
При сплавлении Сr(ОН)3 со щелочами получаются метахромиты и ортохромиты:
4. Соединения хрома. (6)
1. Оксид хрома (6) — СrО3 – темно – красное кристаллическое вещество, хорошо растворимо в воде – типичный кислотный оксид. Этому оксиду соответствует две кислоты:
- СrО3 + Н2О = Н2СrО4(хромовая кислота – образуется при избытке воды)
- СrО3 + Н2О =Н2Сr2О7(дихромовая кислота – образуется при большой концентрации оксида хрома (3)).
Оксид хрома (6) – очень сильный окислитель, поэтому энергично взаимодействует с органическими веществами:
Окисляет также иод, серу, фосфор, уголь:
Задание: составить уравнения химических реакций оксида хрома (6) с йодом, фосфором, углем; к одному из уравнений составить электронный баланс, указать окислитель и восстановитель
При нагревании до 250 0 С оксид хрома (6) разлагается:
Оксид хрома (6) можно получить при действии концентрированной серной кислоты на твердые хроматы и дихроматы:
2. Хромовая и дихромовая кислоты.
Хромовая и дихромовая кислоты существуют только в водных растворах, образуют устойчивые соли, соответственно хроматы и дихроматы. Хроматы и их растворы имеют желтую окраску, дихроматы – оранжевую.
Хромат — ионы СrО4 2- и дихромат – ионы Сr 2О7 2- легко переходят друг в друга при изменении среды растворов
В кислой среде раствора хроматы переходят в дихроматы:
В щелочной среде дихроматы переходят в хроматы:
При разбавлении дихромовая кислота переходит в хромовую кислоту:
5. Зависимость свойств соединений хрома от степени окисления.
| Степень окисления | +2 | +3 | +6 |
| Оксид | СrО | Сr2О3 | СrО3 |
| Характер оксида | основной | амфотерный | кислотный |
| Гидроксид | Сr(ОН)2 | Сr(ОН)3 – Н3СrО3 | Н2СrО4 |
Н2Сr2О7
→ ослабление основных свойств и усиление кислотных→
6. Окислительно – восстановительные свойства соединений хрома.
Реакции в кислотной среде.
В кислотной среде соединения Сr +6 переходят в соединения Сr +3 под действием восстановителей: H2S, SO2, FeSO4
1. Уравнять уравнение реакции методом электронного баланса, указать окислитель и восстановитель:
2. Дописать продукты реакции, уравнять уравнение методом электронного баланса, указать окислитель и восстановитель:
Реакции в щелочной среде.
В щелочной среде соединения хрома Сr +3 переходят в соединения Сr +6 под действием окислителей: J2, Br2, Cl2, Ag2O, KClO3, H2O2, KMnO4:
- 2KCrO2 +3 Br 2 +8NaOH =2Na2CrO4 + 2KBr +4NaBr + 4H2O
- Cr +3 — 3e → Cr +6
- Br2 0 +2e → 2Br —
Уравнять уравнение реакции методом электронного баланса, указать окислитель и восстановитель:
Дописать продукты реакции, уравнять уравнение методом электронного баланса, указать окислитель и восстановитель:
Таким образом, окислительные свойства последовательно усиливаются с изменением степеней окисления в ряду: Cr +2 → Сr +3 → Сr +6 . Соединения хрома (2) — сильные восстановители, легко окисляются, превращаясь в соединения хрома (3). Соединения хрома (6) – сильные окислители, легко восстанавливаются в соединения хрома (3). Соединения хрома (3) при взаимодействии с сильными восстановителями проявляют окислительные свойства, переходя в соединения хрома (2), а при взаимодействии с сильными окислителями проявляют восстановительные свойства, превращаясь в соединеня хрома (6)
К методике проведения лекции:
- Для активизации познавательной деятельности учащихся и поддержания интереса, целесообразно в ходе лекции проводить демонстрационный эксперимент. В зависимости от возможностей учебной лаборатории можно демонстрировать учащимся следующие опыты:
- получении оксида хрома (2) и гидроксида хрома (2), доказательство их основных свойств;
- получение оксида хрома (3) и гидроксида хрома (3), доказательство их амфотерных свойств;
- получение оксида хрома (6) и растворение его в воде (получение хромовой и дихромовой кислот);
- переход хроматов в дихроматы, дихроматов в хроматы.
- Задания самостоятельной работы можно дифференцировать с учетом реальных учебных возможностей учащихся.
- Завершить лекцию можно выполнением следующих заданий: напишите уравнения химических реакций с помощью которых можно осуществить следующие превращения:
- Cr→ CrCl2→ Cr(OH)2→ Cr(OH)3→ Cr(NO3)3→ Cr2O3→ Cr
- Cr →Cr(NO3)3→ Cr(OH)3→ K3[Cr(OH)6]→ Cr(OH)3→ CrCl3
- Cr2(SO4)3→ Cr(OH)3→ CrCl3
.III. Домашнее задание: доработать лекцию (дописать уравнения химических реакций)
Перечень рекомендуемой литературы:
- Васильева З.Г. Лабораторные работы по общей и неорганической химии. -М.: «Химия», 1979 – 450 с.
- Егоров А.С. Репетитор по химии. – Ростов-на-Дону: «Феникс», 2006.-765 с.
- Кудрявцев А.А. Составление химических уравнений. — М., «Высшая школа», 1979. — 295 с.
- Петров М.М. Неорганическая химия. – Ленинград: «Химия», 1989. – 543 с.
- Ушкалова В.Н. Химия: конкурсные задания и ответы. — М.: «Просвещение», 2000. – 223 с.
Составление уравнений в ионно-молекулярной форме
S 2 — + MnO4 2- + 2H2O = MnO2 + S 0 + 4OH —
После приведения членов обеих частей уравнения, получим:
Уравнение в ионно-молекулярной форме:
4K + + S 2- + MnO4 2- + 2H2O = S + MnO2 + 4K + + 4OH — .
После приведения членов обеих частей уравнения, получим:
Уравнение в ионно-молекулярной форме:
После приведения членов обеих частей уравнения, получим:
Для уравнивания добавим в уравнение 1 моль K2SO4, получим:
Уравнение в ионно-молекулярной форме:
После приведения членов обеих частей уравнения, получим:
Уравнение в ионно-молекулярной форме:
3Zn 0 + AsO3 3- + 6H + = 3Zn 2+ + As 3- + 3H2O.
После приведения членов обеих частей уравнения, получим:
Составьте электронно-ионные схемы и молекулярные уравнения реакций. Укажите окислитель и восстановитель. 275 а) Cr2O3 + KClO3 + KOH → CrO4 2—






Чтобы получить решение , напишите мне в WhatsApp , оплатите, и я Вам вышлю файлы.
Кстати, если эта работа не по вашей теме или не по вашим данным , не расстраивайтесь, напишите мне в WhatsApp и закажите у меня новую работу , я смогу выполнить её в срок 1-3 дня!
Описание и исходные данные задания, 50% решения + фотография:
Составьте электронно-ионные схемы и молекулярные уравнения реакций. Укажите окислитель и восстановитель. Две реакции (а,б) для каждого задания.
275 а ) Cr2O3 + KClO3 + KOH → CrO4 2— , Cl —
б ) FeCl2 +HNO3 + HCl → Fe 3+ , N2O
Решение :
1 ClO 3 — + 6 ē + 3 H 2 O = Cl — + 6ОН —
| Изучите химию на странице ➔ решение заданий и задач по химии. |
| Похожие готовые решения: |
- Используя потенциалы (табл. П.6, П.7, П.8), допишите уравнения реакций (по две для каждого варианта). 295. а) Fe + H2SO4 (конц.) → Т 0 Fe3+ б) Al + H2O
- Для предложенных гальванических элементов рассчитайте электродные потенциалы и ЭДС. Zn / Zn(NO3)2, 0,001 M // Zn(NO3)2 / Zn
- Напишите в молекулярной и ионной формах уравнения реакций совместного гидролиза предложенных солей. 235. NH4NO3 + Na2SiO3
- Рассчитайте и укажите степень окисления (CO) атомов элементов в предложенных частицах. 255. ClO4—, Cl —, CrO2—, F2
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.
http://buzani.ru/zadachi/khimiya-glinka/1213-uravneniya-v-ionno-molekulyarnoj-forme-zadachi-631-632
http://natalibrilenova.ru/sostavte-elektronno-ionnyie-shemyi-i-molekulyarnyie-uravneniya-reaktsij-ukazhite-okislitel-i-vosstanovitel-275-a-cr2o3—kclo3—koh—cro4-2-/