PH3 + BR2 + H2O = H3PO4 + HBR ЭЛЕКТРОННЫЙ БАЛАН(окислитель восстановитель)?
Химия | 10 — 11 классы
PH3 + BR2 + H2O = H3PO4 + HBR ЭЛЕКТРОННЫЙ БАЛАН(окислитель восстановитель).
P⁻³ H₃⁺¹ + Br₂⁰ + H₂⁺¹ O⁻² = H₃⁺¹ P⁺⁵ O₄⁻² + H⁺¹ Br⁻¹
P⁻³ — 8e→ P⁺⁵ — восстановитель | 1
2Br⁰ + 2e→ Br⁻¹ — окислитель | 4
PH₃ + 4Br₂ + 4H₂O = H₃PO₄ + 8HBr.
Используя метод электронного баланса, составьте уравнение реакцииHNO3 + Cu → Cu(NO3)2 + NO + H2OОпределите окислитель и восстановитель?
Используя метод электронного баланса, составьте уравнение реакции
HNO3 + Cu → Cu(NO3)2 + NO + H2O
Определите окислитель и восстановитель.
Используя метод электронного баланса, составьте уравнение реакции
CrO3 + HBr → CrBr3 + Br2 + H2O
Определите окислитель и восстановитель
Используя метод электронного баланса, составьте уравнение реакции
I2 + HNO3 → HIO3 + NO + H2O
Определите окислитель и восстановитель.
Используя метод электронного баланса, составьте уравнение реакции HBr + HNO3 → NO + Br2 + H2O Определите окислитель и восстановитель?
Используя метод электронного баланса, составьте уравнение реакции HBr + HNO3 → NO + Br2 + H2O Определите окислитель и восстановитель.
Составь уравнение электронного баланса окислитель и восстановитель?
Составь уравнение электронного баланса окислитель и восстановитель.
В схеме химической реакции Н2 + Br2 = HBr расставьте коэфициенты ; укажите окислитель и восстановитель, составьте схему перехода электронов?
В схеме химической реакции Н2 + Br2 = HBr расставьте коэфициенты ; укажите окислитель и восстановитель, составьте схему перехода электронов.
Используя метод электронного баланса составьте уравнение HBr + HNO3 = NO2 + HBrO3 + H2O?
Используя метод электронного баланса составьте уравнение HBr + HNO3 = NO2 + HBrO3 + H2O.
H2SO3 + Br + H2O→H2SO4 + HBr баланс электронная?
H2SO3 + Br + H2O→H2SO4 + HBr баланс электронная.
Al(OH) + HPO = AlPO + HO коеффициенты?
Al(OH) + HPO = AlPO + HO коеффициенты.
Cl2O + HBr =Написать уравнение реакции и расставить коэффициенты с помощью метода электронного баланса?
Написать уравнение реакции и расставить коэффициенты с помощью метода электронного баланса.
NO₃ — = nh4 + окислитель или восстановитель , сколько электронов?
NO₃ — = nh4 + окислитель или восстановитель , сколько электронов.
Используя метод электронного баланса, составьте уравнение реакцииBr2 + KI + H2O → KIO3 + HBr Определите окислитель и восстановитель?
Используя метод электронного баланса, составьте уравнение реакции
Br2 + KI + H2O → KIO3 + HBr Определите окислитель и восстановитель.
Вы находитесь на странице вопроса PH3 + BR2 + H2O = H3PO4 + HBR ЭЛЕКТРОННЫЙ БАЛАН(окислитель восстановитель)? из категории Химия. Уровень сложности вопроса рассчитан на учащихся 10 — 11 классов. На странице можно узнать правильный ответ, сверить его со своим вариантом и обсудить возможные версии с другими пользователями сайта посредством обратной связи. Если ответ вызывает сомнения или покажется вам неполным, для проверки найдите ответы на аналогичные вопросы по теме в этой же категории, или создайте новый вопрос, используя ключевые слова: введите вопрос в поисковую строку, нажав кнопку в верхней части страницы.
AgCl молярная масса = 108 + 35, 5 = 143, 5г / моль в 143, 5г хлорида содержится 35, 5 г хлора в 0, 5413 г — хг х = 0, 5413 * 35, 5 / 143, 5 = 0, 1339 г.
Ba(OH)2 + CuCL2 — — >BaCL + Cu(OH)2↓ 2OH — + Cu²⁺ — — >Cu(OH)2 Mg(NO3)2 + CaCL2≠ Na2CO3 + H2SO4 — — >Na2SO4 + H2O + CO2 CO⁻²₃ + 2H⁺ — — >H2O + CO2.
Дано : m(C) = 250 r + H2 Найти : V(CH4) — ? M(C) = 12 г / моль n = m / M n = 250 г / 12 г / моль = 20, 833 моль Vm = 22, 4 л / моль С + 2Н2 = СН4 Из УХР следует, что n(CH4) = n(C) n(CH4) = 20, 833 моль V = n * Vm V(CH4) = 20, 833 моль * 22, 4 л / мо..
Дано m(C) = 250 g H2 — — — — — — — — — — — — — — — V(CH4) — ? 250 X C + 2H2 — — >CH4 M(C) = 12 g / mol , Vm = 22. 4L / mol 12 22. 4 X = 250 * 22. 4 / 12 X = 466. 67 L ответ 466. 67 л.
1. 5NaI + NaIO3 + 3H2SO4 = 3I2 + 3Na2SO4 + 3H2O 2. 3KNO2 + KCLO3 = KCL + 3KNO3 4. 3C + 4HNO3 = 3CO2 + 4NO + 2H2O.
SiO₂ + 2Mg = Si + 2MgO 2Ca (изб. ) + Si = Ca₂Si Ca₂Si + 4HCl = CaCl₂ + SiH₄↑ SiH₄ + 2O₂ = SiO₂ + 2H₂O SiO₂ + 2Mg = Si + 2MgO.
Дано : m(Fe2O3) = 16 г Найти : V(H2) — ? M(Fe2O3) = 160 г / моль n(Fe2O3) = m / M = 16 г / 160 г / моль = 0, 1 моль Fe2O3 + 3H2 = 2Fe + 3H2O Из УХР следует, что n(H2) = 3n(Fe2O3) n(H2) = 3 * 0. 1 моль = 0, 3 моль V(H2) = n * Vm = 0, 3 моль * 22, 4 ..
Решение на листочке — — — — — — — -.
Хл 0, 5моль Н2 + CI2 = 2HCI Х = 22, 4 * 0, 5 22, 4л 1моль — — — — — — — — — — — = 11, 2 л.
Метод электронного баланса и ионно-электронный метод (метод полуреакций)
Спецификой многих ОВР является то, что при составлении их уравнений подбор коэффициентов вызывает затруднение.
Для облегчения подбора коэффициентов чаще всего используют метод электронного баланса и ионно-электронный метод (метод полуреакций). Рассмотрим применение каждого из этих методов на примерах.
Метод электронного баланса
В его основе метода электронного баланса лежит следующее правило: общее число электронов, отдаваемое атомами-восстановителями, должно совпадать с общим числом электронов, которые принимают атомы-окислители .
В качестве примера составления ОВР рассмотрим процесс взаимодействия сульфита натрия с перманганатом калия в кислой среде.
1) Составить схему реакции:
Записать исходные вещества и продукты реакции, учитывая, что в кислой среде MnO4 — восстанавливается до Mn 2+ (см. схему):
Найдем степень окисления элементов:
Из приведенной схемы понятно, что в процессе реакции происходит увеличение степени окисления серы с +4 до +6. S +4 отдает 2 электрона и является восстановителем. Степень окисления марганца уменьшилась от +7 до +2, т.е. Mn +7 принимает 5 электронов и является окислителем.
3) Составить электронные уравнения и найти коэффициенты при окислителе и восстановителе.
S +4 – 2e — = S +6 | 5 восстановитель, процесс окисления
Mn +7 +5e — = Mn +2 | 2 окислитель, процесс восстановления
Чтобы число электронов, отданных восстановителем, было равно числу электронов, принятых восстановителем, необходимо:
- Число электронов, отданных восстановителем, поставить коэффициентом перед окислителем.
- Число электронов, принятых окислителем, поставить коэффициентом перед восстановителем.
Таким образом, 5 электронов, принимаемых окислителем Mn +7 , ставим коэффициентом перед восстановителем, а 2 электрона, отдаваемых восстановителем S +4 коэффициентом перед окислителем:
4) Уравнять количества атомов элементов, не изменяющих степень окисления
Соблюдаем последовательность: число атомов металлов, кислотных остатков, количество молекул среды (кислоты или щелочи). В последнюю очередь подсчитывают количество молекул образовавшейся воды.
Итак, в нашем случае число атомов металлов в правой и левой частях совпадают.
По числу кислотных остатков в правой части уравнения найдем коэффициент для кислоты.
В результате реакции образуется 8 кислотных остатков SO4 2- , из которых 5 – за счет превращения 5SO3 2- → 5SO4 2- , а 3 – за счет молекул серной кислоты 8SO4 2- — 5SO4 2- = 3SO4 2- .
Таким образом, серной кислоты надо взять 3 молекулы:
Аналогично, находим коэффициент для воды по числу ионов водорода, во взятом количестве кислоты
6H + + 3O -2 = 3H2O
Окончательный вид уравнения следующий:
Признаком того, что коэффициенты расставлены правильно является равное количество атомов каждого из элементов в обеих частях уравнения.
Ионно-электронный метод (метод полуреакций)
Реакции окисления-восстановления, также как и реакции обмена, в растворах электролитов происходят с участием ионов. Именно поэтому ионно-молекулярные уравнения ОВР более наглядно отражают сущность реакций окисления-восстановления.
При написании ионно-молекулярных уравнений, сильные электролиты записывают в виде ионов, а слабые электролиты, осадки и газы записывают в виде молекул (в недиссоциированном виде).
При написании полуреакций в ионной схеме указывают частицы, подвергающиеся изменению их степеней окисления, а также характеризующие среду, частицы:
H + — кислая среда, OH — — щелочная среда и H2O – нейтральная среда.
Пример 1.
Рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в кислой среде.
1) Составить схему реакции:
Записать исходные вещества и продукты реакции:
2) Записать уравнение в ионном виде
В уравнении сократим те ионы, которые не принимают участие в процессе окисления-восстановления:
SO3 2- + MnO4 — + 2H + = Mn 2+ + SO4 2- + H2O
3) Определить окислитель и восстановитель и составить полуреакции процессов восстановления и окисления.
В приведенной реакции окислитель — MnO4 — принимает 5 электронов восстанавливаясь в кислой среде до Mn 2+ . При этом освобождается кислород, входящий в состав MnO4 — , который, соединяясь с H + образует воду:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O
Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона. Как видно образовавшийся ион SO4 2- содержит больше кислорода, чем исходный SO3 2- . Недостаток кислорода восполняется за счет молекул воды и в результате этого происходит выделение 2H + :
SO3 2- + H2O — 2e — = SO4 2- + 2H +
4) Найти коэффициенты для окислителя и восстановителя
Необходимо учесть, что окислитель присоединяет столько электронов, сколько отдает восстановитель в процессе окисления-восстановления:
MnO4 — + 8H + + 5e — = Mn 2+ + 4H2O |2 окислитель, процесс восстановления
SO3 2- + H2O — 2e — = SO4 2- + 2H + |5 восстановитель, процесс окисления
5) Просуммировать обе полуреакции
Предварительно умножая на найденные коэффициенты, получаем:
2MnO4 — + 16H + + 5SO3 2- + 5H2O = 2Mn 2+ + 8H2O + 5SO4 2- + 10H +
Сократив подобные члены, находим ионное уравнение:
2MnO4 — + 5SO3 2- + 6H + = 2Mn 2+ + 5SO4 2- + 3H2O
6) Записать молекулярное уравнение
Молекулярное уравнение имеет следующий вид:
Пример 2.
Далее рассмотрим пример составления уравнения реакции между сульфитом натрия и перманганатом калия в нейтральной среде.
В ионном виде уравнение принимает вид:
Также, как и предыдущем примере, окислителем является MnO4 — , а восстановителем SO3 2- .
В нейтральной и слабощелочной среде MnO4 — принимает 3 электрона и восстанавливается до MnО2. SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + 2H2O + 3e — = MnО2 + 4OH — |2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O |3 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
Пример 3.
Составление уравнения реакции между сульфитом натрия и перманганатом калия в щелочной среде.
В ионном виде уравнение принимает вид:
В щелочной среде окислитель MnO4 — принимает 1 электрон и восстанавливается до MnО4 2- . Восстановитель SO3 2- — окисляется до SO4 2- , отдав 2 электрона.
Полуреакции имеют следующий вид:
MnO4 — + e — = MnО2 |2 окислитель, процесс восстановления
SO3 2- + 2OH — — 2e — = SO4 2- + H2O |1 восстановитель, процесс окисления
Запишем ионное и молекулярное уравнения, учитывая коэффициенты при окислителе и восстановителе:
Необходимо отметить, что не всегда при наличии окислителя и восстановителя, возможно самопроизвольное протекание ОВР. Поэтому для количественной характеристики силы окислителя и восстановителя и для определения направления реакции пользуются значениями окислительно-восстановительных потенциалов.
Еще больше примеров составления окислительно-восстановительных реакций приведены в разделе Задачи к разделу Окислительно-восстановительные реакции. Также в разделе тест Окислительно-восстановительные реакции
Окислительно-восстановительные реакции

Процессы, протекающие в природе и осуществляемые человеком, в большинстве своём представляют ОВР. Такие важнейшие процессы, как дыхание, обмен веществ, фотосинтез (6CO2+H2O = C6H12O6 + 6O2), — всё это ОВР.
В промышленности с помощью ОВР получают аммиак, серную, соляную кислоты и многое другое.
Восстановление металлов из руд — фактически основа всей металлургической промышленности — тоже окислительно-восстановительные процессы. Например, реакция получения железа из гематита: 2Fe2O3 + 3С = 4Fe+3CO2.
Окислители и восстановители: характеристика

Говорят, что окислители, принимая электроны, восстанавливаются, а восстановители — окисляются в процессе отдачи электронов.
Важнейшие представители окислителей и восстановителей представлены в следующей таблице:
| Типичные окислители | Типичные восстановители |
| Простые вещества, состоящие из элементов с высокой электроотрицательностью (неметаллы): йод, фтор, хлор, бром, кислород, озон, сера и т. п. | Простые вещества, состоящие из атомов элементов с низкой электроотрицательностью (металлы или неметаллы): водород H2, углерод C (графит), цинк Zn, алюминий Al, кальций Ca, барий Ba, железо Fe, хром Cr и так далее. |
Молекулы или ионы, содержащие в составе атомы металлов или неметаллов с высокими степенями окисления:
| Молекулы или ионы, имеющие в своём составе атомы металлов или неметаллов с низкими степенями окисления:
|
| Ионные соединения, содержащие катионы некоторых металлов с высокими СО: Pb3+, Au3+, Ag+, Fe3+ и другие. | Органические соединения: спирты, кислоты, альдегиды, сахара. |

Как определить, является атом окислителем или восстановителем: достаточно записать СО и понять, какие атомы её увеличили впроцессе реакции (восстановители), а какие уменьшили (окислители).
Вещества с двойственной природой
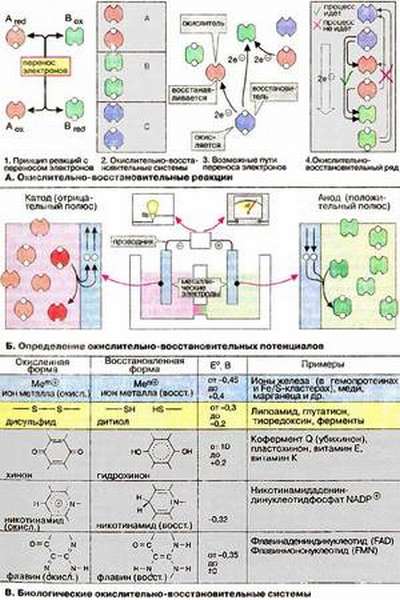
Примером может быть пероксид водорода. Содержащийся в его составе кислород в СО -1 может как принять электрон, так и отдать его.
При взаимодействии с восстановителем пероксид проявляет окислительные свойства, а с окислителем — восстановительные.
Рассмотреть подробнее можно при помощи следующих примеров:
- восстановление (пероксид выступает как окислитель) при взаимодействии с восстановителем,
SO2 + H2O2 = H2SO4
- окисление (пероксид является в этом случае восстановителем) при взаимодействии с окислителем.
2KMnO4 + 5H2O2 + 3H2SO4 = 2MnSO4 + 5О2 + K2SO4 + 8H2O
Классификация ОВР: примеры
Различают следующие типы окислительно-восстановительных реакций:
- межмолекулярное окисление-восстановление (окислитель и восстановитель находятся в составе разных молекул),
- внутримолекулярное окисление-восстановление (окислитель находится в составе той же молекулы, что и восстановитель),
- диспропорционирование (окислителем и восстановителем является атом одного и того же элемента),
- репропорционирование (окислитель и восстановитель образуют в результате реакции один продукт).
Примеры химических превращений, относящихся к различным типам ОВР:
- Внутримолекулярные ОВР — это чаще всего реакции термического разложения вещества:
2KCLO3 = 2KCl + 3O2
(NH4)2Cr2O7 = N2 + Cr2O3 + 4H2O
2NaNO3 = 2NaNO2 + O2
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
2Al + Fe2O3 = Al2O3 + 2Fe
3Br2 + 6KOH = 5KBr + KBrO3 + 6H2O
3HNO2 = HNO3 + 2NO + H2O
2NO2 + H2O = HNO3 + HNO2
4KClO3 = KCl + 3KClO4
2H2S + SO2 = 3S + 2H2O
HOCl + HCl = H2O + Cl2
Токовые и бестоковые ОВР

Первый случай — это получение электрической энергии за счёт химической реакции (такие источники энергии могут использоваться в двигателях машин, в радиотехнических устройствах, приборах управления), либо электролиз, то есть химическая реакция, наоборот, возникает за счёт электроэнергии (с помощью электролиза можно получать различные вещества, обрабатывать поверхности металлов и изделий из них).
Примерами бестоковых ОВР можно назвать процессы горения, коррозии металлов, дыхания и фотосинтеза и т.д.
Метод электронного баланса ОВР в химии
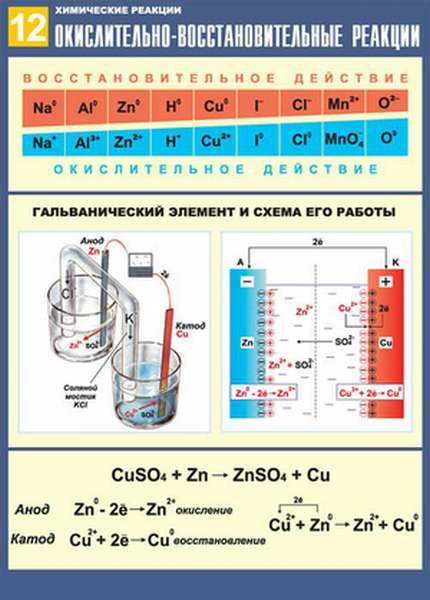
Основывается метод на том, что сумма принимаемых окислителем электронов и количество отдаваемых восстановителем приводится к равновесию.
Метод складывается из нескольких этапов:
- Записывается уравнение реакции.
- Определяются СО элементов.
- Определяются элементы, которые в результате реакции изменили свои степени окисления. Отдельно записываются полуреакции окисления и восстановления.
- Подбираются множители для уравнений полуреакций так, чтобы уравнять принятые в полуреакции восстановления и отданные в полуреакции окисления электроны.
- Подобранные коэффициенты проставляются в уравнение реакции.
- Подбираются остальные коэффициенты реакции.
На простом примере взаимодействия алюминия с кислородом удобно написать уравнивание поэтапно:
- Уравнение: Al + O2 = Al2О3
- СО у атомов в простых веществах алюминия и кислорода равны 0.
Al0 + O20 = Al+32O-23
- Подбираем коэффициенты, при умножении на которые сравняется количество принятых и количество отданных электронов будет одинаковым:
Al0 -3е = Al+3 коэффициент 4,
O20 +4e = 2O-2 коэффициент 3.
- Проставляем коэффициенты в схему реакции:
4Al + 3O2 = Al2O3
- Видно, что для уравнивания всей реакции достаточно поставить коэффициент перед продуктом реакции:
4Al + 3O2 = 2Al2O3
Примеры заданий на составление электронного баланса
Могут встречаться следующие задания на уравнивания ОВР:
- Взаимодействие перманганата калия с хлоридом калия в кислой среде с выделением газообразного хлора.
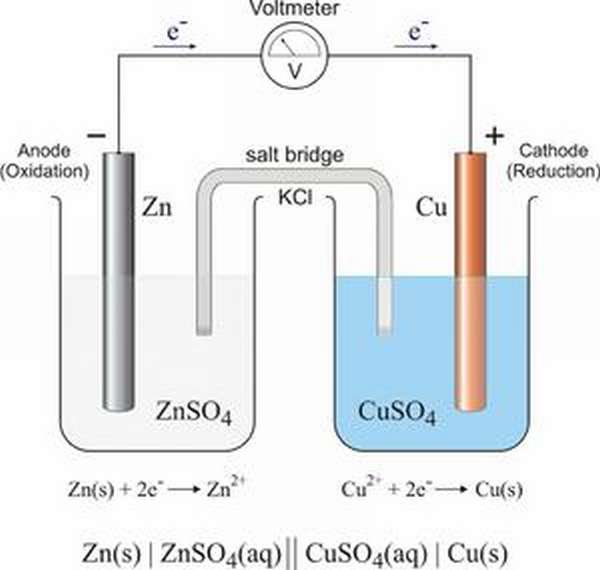
KCl + KMnO4 + H2SO4 = Cl2 + MnSO4 + K2SO4 + H2O
K+1Cl-1 + K+1Mn+7O4-2 + H2+1S+6O4-2 = Cl20 + Mn+2S+6O4-2 + K2+1S+6O4-2 + H2+1O-2
Как видно после расстановки СО, атомы хлора отдают электроны, повышая свою СО до 0, а атомы марганца электроны принимают:
Mn+7 +5е = Mn+2 множитель два,
2Cl-1 -2е = Cl20 множитель пять.
Проставляем в уравнение коэффициенты в соответствии с подобранными множителями:
10K+1Cl-1 + 2K+1Mn+7O4-2 +H2SO4 = 5Cl20 + 2Mn+2S+6O4-2 + K2SO4 + H2O
Уравниваем количество остальных элементов:
10KCl + 2KMnO4 + 8H2SO4 = 5Cl2 + 2MnSO4 + 6K2SO4 + 8H2O
- Взаимодействие меди (Cu) с концентрированной азотной кислотой(HNO3) с выделением газообразного оксида азота (NO2):
Cu + HNO3(конц.) = NO2 + Cu(NO3)2 + 2H2O
Cu0 + H+1N+5O3-2 = N+4O2 + Cu+2(N+5O3-2)2 + H2+1O-2
Как видно, атомы меди повышают свою СО с нуля до двух, а атомы азота — снижают с +5 до +4
Cu0 -2е = Cu+2 множитель один,
N+5 +1е = N+4 множитель два.
Проставляем в уравнение коэффициенты:
Cu0 + 4H+1N+5O3-2 = 2N+4O2 + Cu+2(N+5O3-2)2 + H2+1O-2
Уравниваем остальные элементы:
Cu + 4HNO3(конц.) = 2NO2 + Cu (NO3)2 + 2H2O
- Взаимодействие дихромата калия с Н2S в кислой среде:
Запишем схему реакции, расставим СО:
К2+1Сr2+6О7-2 + Н2+1S-2 + Н2+1S+6O4-2 = S0 + Сr2+3(S+6O4-2)3 + K2+1S+6O4-2 + H2O
S-2 –2e = S0 коэффициент 3,
2Cr+6 +6e = 2Cr+3 коэффициент 1.
К2Сr2О7 + 3Н2S + Н2SО4 = 3S + Сr2(SО4)3 + K2SO4 + Н2О
Уравниваем остальные элементы:
К2Сr2О7 + 3Н2S +4Н2SО4 = 3S + Сr2(SО4)3 + K2SO4 + 7Н2О
Влияние реакционной среды
Характер среды влияет на протекание тех или иных ОВР. Роль реакционной среды можно проследить на примере взаимодействия перманганата калия (KMnO4) и сульфита натрия (Na2SO3) при различных значениях рН:
- Na2SO3 + KMnO4 = Na2SO4 + MnSO4 + K2SO4 (pH <,7 кислая среда),
- Na2SO3 + KMnO4 = Na2SO4 + MnO2 + KOH (pH =7 нейтральная среда),
- Na2SO3 + KMnO4 = Na2SO4 + K2MnO4 + H2O (pH >,7 щелочная среда).
Видно, что изменение кислотности среды приводит к образованию разных продуктов взаимодействия одних и тех же веществ. При изменении кислотности среды они происходят и для других реагентов, вступающих в ОВР. Аналогично показанным выше примерам реакции с участием дихромат-иона Cr2O72- будут проходить с образованием разных продуктов реакции в различных средах:
http://zadachi-po-khimii.ru/obshaya-himiya/metod-elektronnogo-balansa-ionno-elektronnyj-metod-metod-polureakcij.html
http://tvercult.ru/nauka/okislitelno-vosstanovitelnyie-reaktsii









