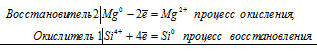Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6e1c3cc019414991 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
Оксид кремния (IV)
Оксид кремния (IV)
Физические свойства и нахождение в природе
Оксид кремния (IV) SiO2 – это твердое вещество с атомной кристаллической решеткой. В природе встречается в виде кварца, речного песка, кремнезема и прочих модификаций:
Химические свойства
Оксид кремния (IV) – типичный кислотный оксид . За счет кремния со степенью окисления +4 проявляет слабые окислительные свойства.
1. Как кислотный оксид, диоксид кремния (IV) взаимодействует с растворами и расплавами щелочей и в расплаве с основными оксидами . При этом образуются силикаты.
Например , диоксид кремния взаимодействует с гидроксидом калия:
Еще пример : диоксид кремния взаимодействует с оксидом кальция.
SiO2 + CaO → CaSiO3
2. Оксид кремния (IV) не взаимодействует с водой , т.к. кремниевая кислота нерастворима .
3. Оксид кремния (IV) реагирует при сплавлении с карбонатами щелочных металлов . При этом работает правило: менее летучий оксид вытесняет более летучий оксид из солей при сплавлении.
Например , оксид кремния (IV) взаимодействует с карбонатом калия. При этом образуется силикат калия и углекислый газ:
4. Из кислот диоксид кремния реагирует только с плавиковой или с газообразным фтороводородом:
5. При температуре выше 1000 °С оксид кремния реагирует с активными металлами, при этом образуется кремний.
Например , оксид кремния взаимодействует с магнием с образованием кремния и оксида магния:
SiO2 + 2Mg → Si + 2MgO
Видеоопыт взаимодействия оксида кремния (IV) с магнием можно посмотреть здесь.
При избытке восстановителя образуются силициды:
SiO2 + 4Mg → Mg2Si + 2MgO
6. Оксид кремния (IV) взаимодействует с неметаллами.
Например , оксид кремния (IV) реагирует с водородом в жестких условиях. При этом оксид кремния проявляет окислительные свойства:
Еще пример : оксид кремния взаимодействует с углеродом. При этом образуется карборунд и угарный газ:
SiO2 + 3С → SiС + 2СО
При сплавлении оксид кремния взаимодействует с фосфатом кальция и углем:
Степень окисления кремния. Применение кремниевых соединений
Решение задач на составление уравнений окислительно-восстановительных реакций кремниевых соединений
Задание 387
Какую степень окисления может проявлять кремний в своих соединениях? Составьте уравнения реакций, которые надо провести для осуществления следующих превращений:
МgSi → SiH4 → SiO2 → K2SiO3 → Н2SiO3
При каком превращении происходит окислительно-восстановительная реакция?
Решение:
Для кремния в своих соединениях характерна степень окисления +4.
Уравнения реакций следующих превращений:
б) Окислительно-восстановительной реакцией является реакция силана с водой.
Здесь кремний увеличивает свою степень окисления от -4 до +4, т. е. проявляет свойство восстановителя, а водород уменьшает свою степень окисления от +1 до 0, т. е. Проявляет свойство окислителя;
Задание 388
Какое применение находит кремний? Составьте уравнения реакций, которые надо провести для осуществления следующих превращений: SiO2 → Si → K2SiO3 → Н2SiO3
Окислительно-восстановительные реакции напишите на основании электронных уравнений.
Решение:
а) Применение кремниевых соединений
Кремний в больших количествах используется для получения динамной и трансформаторной стали, которые применяются для изготовления трансформаторов, электромоторов и генераторов. В химическом машиностроении применяют кремниевый чугун (15-17% Si), обладающий кислотоупорными свойствами. Ферросилиций служит добавкой в сталь при её выплавке, для удаления из неё кислорода (образуется SiO2, который уходит в шлак).
Особо чистый кремний применяют для изготовления полупроводниковых устройств (интегральные схемы, солнечные батареи и др.). Кварц используется для изготовления кварцевого стекла, выдерживающего нагревание до 1200 0 С и пропускающего ультрафиолетовое излучение. Изделие из кварца не растрескивается, даже если его нагреть до красного каления и, затем, опустить в холодную воду, благодаря ничтожно малому коэффициенту термического расширения.
Кристаллический кварц обладает пьезоэлектрическими свойствами. Широко используются кварцевые ультразвуковые вибраторы и эталоны частоты.
Огромное применение имеет стекло. Из него изготавливают стеклянные изделия, оконное стекло, посуду, строительные материалы, стекловолокно, стеклоткань и др. изделия.
Из кремния изготавливают ситаллы – материалы, обладающие химической стойкостью и высокой механической прочностью. Их изготавливают из металлургического шлака.
Цемент, керамика, огнеупоры, кирпичи, фаянс, фарфор, асбоцемент представляют собой материалы, содержащие оксид кремния.
Силикат натрия применяют для огнезащитного покрытия деревянных изделий, в производстве силикатных материалов. Фторокремниевую кислоту используют качестве дезинфицирующего средства.
Муллит – соединение в системе Al2O3 — SiO2, устойчивое при высоких температурах.
Цеолиты используют в качестве селективных адсорбентов при очистке и осушке газов (природный газ) и органических жидкостей (углеводороды).
SiH4 и SiCl4 используют для получения кремнийорганических соединений, из которых получают каучукоgодобные материалы, выдерживающие длительное нагревание до 250 0 С и сохраняющие эластичность даже при -60 0 С, клей, огнеупорные лаки и эмали, водоотталкивающие вещества для пропитки тканей, силиконовые смазки, протезные пластмассы, электроизоляционные материалы.
б) Уравнения реакций, которые надо провести для осуществления следующих превращений:
1) SiO2 + 2Mg = Si + 2MgO
2Mg 0 + Si 4+ = 2Mg 2+ + Si 0
SiO2 + 2Mg = Si + 2MgO
В данной реакции магний увеличивает свою степень окисления от 0 до +2, т. е. проявляет свойства восстановителя, а кремний уменьшает свою степень окисления от +4 до 0, т. е. проявляет свойства окислителя.
Si 0 + 4H + = Si 4+ + 2H2 0
В данной реакции кремний увеличивает свою степень окисления от 0 до +4, т. е. проявляет свойства восстановителя, а водород уменьшает свою степень окисления от + до 0, т. е. проявляет свойства окислителя.
В данной реакции кремний не изменяет свою степень окисления — реакция не является окислительно-восстановительной.
http://chemege.ru/oksid-kremniya-iv/
http://buzani.ru/zadachi/khimiya-shimanovich/985-kremnij-i-ego-soedineniya-zadaniya-387-388