Помогите,пожалуйста! Итоговая работа по химии.Кто,чем сможет)
Задание №1.
Даны уравнения трех химических реакций:
а) СО(r) + 2Н2(r) = СН3ОН(r) + Q (реакция обратимая,Cu,ZnO)
б) СН3СООН + С2Н5ОН = СН3СООС2Н5 + Н2О + Q ( реакция обратимая, Н+)
в) 4Р + 5О2 = 2Р2О5 + Q
Рассмотрите их,сопоставьте друг с другом и ответьте на вопросы:
1)Какое из низ соответствует следующей характеристике: реакция соединения,экзотермическая и т.д.?Дополните описание этой реакции.
2)Дайте полную характеристику реакции «Б».
3)В какую сторону сместиться химическое равновесие системы,записанной как уравнение «А», при: а)повышении давления; б) понижения температуры; в) увеличении концентрации водорода; Почему?
Задание №2.
Рассмотрите на конкретном примере зависимость скорости химической реакции от концентрации реагирующих веществ. Ответ подтвердите уравнением реакции.
Задание №3.
Допишите краткие ионные уравнения реакции гидролиза:
а) S(2-) + HOH = HS(-) + . ; (реакция обратимая)
б) Pd(2+) + НОН = . + . . (реакция обратимая).
Составьте соответствующие им молекулярные уравнения (для первой стадии гидролиза). Какова среда раствора в каждом случае?
Задание №4.
Чем различаются составы продуктов полного гидролиза сахарозы и крахмала? В какой среде ведут гидролиз этих веществ? Почему? Ответ подтвердите уравнениями реакций.
Контрольная работа по химии 11 класс
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Контрольная работа «Химические реакции»
А. Равновесие химических реакций.
Даны уравнения трех реакций:
б) 2 KClO 3 2 KCl + 3 O 2 ↑ — Q ;
Какое из них соответствует следующей характеристике: реакция соединения, экзотермическая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «в», при следующих воздействиях: а) повышение давления; б) повышение температуры; в) добавление в систему водорода?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции
2. Даны соли: хлорид алюминия, нитрат калия. При гидролизе одной из них среда становится щелочной. Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава иодида калия.
Рассчитайте массу воздуха необходимого для полного сжигания 12 куб. м метана.
Контрольная работа «Химические реакции»
Даны уравнения трех реакций:
Какое из них соответствует следующей характеристике: реакция соединения, эндотермическая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «а», при следующих воздействиях: а) понижение давления; б) понижение температуры; в) удаление метанола?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции реакции
Даны соли: хлорид алюминия, карбонат натрия . При гидролизе одной из них среда становится кислой . Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава хлорида меди( II )
Рассчитайте объем водорода, выделившегося при взаимодействии 60 г. алюминия содержащего 20% примесей с соляной кислотой.
Контрольная работа. «Химические реакции»
Даны уравнения трех реакций:
Какое из них соответствует следующей характеристике: реакция соединения, обратимая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «а», при следующих воздействиях: а) повышение давления; б) понижение температуры; в) удаление углекислого газа?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции
2. Даны соли: сульфат натрия , нитрат алюминия . При гидролизе одной из них среда становится щелочной. Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава хлорида бария.
Рассчитайте массу соли образовавшейся при взаимодействии технического железа массой 150 г. , с массовой долей чистого вещества 80%
Контрольная работа «Химические реакции»
А. Равновесие химических реакций.
Даны уравнения трех реакций:
б ) 2KClO 3 2KCl + 3O 2 ↑ — Q;
Какое из них соответствует следующей характеристике: реакция соединения, экзотермическая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «в», при следующих воздействиях: а) повышение давления; б) повышение температуры; в) добавление в систему водорода?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции
2. Даны соли: хлорид алюминия, нитрат калия. При гидролизе одной из них среда становится щелочной. Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава иодида калия.
Рассчитайте массу воздуха необходимого для полного сжигания 12 куб. м метана.
Контрольная работа «Химические реакции»
Даны уравнения трех реакций:
1. Какое из них соответствует следующей характеристике: реакция соединения, эндотермическая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «а», при следующих воздействиях: а) понижение давления; б) понижение температуры; в) удаление метанола?
В.Гидролиз. Реакции обмена.
1.В каких случаях попарно взятые вещества, формулы которых приведены ниже, вступают в реакции ионного обмена, идущие до конца: а) C а 3 ( PO 4 ) 2 и HCl ; б) CaCl 2 и AgNO 3 ; в) KOH и Na 2 SO 4 ; Напишите молекулярное, полное и краткое ионные уравнения данной реакции реакции
2. Даны соли: хлорид алюминия, карбонат натрия . При гидролизе одной из них среда становится кислой . Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава хлорида меди( II )
Рассчитайте объем водорода, выделившегося при взаимодействии 60 г. алюминия содержащего 20% примесей с соляной кислотой.
Контрольная работа. «Химические реакции»
Даны уравнения трех реакций:
1. Какое из них соответствует следующей характеристике: реакция соединения, обратимая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «а», при следующих воздействиях: а) повышение давления; б) понижение температуры; в) удаление углекислого газа?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции
2. Даны соли: сульфат натрия , нитрат алюминия . При гидролизе одной из них среда становится щелочной. Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава хлорида бария.
Рассчитайте массу соли образовавшейся при взаимодействии технического железа массой 150 г. , с массовой долей чистого вещества 80%
Контрольная работа «Химические реакции»
А. Равновесие химических реакций.
Даны уравнения трех реакций:
б ) 2KClO 3 2KCl + 3O 2 ↑ — Q;
1. Какое из них соответствует следующей характеристике: реакция соединения, экзотермическая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «в», при следующих воздействиях: а) повышение давления; б) повышение температуры; в) добавление в систему водорода?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции
2. Даны соли: хлорид алюминия, нитрат калия. При гидролизе одной из них среда становится щелочной. Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава иодида калия.
Рассчитайте массу воздуха необходимого для полного сжигания 12 куб. м метана.
Контрольная работа «Химические реакции»
Даны уравнения трех реакций:
1. Какое из них соответствует следующей характеристике: реакция соединения, эндотермическая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «а», при следующих воздействиях: а) понижение давления; б) понижение температуры; в) удаление метанола?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции реакции
2. Даны соли: хлорид алюминия, карбонат натрия . При гидролизе одной из них среда становится кислой . Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава хлорида меди( II )
Рассчитайте объем водорода, выделившегося при взаимодействии 60 г. алюминия содержащего 20% примесей с соляной кислотой.
Контрольная работа. «Химические реакции»
Даны уравнения трех реакций:
1 Какое из них соответствует следующей характеристике: реакция соединения, обратимая и т.д.? Дополните описание этой реакции
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «а», при следующих воздействиях: а) повышение давления; б) понижение температуры; в) удаление углекислого газа?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции
2. Даны соли: сульфат натрия , нитрат алюминия . При гидролизе одной из них среда становится щелочной. Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава хлорида бария.
Рассчитайте массу соли образовавшейся при взаимодействии технического железа массой 150 г. , с массовой долей чистого вещества 80%
Контрольная работа «Химические реакции»
А. Равновесие химических реакций.
Даны уравнения трех реакций:
б ) 2KClO 3 2KCl + 3O 2 ↑ — Q;
1. Какое из них соответствует следующей характеристике: реакция соединения, экзотермическая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «в», при следующих воздействиях: а) повышение давления; б) повышение температуры; в) добавление в систему водорода?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции
2. Даны соли: хлорид алюминия, нитрат калия. При гидролизе одной из них среда становится щелочной. Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава иодида калия.
Рассчитайте массу воздуха необходимого для полного сжигания 12 куб. м метана.
Контрольная работа «Химические реакции»
Даны уравнения трех реакций:
1. Какое из них соответствует следующей характеристике: реакция соединения, эндотермическая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «а», при следующих воздействиях: а) понижение давления; б) понижение температуры; в) удаление метанола?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции реакции
2. Даны соли: хлорид алюминия, карбонат натрия . При гидролизе одной из них среда становится кислой . Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава хлорида меди( II )
Рассчитайте объем водорода, выделившегося при взаимодействии 60 г. алюминия содержащего 20% примесей с соляной кислотой.
Контрольная работа. «Химические реакции»
Даны уравнения трех реакций:
1. Какое из них соответствует следующей характеристике: реакция соединения, обратимая и т.д.? Дополните описание этой реакции.
2. Дайте полную характеристику реакции «б».
3. В какую сторону сместится химическое равновесие системы, записанной как уравнение «а», при следующих воздействиях: а) повышение давления; б) понижение температуры; в) удаление углекислого газа?
В.Гидролиз. Реакции обмена.
Напишите молекулярное, полное и краткое ионные уравнения данной реакции
2. Даны соли: сульфат натрия , нитрат алюминия . При гидролизе одной из них среда становится щелочной. Напишите молекулярное и краткое ионное уравнения гидролиза этой соли.
Рассмотрите процессы, идущие на катоде и аноде при гидролизе раствора и расплава хлорида бария.
Рассчитайте массу соли образовавшейся при взаимодействии технического железа массой 150 г. , с массовой долей чистого вещества 80%
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
- Сейчас обучается 932 человека из 80 регионов
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
- Курс добавлен 23.11.2021
- Сейчас обучается 40 человек из 25 регионов
Курс повышения квалификации
Инструменты онлайн-обучения на примере программ Zoom, Skype, Microsoft Teams, Bandicam
- Курс добавлен 31.01.2022
- Сейчас обучается 26 человек из 16 регионов
Ищем педагогов в команду «Инфоурок»
Дистанционные курсы для педагогов
Самые массовые международные дистанционные
Школьные Инфоконкурсы 2022
33 конкурса для учеников 1–11 классов и дошкольников от проекта «Инфоурок»
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
5 573 337 материалов в базе
Другие материалы
- 14.06.2017
- 911
- 2
- 14.06.2017
- 811
- 0
- 14.06.2017
- 713
- 4
- 14.06.2017
- 732
- 7
- 14.06.2017
- 473
- 1
- 14.06.2017
- 1192
- 1
- 14.06.2017
- 433
- 0
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Добавить в избранное
- 14.06.2017 4254
- DOCX 49.8 кбайт
- 2 скачивания
- Оцените материал:
Настоящий материал опубликован пользователем Агибалова Ирина Анатольевна. Инфоурок является информационным посредником и предоставляет пользователям возможность размещать на сайте методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайт
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Автор материала
- На сайте: 5 лет и 7 месяцев
- Подписчики: 0
- Всего просмотров: 8698
- Всего материалов: 8
Московский институт профессиональной
переподготовки и повышения
квалификации педагогов
Дистанционные курсы
для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы
установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
Инфоурок стал резидентом Сколково
Время чтения: 2 минуты
В Забайкалье в 2022 году обеспечат интернетом 83 школы
Время чтения: 1 минута
Тринадцатилетняя школьница из Индии разработала приложение против буллинга
Время чтения: 1 минута
Профессия педагога на третьем месте по популярности среди абитуриентов
Время чтения: 1 минута
В России могут объявить Десятилетие науки и технологий
Время чтения: 1 минута
Полный перевод школ на дистанционное обучение не планируется
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Контрольная работа по химии 11 класс на тему: «Химические реакции»
Контрольная работа по химии 11 класс на тему: «Химические реакции»
Просмотр содержимого документа
«Контрольная работа по химии 11 класс на тему: «Химические реакции»»
Контрольная работа к главе “Химические реакции”
А1. Даны уравнения трех реакций:
Для реакции замещения рассчитайте суммарную массу продуктов, образующихся при взаимодействии исходных веществ массой по 10 г каждое:
а) 20,0г; б)15,6г; в)14,8г; г)19,2г.
А2. В окислительно-восстановительной реакции, схема которой
KCLO3 + FeSO4 + H2SO4 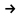
Сумма коэффициентов перед окислителем и восстановителем равна:
а) 4; б) 7; в) 9; г) 10.
А3. Дана цепочка превращений:
Ca 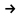
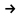
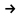
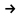
Из четырех приведенных реакций:
а) большинство экзотермических;
б) большинство эндотермических;
в) эндотермических реакций нет;
г) число экзотермических и эндотемических реакций одинаково.
А4. Количество тепловой энергии, которое выделяется или поглощается в ходе химической реакции, называется:
А) тепловым эффектом;
Б) энергией активации;
В) теплотой образования;
Г) температурным коэффициентом.
А5. При добавлении к избытку воды 5,6 г оксида кальция выделяется 6,4 кДж теплоты, а при реакции 14 г оксида кальция с водой можно получить 3,8 ккал теплоты. Укажите соотношение между этими двумя единицами измерения энергии:
а) 1 кал = 1 Дж; б) 1 Дж 
в) 1 Дж 

А6. На графике изображено изменение концентрации продукта некоторой реакции с течением времени. В какой из равных временных промежутков средняя скорость реакции максимальна?
А7. Физический смысл температурного коэффициента Вант-Гоффа заключается в том, что он показывает:
А) скорость химической реакции при увеличении температуры на 10 о С;
Б) во сколько раз увеличивается скорость химической реакции при увеличении температуры на 2-4 о С;
В) во сколько раз увеличивается скорость химической реакции при увеличении температуры на каждые 10 о С;
Г) на сколько градусов необходимо увеличить температуру реакции, чтобы ее скорость увеличилась в 2-4 раза.
А8. В промышленности гидрирование жидких жиров проводят с использованием катализатора:
а) серебра; б) меди;
б) платины; г) никеля.
А9. Дегидрирование алканов является эндотермическим процессом. Какое из воздействий будет способствовать смещению равновесия в реакции:
CH3 – CH2 – CH2 – CH3(r) 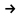
в сторону образования бутадиена-1 ,3?
Б) уменьшение давления;
В) увеличение концентрации водорода;
Г) внесение катализатора.
А10. Увеличение температуры приводит к смещению равновесия в реакции синтеза аммиака в сторону исходных веществ:
N2 + 3H2 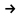
Почему в промышленности этот процесс ведут при повышенной температуре?
А) прямая реакция экзотермична , смесь газов нагревается, и ее охлаждение требует значительных материальных затрат;
Б) значительно сокращается время достижения равновесия;
В) аммиак получается более высокого качества;
Г) все приведенные выше причины верны.
А11. Долю молекул, распавшихся на ионы в растворе, показывает величина:
А) константы диссоциации;
Б) степени диссоциации;
в) температурного коэффициента;
г) верного ответа среди перечисленных нет.
А12. Краткому ионному уравнению
CH3COO — + H + 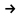
соответствует взаимодействие между:
а) ацетатом магния и водой;
б) ацетатом аммония и гидроксидом натрия;
в) ацетатом натрия и кремниевой кислотой;
г) ацетатом калия и азотной кислотой.
А13. Ионы какой группы могут быть легко удалены из раствора в виде труднорастворимых соединений?
а) Cu 2+ , CO3 2- , NO3 — ; б)Fe 3+ , Na + , Cl — ;
б) Ca 2+ , S 2- , SiO3 2- ; г) Pb 2+ , NH4 + , Br — .
А14. В каком случае растворы трех солей в группе можно распознать с помощью универсальной индикаторной бумаги?
А15. В водном растворе какой соли концентрация ионов водорода будет наибольшей?
В1. Дана цепочка превращений:
C2H2 
Напишите название вещества, полученного по реакции замещения.
В2. На скорость гомогенной газофазной реакции оказывают влияние природа реагирующих веществ, давление (и, следовательно, концентрация веществ), присутствие катализатора. Какой важный фактор не назван?
В3. Реакция синтеза аммиака, уравнение которой
N2(r) + 3H2(r) 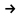
достигла состояния равновесия. Напишите название вещества, удаление которого из смеси газов приведет к смещению равновесия вправо.
В4. Как называются вещества, водные растворы которых проводят электрический ток (напишите термин во множественном числе)?
В5. Приведены названия десяти неорганических и органических веществ: иодид калия, нитрат железа(III), сульфит натрия, сульфат аммония, хлорид серебра, сахароза, этаналь, олеат натрия, этилацетат, глицерин. Сколько из них способны гидролизоваться? (Число в ответе напишите словом)
С1. Допишите левые части уравнений химических реакций. Расставьте коэффициенты.
а) … 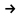
б) … 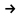
в) … 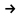

г) … 
С2. Для реакции, уравнение которой
CH3OH 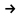

напишите выражение константы равновесия. Укажите все известные вам способы смещения равновесия в сторону образования метаналья.
http://infourok.ru/kontrolnaya-rabota-po-himii-klass-1978331.html
http://multiurok.ru/files/kontrolnaia-rabota-po-khimii-11-klass-na-temu-khim.html



