Давление основное уравнение молекулярно кинетической теории
| Давление. Основное уравнение молекулярно-кинетической теории |   |
Рассмотрим подробнее, что представляет собой один из основных параметров состояния – давление P. Ещё в XVIII веке Даниил Бернулли предположил, что давление газа есть следствие столкновения газовых молекул со стенками сосуда. Именно давление чаще всего является единственным сигналом присутствия газа. Итак, находящиеся под давлением газ или жидкость действуют с некоторой силой на любую поверхность, ограничивающую их объем. В этом случае сила действует по нормали к ограничивающей объем поверхности. Давление на поверхность равно:
Можно также говорить о давлении внутри газа или жидкости. Его можно измерить, помещая в газ или жидкость небольшой куб с тонкими стенками, наполненный той же средой (рис. 1.1). Допустим, автомобиль поднимается гидравлическим домкратом, состоящим, как показано на рисунке 1.2, из двух соединенных трубкой цилиндров с поршнями. Диаметр большого цилиндра равен 1 м, а диаметр малого – 10 см. Автомобиль имеет вес F2. Найдем силу давления на поршень малого цилиндра, необходимую для подъема автомобиля.
Таким образом, для подъема автомобиля достаточно давить на малый поршень с силой, составляющей лишь 1 % веса автомобиля. Вычислим давление, оказываемое газом на одну из стенок сосуда (рис. 1.3). Каждая молекула обладает импульсом m0υx, но стенка получает импульс 2m0υx(при абсолютно-упругом ударе m0υx— (-m0υx)=2m0υx). За время dt о стенку площадью S успеет удариться число молекул, которое заключено в объёме V:
Более точно случайную величину характеризует среднеквадратичная величина. Поэтому под скоростью vx 2 понимаем среднеквадратичную скорость 2 > . Вектор скорости, направленный произвольно в пространстве, можно разделить на три составляющих:
Итак, давление газов определяется средней кинетической энергией поступательного движения молекул. Уравнение (1.2.3) называют основным уравнением, потому что давление Р – макроскопический параметр системы здесь связан с основными характеристиками – массой и скоростью молекул. Иногда за основное уравнение принимают выражение Рассмотрим единицы измерения давления. По определению, 1 Н/м 2 = 1 Па; 1 атм. = 9,8 Н/см 2 = 98066 Па ≈10 5 Па, 1 мм рт.ст. = 1 тор = 1/760 атм. = 133,3 Па, Основное уравнение МКТ идеального газатеория по физике 🧲 молекулярная физика, МКТ, газовые законыИдеальный газ — газ, удовлетворяющий трем условиям:
Реальный газ с малой плотностью можно считать идеальным газом. Измерение температурыТемпературу можно измерять по шкале Цельсия и шкале Кельвина. По шкале Цельсия за нуль принимается температура, при которой происходит плавление льда. По шкале Кельвина за нуль принимается абсолютный нуль — температура, при котором давление идеального газа равно нулю, и его объем тоже равен нулю. Обозначение температуры
Цена деления обеих шкал составляет 1 градус. Поэтому изменение температуры в градусах Цельсия равно изменению температуры в Кельвинах: При решении задач в МКТ используют значения температуры по шкале Кельвина. Если в условиях задачи температура задается в градусах Цельсия, нужно их перевести в Кельвины. Это можно сделать по формуле: Если особо важна точность, следует использовать более точную формулу: Пример №1. Температура воды равна o C. Определить температуру воды в Кельвинах. T = t + 273 = 2 + 273 = 275 (К) Основное уравнение МКТ идеального газаДавление идеального газа обусловлено беспорядочным движением молекул, которые сталкиваются друг с другом и со стенками сосуда. Основное уравнение МКТ идеального газа связывает давление и другие макропараметры (объем, температуру и массу) с микропараметрами (массой молекул, скоростью молекул и кинетической энергией). Основное уравнение МКТ Давление идеального газа пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы. p = 2 3 . . n − E k p — давление идеального газа, n — концентрация молекул газа, − E k — средняя кинетическая энергия поступательного движения молекул. Выражая физические величины друг через друга, можно получить следующие способы записи основного уравнения МКТ идеального газа: p = 1 3 . . m 0 n − v 2 m 0 — масса одной молекулы газа; n — концентрация молекул газа; − v 2 — среднее значение квадрата скорости молекул газа. Среднее значение квадрата скорости не следует путать со среднеквадратичной скоростью v, которая равна корню из среднего значения квадрата скорости: p = 1 3 . . ρ − v 2 | ρ — плотность газа | ||||||||||||

 ,
, ,
, ,
, ,
, ,
, ,
, ,
,

 , поэтому размерность давления Н/м 2 .
, поэтому размерность давления Н/м 2 .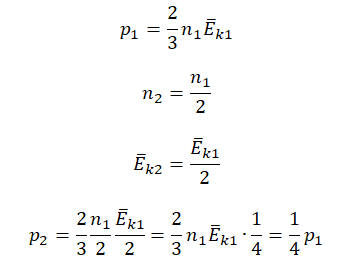
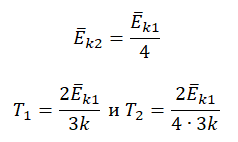
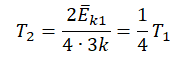
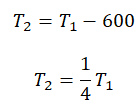
 На графике представлена зависимость объёма постоянного количества молей одноатомного идеального газа от средней кинетической энергии теплового движения молекул газа. Опишите, как изменяются температура и давление газа в процессах 1−2 и 2−3. Укажите, какие закономерности Вы использовали для объяснения.
На графике представлена зависимость объёма постоянного количества молей одноатомного идеального газа от средней кинетической энергии теплового движения молекул газа. Опишите, как изменяются температура и давление газа в процессах 1−2 и 2−3. Укажите, какие закономерности Вы использовали для объяснения.