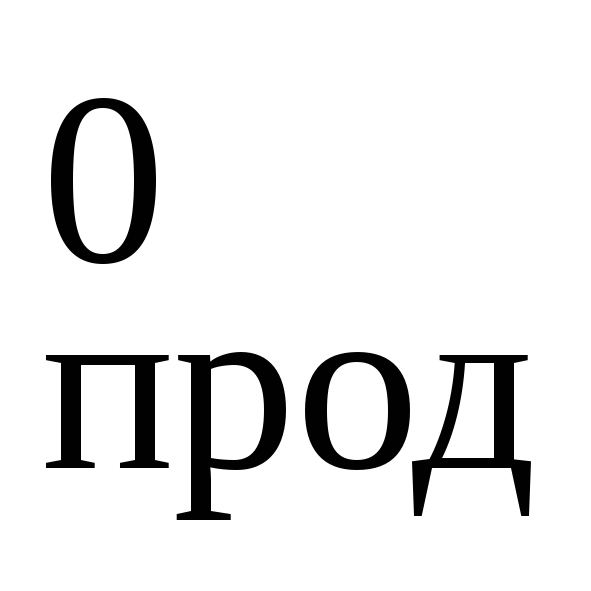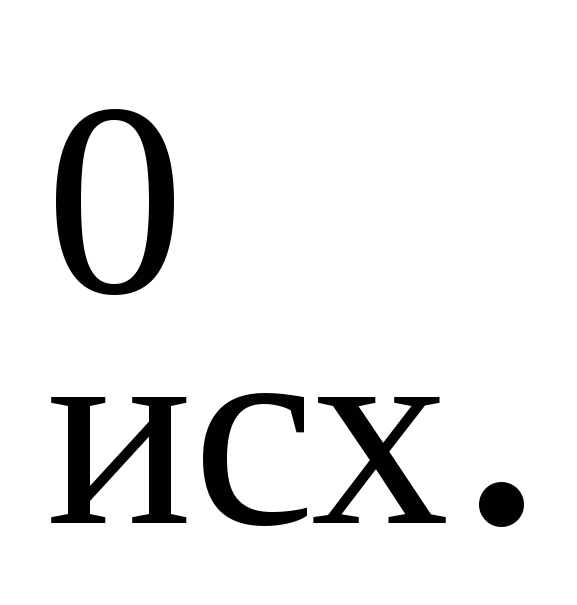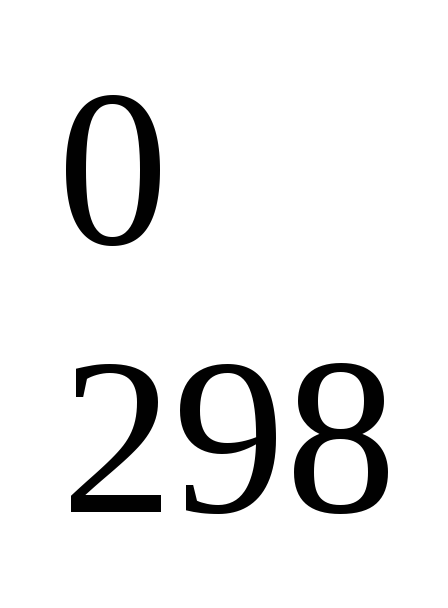Энергия Гиббса. Энергия Гельмгольца. Направление процесса.
Чтобы дать ответ на вопрос о возможности протекания той или иной реакции, о ее направлении и глубине необходимо снова воспользоваться II – законом термодинамики, который может быть сформулирован следующим образом: любой самопроизвольно протекающий процесс, а также и химическая реакция, идет в том направлении, которое сопровождается уменьшением свободной энергии в системе (при постоянных температуре и давлении) или энергии Гельмгольца (при постоянных температуре и объеме).
Свободная энергия или Энергия Гиббса G – это та часть всей энергии системы, которую можно использовать для совершения максимальной работы.
Энергия Гельмгольца A — это та часть внутренней энергии системы, также определяющая работоспособность и может быть применена для совершения максимальной работы.
При протекании химических реакций единовременно совершаются два направления: стремление простых частиц объединиться в более сложные, а также стремление сложных частиц к распаду на более простые.
Они не зависят друг от друга и их величины противоположны, и процесс идет в сторону той реакции, при которой изменение величины больше. Разность между этими величинами определяет свободную энергию реакции (при постоянных температуре и давлении). Ее изменение в реакции определяется разностью сумм энергий Гиббса конечных продуктов реакции и исходных веществ:
При постоянных температуре и давлении изменение энергии Гиббса связано с энтальпией и энтропией следующим выражением:
Здесь изменение энергии Гиббса учитывает одновременно изменение энергетического запаса системы и степень ее беспорядка (самопроизвольность протекания процесса).
Т.к. энергия Гиббса является мерой самопроизвольности протекания процесса, то между знаком ΔG для любой реакции и ее самопроизвольным протеканием (при постоянных температуре и давлении) существуют такие зависимости:
- Если ΔG отрицательно (ΔG 0), то реакция протекать самопроизвольно в прямом направлении не может. Однако обратная реакция идет самопроизвольно.
Энтальпийный и энтропийный факторы и направление процесса
Выясним, как функция свободной энергии зависит от изменений энтропии и энтальпии идущего процесса. Вернемся к выражению, связывающему энергию Гиббса с энтальпией и энтропией:
Без энтропийных факторов все экзотермические реакции (ΔH˂0) должны были быть самопроизвольными. Но энтропийный фактор, который определяется величиной – TΔS, может привести к росту или, наоборот, к падению способности самопроизвольного протекания.
Так, при ΔS>0, член – TΔS вносит отрицательный вклад в общую величину ΔG, следовательно он повышает возможность реакции протекать самопроизвольно.
А при при ΔS 0 Изменение энергии Гиббса. Для удобства принято сравнивать значения ΔG при стандартных условиях – концентрации равны 1 моль/л, парциальное давление газообразных веществ равно 101,3 кПа, температура 298,15 К. Тогда свободную энергию обозначают через ΔG 0 , на основе значений которой можно вычислить изменение энергии Гиббса химической реакции: Величина ΔG 0 р-ции позволяет определить, будет ли данная реакция, находящаяся в стандартных условиях, протекать самопроизвольно в прямом или обратном направлении. Аналогично теплоте образования, энергии Гиббса образования простых веществ равны нулю. Энергия Гельмгольца системы с определенной внутренней энергией (U), энтропией (S) при абсолютной температуре (Т) определяется уравнением: Изменение энергии Гельмгольца для процессов (при постоянных температуре и объеме) можно определить соотношением: ΔA — величина, которая не зависит от пути, а зависит только от исходного и конечного состояния системы, т.е. ΔA также, как и другие рассмотренные термодинамические величины, является функцией состояния. Энергия Гельмгольца подобно энергии Гиббса связана с самопроизвольностью протекания процесса. Если допустить, что система изолирована, а объем и температура постоянны, то самопроизвольно будут протекать только те процессы, при которых А уменьшается. Таким образом, при ΔA 0 – в обратном направлении, а при ΔA=0 система находится в состоянии равновесия. Энергию Гельмгольца и энергию Гиббса в стандартных состояниях можно связать с константой равновесия: Где R– универсальная газовая постоянная, K – константа равновесия, Т – абсолютная температура. Если K>>1, т.е. реакция идет в прямом направлении, то ΔG 0 ˂˂0. Если K 0 >>0 Если K=1, то ΔG 0 =0 В случае химической реакции, протекающей в гальваническом элементе при стандартных условиях ΔG 0 можно связать с ЭДС гальванического элемента следующим соотношением: ΔG 0 =-nFE 0 , где nF – количество прошедшего электричества E 0 – электродвижущая сила, при условии что все вещества, принимающие участие в реакции, находятся в стандартном состоянии. При самопроизвольном протекании процесса, его ΔG 0. Порог реакционной способности веществ для большинства реакций имеет значение ΔG 0 ≈41 кДж/моль. То есть, если ΔG 0 0 >+41 кДж/моль, то процесс неосуществим в любых реальных и стандартных условиях. Если реакцию проводят в стандартных условиях (единичные концентрации и давления) и при температуре, которая соответствует таблице термодинамических значений (обычно 298,15 К), то можно вычесть стандартную свободную энергию образования Гиббса ( # DeltaG_f # ) реагентов из продуктов. В противном случае вам потребуется более сложный подход: Рассчитайте стандартную энтальпию реакции, вычитая # DeltaH_f # реагентов из продуктов. Выполните аналогичную процедуру для расчета стандартной энтропии реакции ( # Дельт # ). подсчитывать # DeltaG ^ 0 # для реакции с использованием уравнения # DeltaG ^ 0 = DeltaH ^ 0-TDeltaS ^ 0 # , Это делает приближение, что # DeltaH ^ 0 # а также # Дельт ^ 0 # не зависят от температуры. Верхний индекс 0 обозначает «при стандартных условиях». # DeltaG ^ 0 # то, что вы рассчитали на шаге 3, является стандартным изменением свободной энергии Гиббса, предполагая, что все реагенты и продукты присутствуют в единичных концентрациях (1 М для растворенных веществ или 1 бар для парциального давления для газов или чистых жидкостей или чистых твердых веществ). Если вы хотите рассчитать # DeltaG # в нестандартных условиях нужно использовать уравнение #DeltaG = DeltaG ^ 0 + RTlnQ # где Q — соотношение концентраций (или активностей) продуктов, деленное на реагенты. При стандартных условиях Q = 1 и # DeltaG = DeltaG ^ 0 # , В условиях равновесия Q = K и # DeltaG = 0 # так # DeltaG ^ 0 = -RTlnK # . Для большей точности можно учесть температурную зависимость # DeltaH ^ 0 # а также # Дельт ^ 0 # рассматривая # DeltaT # между фактической температурой реакции в стандартной температуре термодинамической таблицы, которую вы используете. Например, если ваша реакция на 350K, а ваша таблица на 298K, то для каждого реагента и продукта энтальпия и энтропия образования: Когнитивное обучение предполагает, что ваш мозг выполняет работу по приобретению знаний. Условное обучение говорит, что ваш мозг не вовлечен. Парень, который предложил эту условную теорию, явно говорил о своем мозге. Шутка в сторону, не простой вопрос. Как вы думаете? M_1u_1 + m_2u_2 = m_1v_1 + m_2v_2, если два упругих шара сталкиваются горизонтально (никакие другие силы не влияют в этом направлении), тогда импульс между ними сохраняется, поэтому, если один шар теряет скорость, другой шар набирает скорость, поэтому применяется вышеуказанное соотношение Пример: как в этих примерах, хотя первый шар остановился, его импульс был передан другому шару. цвет (зеленый) («Примечание:») вышеупомянутое соотношение зависит от направления, поэтому вы полагаете, что одно направление положительно, поэтому скорости в этом направлении положительны, а скорости в другом направлении отрицательны. энтропийно выгодным будет процесс распада АВ(г) на компоненты (∆S>0), а энергетически выгодным является обратный процесс, который сопровождается понижением энтальпии химической системы (∆H 0 возможен лишь обратный процесс. При ∆G=0 все вещества находятся в химическом равновесии и внешне незаметно никаких изменений и процессов в системе. 1) если ∆H 0, то всегда ∆G 0 и ∆S 0, т.е. реакция с поглощением теплоты и увеличением степени порядка невозможна ни при каких условиях; 3) во всех остальных случаях (∆H 0, ∆S>0) знак ∆G зависит от соотношения членов ∆H и T∆S. Значения ∆H и ∆S могут быть как положительными, так и отрицательными в разных сочетаниях в разных реакциях. Их рассматривают как энергетический (энтальпийный) и энтропийный факторы, определяющие возможность самопроизвольного протекания реакции. Реакция возможна, только если она сопровождается уменьшением энергии Гиббса. Если ∆H>0, ∆S>0, то произведение T∆S будет больше, чем ∆H и определяющим фактором будет знак ∆S. В этом случае ∆G o A+RT lnpA)nA, (3.16) где GA− энергия Гиббса образования вещества А при его парциальном давлении рА (pА¹1атм); G o A− энергия Гиббса образования одного моля вещества А при стандартных условиях (рА=1 атм и Т=298 К); nA − число молей вещества А. Стандартная энергия Гиббса образования вещества DG о 298 − изменение энергии Гиббса в реакции образования 1моль вещества из простых веществ, находящихся в устойчивых состояниях при стандартных условиях(р=101,3 кПа и Т=298 К). Значения ∆G о 298 для некоторых веществ приводятся в справочной литературе, размерность − кДж/моль. Стандартные энергии Гиббса образования простых веществ, находящихся в стандартном состоянии в устойчивой модификации, равны нулю. Например, ∆G о 298,Н2(газ) = 0 кДж/моль. Энергия Гиббса химических реакций. Изменение энергии Гиббса химической реакции при стандартных условиях (р =101,3 кПа и Т=298 К) можно вычислить по уравнению где ∆H о 298,реакции, ∆S о 298,реакции − стандартные изменения энтальпии и энтропии химической реакции, соответственно в кДж и Дж/К; Т− стандартная температура, равная 298 К. Поскольку энергия Гиббса является функцией состояния, то ее значение не зависит от пути протекания процесса, а зависит только от исходного и конечного состояний системы. Изменение энергии Гиббса при стандартных условиях (∆G о 298, реакции) можно рассчитать, используя стандартные значения энергий Гиббса образования исходных веществ и продуктов реакции с учетом стехиометрических коэффициентов: ∆G о 298,реакции = Изменение энергии Гиббса ∆GТ для реакции, протекающей при температуре, отличной от стандартной (Т Не нашли то, что искали? Воспользуйтесь поиском: При решении задач этого раздела см. табл. 5-7. Направление, в котором самопроизвольно могут протекать реакции, определяется совместным действием двух тенденций: стремлением системы к переходу в состояние с наименьшей энергией; стремлением к наиболее вероятному состоянию. Первая тенденция характеризуется величиной ∆Н, т.е. самопроизвольно протекают реакции, сопровождающиеся уменьшением энтальпии (∆Н S1, то S > 0. Если S2 0 прод – S 0 исх. Энтропия выражается в Дж/(моль . К). Очевидно, что, характеризуя две противоположные тенденции процесса, энтальпия или энтропия, взятые по отдельности, не могут служить критерием его самопроизвольного протекания. Функцией состояния, учитывающей обе тенденции, является энергия Гиббса G: или ∆H = ∆G + T ∆S. (2) Из уравнения (2) следует, что энтальпия химической реакции состоит из двух слагаемых. Первое – ∆G – представляет собой ту часть энергии, которая может быть превращена в работу. Поэтому энергию Гиббса иногда называют свободной энергией. Второе слагаемое – это та часть энергии, которую невозможно превратить в работу. Произведение T·∆S называют рассеянной или связанной энергией, она рассеивается в окружающую среду в виде теплоты. Энергия Гиббса при постоянном давлении и температуре служит критерием самопроизвольного протекания любого процесса, в том числе и химической реакции. Самопроизвольно протекающие процессы идут в сторону уменьшения потенциала и, в частности, в сторону уменьшения G. Если G О, процесс самопроизвольно проходить не может. Чем меньше G, тем сильнее стремление к протеканию данного процесса и тем дальше он от состояния равновесия, при котором G = 0 и H= T·S. Химическая реакция принципиально возможна, если энергия Гиббса уменьшается ∆G 0, реакция не может протекать самопроизвольно в прямом направлении. Это неравенство свидетельствует о термодинамической возможности самопроизвольного протекания обратной реакции. Из соотношения (1) видно, что самопроизвольно могут протекать и процессы, для которых H>0 (эндотермические). Это возможно, когда ΔS > 0, но│∆H│ │T∆S│, следовательно G>0. Эндотермические реакции, сопровождающиеся уменьшением энтропии, в принципе невозможны. Протекание экзотермических реакций с увеличением энтропии термодинамически возможно при любых температурах. Энергия Гиббса является функцией состояния, поэтому изменение энергии Гиббса в результате протекания химической реакции при стандартных условиях вычисляется по формуле Gхр.= G а при любых других температурах – по уравнению (1). Пример 1. В каком состоянии энтропия 1 моль вещества больше при одинаковой температуре: в кристаллическом или парообразном? Решение. Энтропия есть мера неупорядоченности состояния вещества. В кристалле частицы (атомы, ионы) расположены упорядоченно и могут находиться лишь в определенных точках пространства, а для газа таких ограничений нет. Объем 1 моль газа гораздо больше объема 1 моль кристаллического вещества; возможность хаотичного движения молекул газа больше. А так как энтропию можно рассматривать как количественную меру хаотичности атомно-молекулярной структуры вещества, то энтропия 1 моль паров вещества больше энтропии 1 моль его кристаллов при одинаковой температуре. Пример 2. Прямая или обратная реакция будет протекать при стандартных условиях в системе С Решение. Вычислим G G То, что G Таблица 6. Стандартные энергии Гиббса образования G G Изменение энтропии аналогично. Для того, чтобы найти свободную энергию Гиббса, надо найти изменение энтропии, изменение энтальпии и среднюю теплоемкость ПРИ ЗАДАННОЙ ТЕМПЕРАТУРЕ: ΔНт=ΔН298+ΔС298*(Т-298), где ΔС298 – удельная теплоемкость при нормальных условиях (рассчитывается так же, как для изменения энтальпии при нормальных условиях) http://ru.teratips.com/60137-how-can-i-calculate-delta-g-of-a-reaction-85 http://4systems.ru/inf/delta-g-v-himii-formula/Всегда ˂0 Реакция самопроизвольна при любых температурах, обратная реакция всегда несамопроизвольна >0 ˂0 Всегда >0 Реакция несамопроизвольна при любых температурах, обратная реакция самопроизвольна ˂0 ˂0 При низких температурах ˂0, при высоких температурах >0 Реакция самопроизвольна при низких температурах, обратная реакция становится самопроизвольной при высоких температурах >0 >0 При низких температурах >0, при высоких температурах ˂0 Реакция несамопроизвольна при низких температурах, но при высоких температурах становится самопроизвольной Как я могу рассчитать дельта G реакции? + Пример — Химия — 2022
# Delta_fH_350 # = # Delta_fH_298 + C_P (350-298) #
# S_350 # = # S_298 + C_P ln (350/298) #
Затем рассчитайте # DeltaH # а также # Дельт # для реакции и остальной части процедуры без изменений.Рекомендуем
Объясните разницу между когнитивным обучением и условным обучением (стимулом и ответным обучением)?
Каков закон сохранения импульса?
Дельта g в химии формула