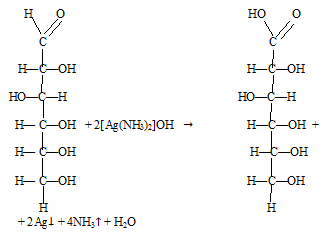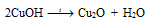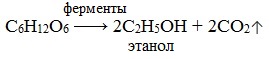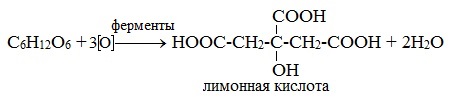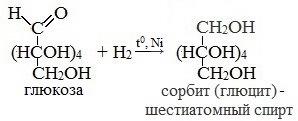Строение и химические свойства угдеводов
Опыт 1. Действие аммиачного раствора гидроксида серебра на глюкозу
Условия выполнения работы:
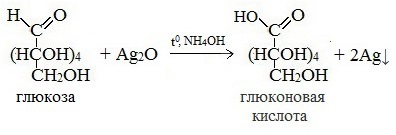
В пробирку налили немного раствора глюкозы и аммиачного раствора оксида серебра. Пробирку нагрели. Наблюдаем осаждение серебра на дне пробирки и стенках пробирки:
В реакцию серебряного зеркала вступает только линейная форма глюкозы.
Опыт 2. Действие гидроксида меди (II) на глюкозу
Условия выполнения работы:
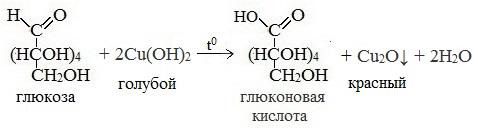
а) В пробирку налили немного раствора глюкозы, 2 мл раствора гидроксида натрия и 1 мл медного купороса. Наблюдаем образование голубого осадка гидроксида меди (II), который сразу растворяется и раствор окрашивается в ярко-синий цвет. Далее раствор в пробирке нагревается. Реакция глюкозы с гидроксидом меди при нагревании демонстрирует восстановительные свойства глюкозы. Происходит изменение — окрашивания раствора. В начале выпадает осадок оксида меди CuO желтого цвета. В процессе дальнейшего нагревания CuO восстанавливается до оксида меди (I) – Cu2O, который выпадает в виде красного осадка. В процессе этой реакции глюкоза окисляется до глюконовой кислоты.
Таким образом, при нагревании реакция глюкозы с гидроксидом меди(II) идет с восстановлением двухвалентной меди Cu (II) до одновалентной меди Cu (I).
Уравнениия реакций можно представить так:
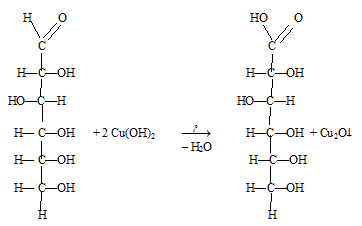
Происходит качественная реакция на многоатомные спирты, коим является глюкоза, реакция обусловлена наличием гидроксильной группы.
б) Если в пробирку налили немного раствора глюкозы, 2 мл раствора гидроксида натрия и 1 мл медного купороса, но не нагревали, то будем наблюдать образование голубого осадка гидроксида меди (II), который сразу растворяется и раствор окрашивается в ярко-синий цвет (образуется растворимая комплексная соль). В пробирку к полученному раствору добавили немного воды, закрепили пробирку на штативе. Нагрели пробирку так, чтобы прогревалась только верхняя часть раствора. Наблюдаем выпадение жёлто-красного осадка и обесцвечивание раствора. 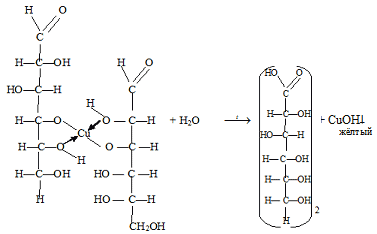
При нагревании происходит окисление глюкозы гидроксидом меди до карбоновой кислоты, эта реакция обеспечивается альдегидной группой 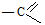
Выводы:
1) глюкоза реагирует с гидроксидом меди без нагревания с образованием ярко-синего раствора комплексной соли Cu 2+ ;
2) если реакцию глюкозы с гидроксидом меди проводить при нагревании, то происходит окисление глюкозы до карбоновой кислоты, образуется жёлто-красный осадок .
Опыт 3. Действие аммиачного раствора оксида серебра на сахарозу
Условия выполнения работы:
а) В пробирку налили немного раствора сахарозы и немного аммиачного раствора оксида серебра и нагрели пробирку. Ничего не происходит, реакция не идёт, так как сахарозу образуют циклические формы глюкозы и фруктозы, а они не дают реакцию серебряного зеркала.
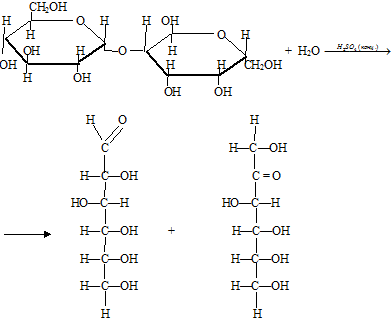
б) В пробирку налили немного раствора сахарозы и несколько капель разбавленной серной кислоты. Пробирку нагрели. Затем добавили в пробирку раствор гидроксида натрия, доводим раствор до слабощелочной среды (используя как индикатор лакмусовую бумагу). К полученному раствору добавили 2 мл аммиачного раствора оксида серебра и опять нагрели пробирку.
При нагревании раствора сахарозы с несколькими каплями серной кислоты, образуется глюкоза и фруктоза в свободной линейной форме:
Так как при гидролизе сахарозы образуется фруктоза и глюкоза, то реакция серебряного зеркала возможна только при линейной форме глюкозы (Смотри уравнение в Опыте 1.).
Опыт 4. Действие иода на крахмал
Условия выполнения работы:
В химический стакан налили 20 мл кипящей воды и присыпали немного крахмала, образовавшуюся смесь перемешали до образования прозрачного коллоидного раствора — крахмального клейстера. В пробирку налили немного охлаждённого клейстера и добавили несколько капель спиртового раствора иода. Наблюдаем синее окрашивание раствора. При нагревании полученного раствора синее окрашивание исчезает.
Действие аммиачного раствора гидроксида серебра на глюкозу
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,297
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,223
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Действие аммиачного раствора гидроксида серебра на глюкозу уравнение
Химические свойства глюкозы, как и других альдоз, обусловлены присутствием в ее молекуле: а)альдегидной группы; б) спиртовых гидроксилов; в) полуацетального (гликозидного) гидроксила.
Специфические свойства
1. Брожение (ферментация) моносахаридов
Важнейшим свойством моносахаридов является их ферментативное брожение, т.е. распад молекул на осколки под действием различных ферментов. Брожению подвергаются в основном гексозы в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента различают реакции следующих видов:
1) Спиртовое брожение
2) Молочнокислое брожение
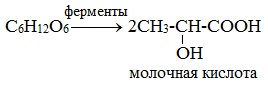
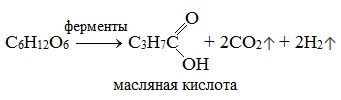
3) Маслянокислое брожение
4) Лимоннокислое брожение
Реакции с участием альдегидной группы глюкозы (свойства глюкозы как альдегида)
1. Восстановление (гидрирование) с образованием многоатомного спирта
В ходе этой реакции карбонильная группа восстанавливается и образуется новая спиртовая группа:
Cорбит содержится во многих ягодах и фруктах, особенно много сорбита в плодах рябины.
2. Окисление
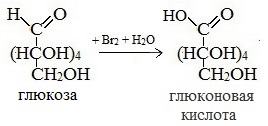
1) Окисление бромной водой
Качественные реакции на глюкозу как альдегид!
Протекающие в щелочной среде при нагревании реакции с аммиачным раствором Ag2O (реакция серебряного зеркала») и с гидроксидом меди (II) Cu (OH)2 приводят к образованию смеси продуктов окисления глюкозы.
2) Реакция серебряного зеркала
Соль этой кислоты – глюконат кальция – известное лекарственное средство.
Видеоопыт «Качественная реакция глюкозы с аммиачным раствором оксида серебра (I)»
3) Окисление гидроксидом меди (II)
В ходе этих реакций альдегидная группа – СНО окисляется до карбоксильной группы – СООН.
Реакции глюкозы с участием гидроксильных групп (свойства глюкозы как многоатомного спирта)
1. Взаимодействие с Cu (ОН)2 с образованием глюконата меди (II)
Качественная реакция на глюкозу как многоатомный спирт!
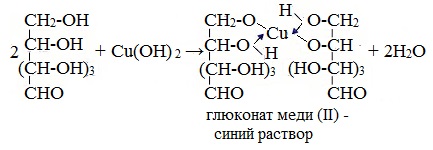
Подобно этиленгликолю и глицерину, глюкоза способна растворять гидроксид меди (II), образуя растворимое комплексное соединение синего цвета:
Прильём к раствору глюкозы несколько капель раствора сульфата меди (II) и раствор щелочи. Осадка гидроксида меди не образуется. Раствор окрашивается в ярко-синий цвет.
В данном случае глюкоза растворяет гидроксид меди (II) и ведет себя как многоатомный спирт, образуя комплексное соединение.
Видеоопыт «Качественная реакция глюкозы с гидроксидом меди (II)»
2. Взаимодействие с галогеналканами с образованием простых эфиров
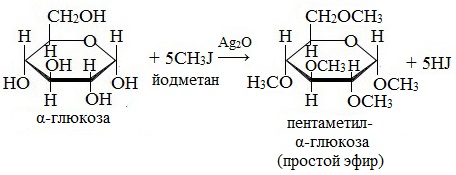
Являясь многоатомным спиртом, глюкоза образует простые эфиры:
Реакция происходит в присутствии Ag2O для связывания выделяющегося при реакции НI.
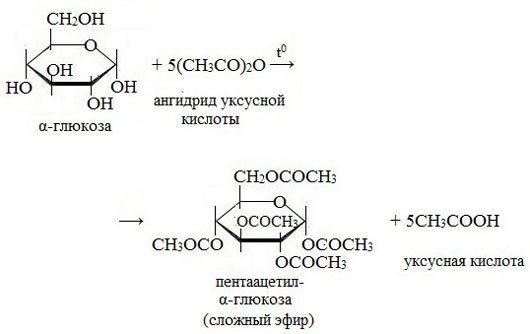
3. Взаимодействие с карбоновыми кислотами или их ангидридами с образованием сложных эфиров.
Например, с ангидридом уксусной кислоты:
Реакции с участием полуацетального гидроксила
1. Взаимодействие со спиртами с образованием гликозидов
Гликозиды – это производные углеводов, у которых гликозидный гидроксил замещен на остаток какого-либо органического соединения.
Содержащийся в циклических формах глюкозы полуацетальный (гликозидный) гидроксил является очень реакционноспособным и легко замещается на остатки различных органических соединений.
В случае глюкозы гликозиды называются глюкозидами. Связь между углеводным остатком и остатком другого компонента называется гликозидной.
Гликозиды построены по типу простых эфиров.
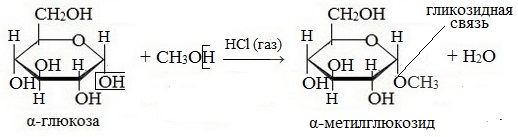
При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу:
В данных условиях в реакцию вступает только гликозидный гидроксил, спиртовые гидроксильные группы в реакции не участвуют.
Гликозиды играют чрезвычайно важную роль в растительном и животном мире. Существует огромное число природных гликозидов, в молекулах которых с атомом С (1) глюкозы остатки самых различных соединений.
Реакции окисления
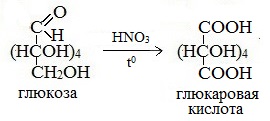
Более сильный окислитель – азотная кислота НNO3 – окисляет глюкозу до двухосновной глюкаровой (сахарной) кислоты:
В ходе этой реакции и альдегидная группа – СНО и первичная спиртовая группа — СН2ОН окисляются до карбоксильных – СООН.
Видеоопыт «Окисление глюкозы кислородом воздуха в присутствии метеленового голубого»
http://www.soloby.ru/312465/%D0%B4%D0%B5%D0%B9%D1%81%D1%82%D0%B2%D0%B8%D0%B5-%D0%B0%D0%BC%D0%BC%D0%B8%D0%B0%D1%87%D0%BD%D0%BE%D0%B3%D0%BE-%D1%80%D0%B0%D1%81%D1%82%D0%B2%D0%BE%D1%80%D0%B0-%D0%B3%D0%B8%D0%B4%D1%80%D0%BE%D0%BA%D1%81%D0%B8%D0%B4%D0%B0-%D1%81%D0%B5%D1%80%D0%B5%D0%B1%D1%80%D0%B0-%D0%B3%D0%BB%D1%8E%D0%BA%D0%BE%D0%B7%D1%83
http://himija-online.ru/organicheskaya-ximiya/uglevody/ximicheskie-svojstva-glyukozy.html