Адиабатический процесс и уравнения адиабаты для идеального газа. Пример задачи
Адиабатический переход между двумя состояниями в газах не относится к числу изопроцессов, тем не менее, он играет важную роль не только в различных технологических процессах, но и в природе. В данной статье рассмотрим, что представляет собой этот процесс, а также приведем уравнения адиабаты идеального газа.
Кратко об идеальном газе
Идеальным называется такой газ, в котором нет взаимодействий между его частицами, и их размеры равны нулю. В природе, конечно же, не существует идеальных на сто процентов газов, поскольку все они состоят из имеющих размеры молекул и атомов, которые взаимодействуют друг с другом всегда как минимум с помощью ван-дер-ваальсовых сил. Тем не менее, описанная модель часто выполняется с достаточной для решения практических задач точностью для многих реальных газов.

Главным уравнением идеального газа является закон Клапейрона-Менделеева. Он записывается в следующей форме:
Это уравнение устанавливает прямую пропорциональность между произведением давления P на объем V и количества вещества n на абсолютную температуру T. Величина R — газовая константа, которая играет роль коэффициента пропорциональности.
Что это адиабатический процесс?
Адиабатический процесс — это такой переход между состояниями газовой системы, при котором обмена энергией с внешней средой не происходит. При этом изменяются все три термодинамических характеристики системы (P, V, T), а количество вещества n остается постоянным.
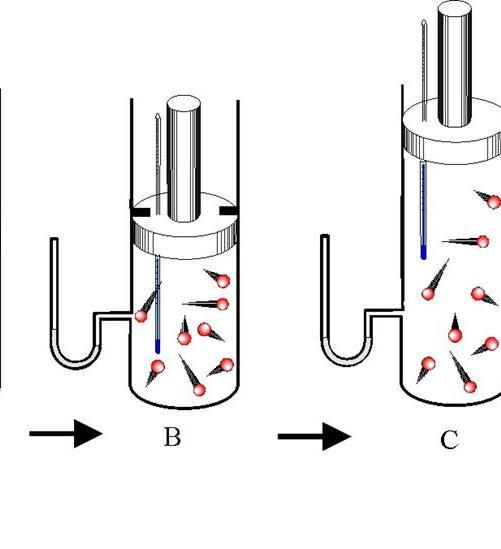
Различают адиабатическое расширение и сжатие. Оба процесса происходят только за счет внутренней энергии системы. Так, в результате расширения давление и особенно температура системы сильно падают. Наоборот, адиабатическое сжатие приводит к положительному скачку температуры и давления.
Чтобы не происходил обмен теплом между окружающей средой и системой, последняя должна обладать теплоизолированными стенками. Кроме того, сокращение длительности протекания процесса значительно уменьшает тепловой поток от и к системе.
Уравнения Пуассона для адиабатического процесса
Первый закон термодинамики записывается в таком виде:
Иными словами, сообщенная системе теплота Q идет на выполнение системой работы A и на повышение ее энергии внутренней ΔU. Чтобы написать уравнение адиабаты, следует положить Q=0, что соответствует определению изучаемого процесса. Получаем:
При изохорном процессе в идеальном газе все тепло идет на повышение внутренней энергии. Этот факт позволяет записать равенство:
Где CV — изохорная теплоемкость. Работа A, в свою очередь, вычисляется так:
Где dV — малое изменение объема.
Помимо уравнения Клапейрона-Менделеева, для идеального газа справедливо следующее равенство:
Где CP — изобарная теплоемкость, которая всегда больше изохорной, так как она учитывает потери газа на расширение.
Анализируя записанные выше равенства и проводя интегрирование по температуре и объему, приходим к следующему уравнению адиабаты:
Здесь γ — это показатель адиабаты. Он равен отношению изобарной теплоемкости к изохорной. Это равенство называется уравнением Пуассона для процесса адиабатического. Применяя закон Клапейрона-Менделеева, можно записать еще два аналогичных выражения, только уже через параметры P-T и P-V:
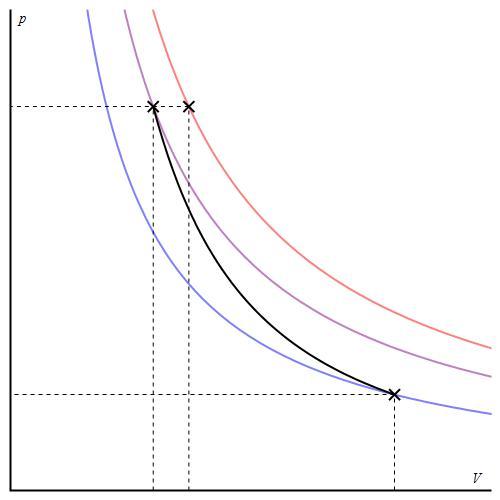
График адиабаты можно привести в различных осях. Ниже он показан в осях P-V.
Цветные линии на графике соответствуют изотермам, черная кривая — это адиабата. Как видно, адиабата ведет себя более резко, чем любая из изотерм. Этот факт просто объяснить: для изотермы давление меняется обратно пропорционально объему, для изобаты же давление изменяется быстрее, поскольку показатель γ>1 для любой газовой системы.
Пример задачи
В природе в горной местности, когда воздушная масса движется вверх по склону, то ее давление падает, она увеличивается в объеме и охлаждается. Этот адиабатический процесс приводит к снижению точки росы и к образованию жидких и твердых осадков.
Предлагается решить следующую задачу: в процессе подъема воздушной массы по склону горы давление упало на 30 % по сравнению с давлением у подножия. Чему стала равна ее температура, если у подножия она составляла 25 oC?
Для решения задачи следует использовать следующее уравнение адиабаты:
Его лучше записать в таком виде:
Если P1 принять за 1 атмосферу, то P2 будет равно 0,7 атмосферы. Для воздуха показатель адиабаты равен 1,4, поскольку его можно считать двухатомным идеальным газом. Значение температуры T1 равно 298,15 К. Подставляя все эти числа в выражение выше, получаем T2 = 269,26 К, что соответствует -3,9 oC.
Адиабатный процесс в термодинамике
Вы будете перенаправлены на Автор24
Адиабатный процесс или адиабатический — это термодинамический процесс, происходящий при отсутствии теплообмена с окружающей средой.
Рисунок 1. Адиабатический процесс. Автор24 — интернет-биржа студенческих работ
Есть несколько основных факторов, которые характеризуют данный класс. Например, адиабатный процесс может происходит динамично и укладывается в достаточно короткий период времени. Происходят все адиабатные процессы в термодинамике, как правило, мгновенно.
Уравнение первого закона термодинамики для исследуемого класса имеет следующий вид: $du = -dl = -pdv$. Из этой формулы видно, что работа адиабатического процесса расширения совершается в результате постепенного уменьшения внутренней энергии идеального газа и, следовательно, температура самого элемента уменьшается. Работа адиабатного сжатия всегда идет на только увеличение внутреннего энергетического потенциала, то есть на повышение температурных параметров. Таким образом, изменения условий работы системы в адиабатном процессе эквивалентны по величине и противоположны по знаку.
В реальных условиях указанное термодинамическое явление возможно осуществить двумя методами:
- провести физический процесс так быстро, чтобы теплообмен не успел произойти;
- полностью изолировать систему от факторов внешней среды.
После введения в эксперименты вышеуказанных способов получаем такое уравнение: $dU + dA = 0$. Графически на координатной плоскости адиабатный процесс практически всегда изображается кривой, которая называется в физике адиабатой. Она падает намного круче, чем более постоянная изотерма, поскольку при этом явлении изменение давления происходит с помощью одновременного уменьшения температуры и увеличения объема.
Готовые работы на аналогичную тему
Этот вывод теоретически подтверждает формула: $p = nkT$, ведь увеличение общего объема идеального газа ведет автоматически к уменьшению концентрации молекул изучаемого вещества, следовательно, уменьшение давления обусловливают два показателя — концентрация молекул $n$ и температура газа $T$.
Связь с первым началом термодинамики
Рисунок 2. Адиабатический процесс. Автор24 — интернет-биржа студенческих работ
Адиабатный процесс возможно легко связать с первым законом термодинамики. Его определение “по умолчанию” звучит следующим образом: изменение количества тепловой энергии в системе при протекании в ней определенного термодинамического процесса будет прямо пропорционально сумме изменения тепла идеального газа и работы, которая совершается данным элементом.
Если записывать первое начало термодинамики в его первоначальном, стандартном виде, то получим такое выражение: $dQ = dU + dA$. А теперь попробуем видоизменить это уравнение применительно к действию адиабатического процесса. Как было сказано ранее, подобные явление протекают только при условии отсутствия теплообмена с окружающей средой.
В таком случае новая формула, описывающая более детально первое начало термодинамики, примет уже совершенно иной вид: $dA = -dU$. Теперь немного подробнее о самом видоизменении.
Если говорить о том, что теплообмена между активно действующими в конкретной системе телами не происходит, тогда изменение количества тепловой энергии (обозначенное в уравнении первого термодинамического закона через $dQ$) будет в обязательно порядке равно нулю. Следовательно, можно перенести одну из слагаемых частей из правой части в левую, после чего получить модернизированную формулу, приведенную к описанному ранее виду.
Влияние первого начала термодинамики на адиабатический процесс
Рисунок 3. Первый закон термодинамики к различным процессам. Автор24 — интернет-биржа студенческих работ
Чтобы определить воздействие первого закона термодинамики на адиабатный процесс, необходимо чисто теоретически предположить, что в системе произошло уже данное явление. В этом случае возможно, не вдаваясь в мельчайшие нюансы и детали, утверждать, что газ при постепенном расширении совершает работу, но при этом теряет собственную внутреннюю энергию. Другими словами, совершаемая при адиабатном расширении газа работа будет осуществляться только посредством убыли энергетического потенциала.
Следовательно, в качестве недопущение такого исхода лучше применять понижение температуры действующего в системе вещества. Абсолютно логично можно определить, что, если газ будет адиабатически сжат, его тепловая энергия вырастет в несколько раз. Несложно заметить, что в ходе этого процесса будут изменяться все ключевые характеристики исследуемого вещества. Речь идет о его объеме, давлении и температуре. Поэтому, грубой ошибкой исследователей стало название адиабатического процесса изопроцессом.
Вскоре после того, как был открыт и описан адиабатический процесс, физики начали проводить огромное количество различных исследований. Так, была разработана первая теоретическая модель, которая имеет непосредственное отношение к универсальному циклу Карно. Именно она позволила ученым установить условные границы, ограничивавшие дальнейшее развитие тепловых машин. Однако в случае некоторых природных явлений осуществлять данную модель достаточно трудно. Все дело в том, что в его состав в основном входят изотермы, которые требуют изначального задания определенной скорости термодинамических процессов.
Использование адиабатного процесса в теоретических циклах тепловых машин
На самом деле на сегодняшний день более 90% электроэнергии вырабатывается только на тепловых электростанциях. В них в качестве рабочего тела применяется водяной пар, который возможно получают при кипении воды в адиабатном процессе.
По аналогии с устаревшими поршневыми автомобилями работают и турбинные. Но в них адиабатический процесс отвода тепловой энергии по завершении постепенного расширения газа выполняется исключительно по изобаре. На самолетах с турбовинтовым и газотурбинным двигателями изучаемое явление совершается дважды: при расширении и сжатии.
Чтобы обосновать все основополагающие и применяемые в науке понятия адиабатического процесса, ученые вывели расчетные формулы.
Здесь фигурирует одна основная величина, которая получила название параметр адиабаты. Его значение для двухатомного газа при любых условиях равно 1,4. Для расчета этого показателя адиабаты применяются две характеристики, а именно: изохорная и изобарная теплоемкости физического тела. Отношение их $k=\frac
Чтобы повысить и удержать рабочий потенциал пара, его желательно перегреть. Затем при максимально высоком давлении данный элемент подается на паровую турбину. Здесь также совершается адиабатический процесс расширения идеального пара. Турбина получает необходимое вращение, которое передается на электрогенератор. Тот, в свою очередь, вырабатывает электроэнергию для потребителей. В идеале увеличение эффективности лучше связать с повышением давления и температуры водяного пара. Как видно из вышесказанного, адиабатный процесс в термодинамике является достаточно распространенным в производстве электрической и механической энергий.
Адиабатический процесс | Все его важные концепции и графические кривые
Тема обсуждения: адиабатический процесс.
- Определение адиабатического процесса
- Примеры адиабатических процессов
- Формула адиабатического процесса
- Вывод адиабатического процесса
- Выполненная работа адиабатического процесса
- Обратимый адиабатический процесс и Необратимыйадиабатический процесс
- Адиабатический график
Определение адиабатического процесса
Соблюдая первый закон термодинамики, процесс, происходящий при расширении или сжатии, когда нет теплообмена от системы к окружающей среде, может быть известен как адиабатический процесс. В отличие от изотермического процесса, адиабатический процесс передает энергию окружающей среде в виде работы. Это может быть как обратимый, так и необратимый процесс.
В действительности, идеально адиабатический процесс никогда не может быть получен, поскольку ни один физический процесс не может происходить самопроизвольно, а система не может быть идеально изолирована.
Следуя первому закону термодинамики, который гласит, что когда энергия (как работа, тепло или материя) переходит в систему или из нее, внутренняя энергия системы изменяется в соответствии с законом сохранения энергии, где E можно обозначить как внутренняя энергия, а Q — это тепло, добавленное к системе, а W — проделанная работа.
ΔE=Q—W
Для адиабатического процесса, в котором нет теплообмена,
ΔE= —W
Условия, необходимые для протекания адиабатического процесса:
- Система должна быть полностью изолирована от окружающей среды.
- Чтобы передача тепла происходила за достаточное время, процесс должен выполняться быстро.
Адиабатический процесс Пример
- Процесс расширения в двигателе внутреннего сгорания среди горячих газов.
- Квантово-механический аналог осциллятора, классически известного как квантовый гармонический осциллятор.
- Сжиженные газы в системе охлаждения.
- Воздух, выпущенный из пневматической шины, является наиболее важным и частым случаем адиабатического процесса.
- Лед, хранящийся в морозильной камере, следует принципам, согласно которым тепло не передается в окружающую среду и обратно.
- Турбины, использующие тепло в качестве среды для создания работы, считаются отличным примером, поскольку они снижают эффективность системы, поскольку тепло теряется в окружающую среду.
Формула адиабатического процесса
Выражение адиабатического процесса в математических терминах может быть дано следующим образом:
ΔQ = 0
ΔU = -W, (так как в системе отсутствует тепловой поток)
Рассмотрим систему, в которой выполняется исключение теплового и рабочего взаимодействий в стационарном адиабатическом процессе. Единственные энергетические взаимодействия — это граничная работа системы в ее окружении.
Идеальный газ
Количество тепловой энергии на единицу температуры, недоступной для выполнения определенной работы, можно определить как энтропию системы. Спекулятивный газ, который представляет собой беспорядочное движение точечных частиц, подверженных межчастичным молекулярным взаимодействиям, идеален.
Молярная форма формулы идеального газа определяется следующим образом:
Уравнение адиабатического процесса можно обозначить как:
PVY = постоянный
Для обратимого адиабатического процесса
- P 1-Y T Y = постоянная,
- VT F / 2 = постоянная,
- TV Y-1 = константа. (T = абсолютная температура)
Этот процесс также известен как изэнтропический процесс, идеализированный термодинамический процесс, включающий передачу работы без трения и адиабатический. В этом обратимом процессе нет передачи тепла или работы.
Вывод адиабатического процесса
Изменение внутренней энергии dU в системе сделать работу dВт плюс добавленное тепло dQ с ним можно связать первый закон термодинамики, с помощью которого можно вывести адиабатический процесс.
Добавление тепла увеличивает количество энергии U определение удельной теплоемкости как количества тепла, добавляемого на единицу повышения температуры на 1 моль вещества.
(n — количество молей), Следовательно:
Получено из закон идеального газа,
Уравнение слияния 1 и 2,
Для постоянного давления Cp, добавляется тепло и,
γ — это удельная теплоемкость
Используя концепции интеграции и дифференциации, мы пришли к следующему:
Это уравнение, приведенное выше, становится реальным для данного идеального газа, который содержит адиабатический процесс.
Адиабатический процесс Работа выполнена.
Для давления P и площадь поперечного сечения A перемещение на небольшое расстояние dx, действующая сила будет определяться следующим образом:
А проделанную работу в системе можно записать так:
Чистая работа, произведенная для расширения газа из объема газа Vi к Vf (от начального до финального) будут представлены как
W = площадь ABDC от графика, построенного как имеет место адиабатический процесс. Условия, которые необходимо соблюдать, связаны с примером совершенно непроводящего поршневого цилиндра с одной граммовой молекулой идеального газа. Емкость баллона должна быть изготовлена из изоляционного материала, а кривая на графике должна быть более резкой.
Принимая во внимание, что в аналитическом методе для вывода работы, выполненной в системе, будет следующее:
Изначально для адиабатического изменения можно предположить:
Который может быть,
Из (1),
Принимая T1 и т2 как начальная и конечная температуры газа соответственно,
Используя это в уравнении (2),
Тепло, необходимое в процессе расширения для выполнения работы:
Поскольку R — универсальная газовая постоянная, и во время адиабатического расширения совершаемая работа прямо пропорциональна снижению температуры, в то время как работа, совершаемая во время адиабатического сжатия, отрицательна.
Это можно представить как работа, выполненная в адиабатическом процессе.
И тепло, выделяемое во время процесса:
Адиабатический график
Математическое представление кривой адиабатического расширения представлено следующим образом:
P, V, T — давление, объем и температура процесса. Рассматривая начальные условия системы как P1, V1, и т1, также определяя финальную стадию как P2, V2, и т2 соответственно, графическая диаграмма PV построена по существу для движения поршневого цилиндра, адиабатически нагретого от начального до конечного состояния для XNUMX кг воздуха.
Адиабатическая энтропия, адиабатическое сжатие и расширение
Газ, которому позволено свободно расширяться без передачи ему внешней энергии от более высокого давления к более низкому, будет по существу охлаждаться по закону адиабатического расширения и сжатия. Точно так же газ нагреется, если его сжать с более низкой температуры до более значительной температуры без передачи энергии веществу.
- Посылка воздуха расширится, если давление окружающего воздуха уменьшится.
- На больших высотах наблюдается снижение температуры из-за уменьшения давления, поскольку они прямо пропорциональны в случае этого процесса.
- Энергия может использоваться либо для работы по расширению, либо для поддержания температуры процесса, но не для того и другого одновременно.
Обратимый адиабатический процесс
Процесс без трения, в котором энтропия системы остается постоянной, получил название обратимого или обратимого. изоэнтропический процесс. Это означает, что изменение энтропии постоянно. Внутренняя энергия эквивалентна работе, совершаемой в процессе расширения.
Поскольку нет теплопередачи,
Которое значит что,
Примеры обратимого изоэнтропического процесса можно найти в газовые турбины.
Необратимый адиабатический процесс
Как следует из названия, процесс рассеяния внутреннего трения, приводящий к изменению энтропии системы во время расширения газов, является необратимым адиабатическим процессом.
Обычно это означает, что энтропия увеличивается по мере развития процесса, который не может быть выполнен в равновесии и не может быть отслежен до исходного состояния.
http://spravochnick.ru/fizika/termodinamika/adiabatnyy_process_v_termodinamike/
http://ru.lambdageeks.com/adiabatic-process/