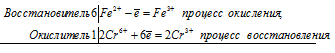Составление уравнений реакций, которые надо провести для осуществления превращений
Задание 392
Составьте уравнения реакций, которые надо провести для осуществления следующих превращений:
Cu → Cu(NO3)2 → Cu(OH)2 → CuCl2 → [Cu(NH3)4]Cl2
Решение:
а) 3Сu + 8HNO3 (разб.) = 3Сu(NO3)2 + 2NO↑ + 4H2O;
б) Сu(NO3)2 + 2NaOH = Cu(OH)2↓ + 2NaNO3;
в) Cu(OH)2 + 2HCl = CuCl2 + 2H2O;
г) CuCl2 + 4NH3 = [Cu(NH3)4]Cl2
Задание 394
Составьте уравнения реакций, которые надо провести для осуществления следующих превращений:
Ag → AgNO3 → AgCl → [Ag(NH3)2]Cl → AgCl
Решение:
Задание 416
Составьте уравнения реакций, которые надо провести для осуществления превращений:
Na2Cr2O7 → Na2CrO4 → Na2Cr2O7 → СгС13 → Сг(ОН)3
Уравнение окислительно-восстановительной реакции напишите на основании электронных уравнений.
Решение:
Уравнения реакций, которые надо провести для осуществления превращений:
Na2Cr2O7 → Na2CrO4 → Na2Cr2O7 → СгС13 → Сг(ОН
Под действием щёлочи дихромат-ионы Cr2O7 2- переходят в хромат-ионы CrO4. При подкислении растворов хроматов ионы CrO4 2- переходят в Cr2O7 2- .
в) Кислые растворы хроматов и дихроматов обладают окислительными свойствами. При их восстановлении жёлтая окраска хроматов или оранжевая дихроматов переходят в зеленную окраску, обусловленную присутствием ионов Cr 3+ .
6Fe 2+ + 2Cr 6+ = 6Fe 3+ + 2Cr 3+
г) При действии на соль CrCl3 раствором щёлочи выпадает осадок Сг(ОН)3:
Задание 427
Составьте уравнения реакций, которые надо провести для осуществления превращений:
Ni → N i(NO3)2 → Ni(OH)2 → Ni(ОН)3 → NiCl2
Уравнения окислительно-восстановительных реакций напишите на основании электронных уравнений.
Решение:
Уравнения реакций, которые надо провести для осуществления превращений:
а) Ni → N i(NO 3 ) 2 =
Для схемы превращений составьте уравнения реакций
Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
Напишем уравнения реакции, соответствующие схеме превращений:
1)
2)
3)
Составим сокращённое ионное уравнение для второго превращения:
4)
Можно ли записать реакцию в виде Сu(NO3)2=CuO+N2O5
Нет, потому что разложение нитрата меди выглядит так
Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
Напишем уравнения реакции, соответствующие схеме превращений:
1)
2)
3)
Составим сокращённое ионное уравнение для второго превращения:
4)
Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
Напишем уравнения реакции, соответствующие схеме превращений:
1)
2)
3)
Составим сокращённое ионное уравнение для третьего превращения:
4)
Химия, Биология, подготовка к ГИА и ЕГЭ
Вопрос А12 теста ЕГЭ по химии — «Взаимосвязь неорганических веществ»
Если посмотрите это задание в вариантах ЕГЭ, то там дана схема превращений неорганических веществ и в ответах даны варианты реагентов. Как решать такие задачи?
Темы, которые нужно знать:
Составить уравнения реакций по схеме превращений
На самом деле это не так и сложно. Для этого необходимо знать типы реакций и основные условия их протекания.
1. Химические реакции соединения
- Реакция горения — одна из самых распространенных химических реакций соединения — все вещества горят — и металлы, и неметаллы:
- Химические реакции соединения металла и неметалла — приводят к образованию солей:
(а вот этот момент надо запомнить (или выучить) — железо при взаимодействии с соляной кислотой дает хлорид железа (II), а с хлором — простым веществом — хлорид железа (III))
- Неметаллы также могут взаимодействовать между собой:
2. Составление уравнений реакций по схеме — реакции разложения
- Обычно уравнения реакций разложения солей дают соответствующие основные и кислотные оксиды:
Исключения:
- по-другому разлагаются нитраты — в зависимости от металла, входящего в состав соли. Это можно прочитать >;
- хлорид аммония — NH4Cl — разлагается до аммиака и соляной кислоты: NH4Cl = NH3 + HCl;
- не разлагаются сульфаты
- соли, образованные сильными окислителями:
- Разлагаются некоторые основания:
3. Составление уравнений реакций по схеме — п римеры реакций замещения
- реакция замещения водорода в кислотах:
когда нам дана реакция замещения металлом водорода в кислотах, нужно учитывать электрохимический ряд напряжений металлов: металлы, находящиеся в ряду ДО водорода, вытесняют его из кислот:
2Na + 2HCl = 2NaCl + H2
- реакции замещения в солях:
Ca + 2NaCl = CaCl2 +2 Na
Правило: предыдущий металл вытесняет последующий из его солей
(т.е. реакция Na + CaCl2 не будет идти)
4. Составление уравнений реакций по схеме — р еакции обмена веществ
Здесь следующие правила — обменные реакции идут в сторону образования продуктов при:
- выпадении осадка: NaCl + AgNO3 = AgCl↓ + NaNO3
- выделении газа: Na2CO3 + HCl = NaCl + CO2 + H2O ;
- образовании малодиссоциирующего вещества (H2O, NH4OH, органические кислоты и соли и т.д.): NaOH + H2SO3 = Na2SO3 + H2O
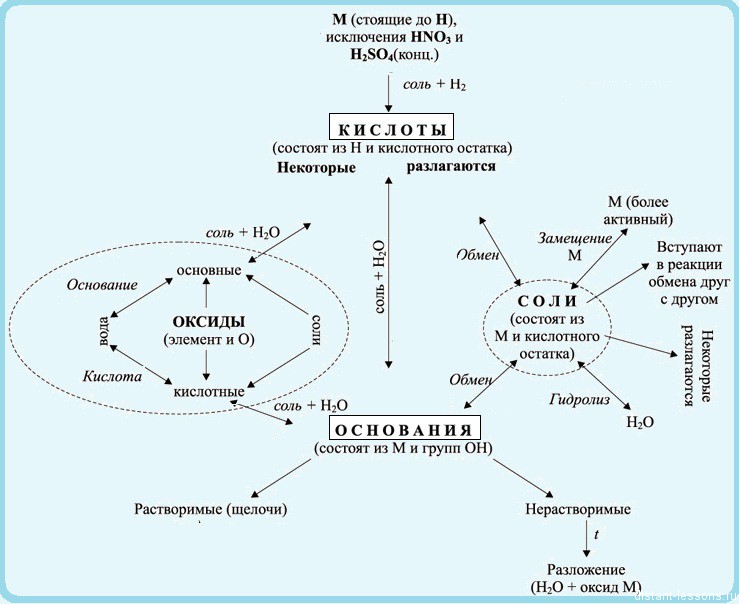
Взаимосвязь неорганических веществ можно отобразить такой таблицей:
Теория, это, конечно, хорошо, но давайте попрактикуемся — попробуем составить уравнения реакций по схемам превращений
В первой реакции к меди можно прибавить либо AgNO3, либо HNO3 — в ряду напряжений медь стоит до серебра, а азотная кислота будет давать окислительно-восстановительную реакцию.
Во второй части схемы нам подходит K2S или H2S, т.к. сульфид меди — осадок.
Ответ: 1)
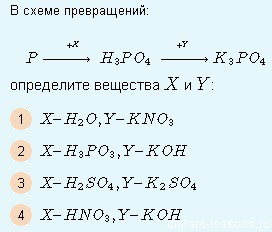
Составим уравнения реакций для данной схемы превращений:
Первая реакция — переход фосфора в фосфорную кислоту — такое под силу только мощным окислителям — либо серной, либо азотной кислоте.
Вторая реакция — обменная — K2SO4 даст растворимые продукты, а вот KOH — в самый раз! Получится вода — малодиссоциирующее вещество.
http://chem-oge.sdamgia.ru/test?theme=25
http://distant-lessons.ru/sostavit-uravneniya-reakcij-po-sxeme-prevrashhenij.html