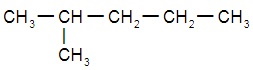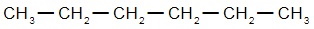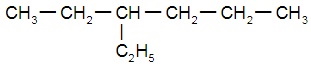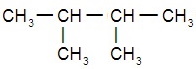Пентан: способы получения и химические свойства
Пентан C5H12 – это предельный углеводород, содержащий пять атомов углерода в углеродной цепи. Бесцветная жидкость с характерным запахом, нерастворим в воде и не смешивается с ней.
Гомологический ряд пентана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4. , или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Строение пентана
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp 3 :
При образовании связи С–С происходит перекрывание sp 3 -гибридных орбиталей атомов углерода:
При образовании связи С–H происходит перекрывание sp 3 -гибридной орбитали атома углерода и s-орбитали атома водорода:
Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:
Это соответствует тетраэдрическому строению.
| Например, в молекуле пентана C5H12 атомы водорода располагаются в пространстве в вершинах тетраэдров, центрами которых являются атомы углерода. При этом углеродный скелет имеет зигзагообразное строение. |
Изомерия пентана
Структурная изомерия
Для пентана характерна структурная изомерия – изомерия углеродного скелета.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета отличаются строением углеродного скелета.
| Например. Для углеводородов состава С5Н12 существуют три изомера углеродного скелета: н-пентан, метилбутан (изопентан), диметилпропан (неопентан) |
| Пентан | Изопентан |
| CH3-CH2-CH2-CH2-CH3 | CH3-CH(CH3)-CH2-CH3 |
Для пентана не характерна пространственная изомерия.
Химические свойства пентана
Пентан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для пентана характерны реакции:
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для пентана характерны радикальные реакции.
Пентан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование
Пентан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании пентана образуется смесь хлорпроизводных.
| Например, при хлорировании пентана образуются 1-хлорпентан, 2-хлорпентан и 3-хлорпентан: Бромирование протекает более медленно и избирательно.
Задание 1 Упражнение 2 Упражнение 3 Упражнение 4
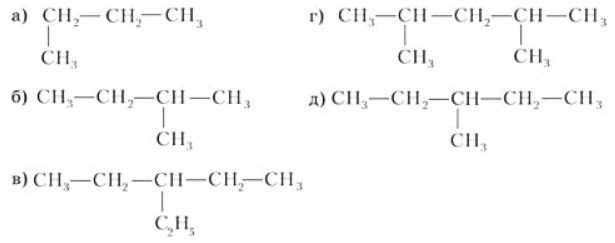
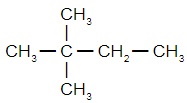
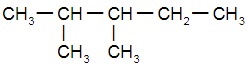
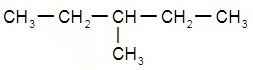
Структурные формулы изомеров н-гексана:
Упражнение 5 Упражнение 6 Упражнение 7 Упражнение 8 источники: http://reshimvse.com/zadacha.php?id=46533 http://gdz.cool/h10_gos_2019/808-h10_gos_2019_3___.html |