Электролиз солей
Самопроизвольные окислительно-восстановительные реакции дают возможность создания гальванических элементов, в которых вырабатывается электрическая энергия. Если же реакция несамопроизвольна, то ее осуществление возможно при помощи электрической энергии. Подобные процессы осуществляют в электролизерах и называются они реакциями электролиза (электролиз солей).
Электролизер
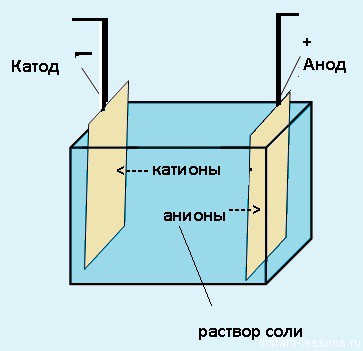
Как видно на рисунке ниже, электролизер состоит из двух электродов, погруженных в расплав или водный раствор соли. Источник электрического тока передает электроны в один из электродов и удаляет их с другого электрода. При отдаче электронов электрод заряжается положительно, а при получении электронов – отрицательно.
Электролиз расплава NaCl
При электролизе расплава NaCl на отрицательном электроде (катоде) происходит присоединение электронов ионом натрия Na + и его восстановление. При этом вблизи электрода концентрация ионов Na + уменьшается и, вследствие этого, к электроду перемещается дополнительное количество ионов Na + .
Аналогично происходит миграция ионов Cl — к положительному электроду, где в результате отдачи электронов протекает процесс окисления. Таким образом, на электродах идет накопление продуктов окисления и восстановления.
Как и в гальваническом элементе, процесс восстановления протекает на катоде, а процесс окисления – на аноде.
При электролизе расплава NaCl протекают следующие реакции:
| Анод | 2Cl — -2e — → Cl2 0 |
| Катод | 2Na + + 2e — → 2Na 0 |
| 2Na + + 2Cl — → 2Na 0 + Cl2 0 |
В промышленности таким образом получают натрий, используя электролизер Даунса, представленный на рисунке ниже.
Сложнее протекает электролиз водных растворов электролитов.
Электролиз водного раствора NaCl
Так, например, при электролизе водного раствора хлорида натрия, происходят иные процессы, нежели при электролизе его расплава. На катоде происходит восстановление воды, а не натрия; на аноде происходит окисление хлорид-ионов:
| Анод | 2Cl — -2e — → Cl2 0 |
| Катод | 2H 2 O + 2e — → H2 0 +2OH — |
| 2H2O + 2Cl — → H2 0 + Cl2 0 |
Таким образом, получить натрий путем электролиза водного раствора его соли не удастся: на катоде выделяется водород, а на аноде хлор.
При электролизе водных растворов солей окислительно-восстановительные процессы, протекающие на катоде и аноде зависят от природы катионов металлов и характера аниона соли.
Процесс на катоде
Предсказать результат восстановительного процесса на катоде можно с помощью таблицы стандартных электродных потенциалов металлов:
- Катионы металлов, имеющие большую величину стандартного потенциала и расположенные в ряду после водорода полностью восстанавливаются на катоде и выделяются в виде металлов: Cu 2+ , Hg2 2+ , Ag + , Hg 2+ , Pt 2+ до Pt 4+
- Катионы металлов, имеющие малую величину стандартного потенциала не восстанавливаются на катоде, вместо этого происходит восстановление воды: от Li + , Na + … до Al 3+ включительно.
- Катионы металлов, имеющие среднюю величину стандартного потенциала будут восстанавливаться на катоде вместе с молекулами воды: от Mn 2+ , Zn 2+ … до H
Если имеется смесь катионов, то легче всего на катоде будут восстанавливаться катионы металла с наиболее положительным потенциалом, например, из смеси Cu 2+ , Ag + , Zn 2+ сначала восстановится Ag + (E = +0,79 В), затем Cu 2+ (E = +0,337 В) и только потом Zn 2+ (E = +0,76 В).
Процесс на аноде
Какие процессы будут протекать на аноде зависит от материала анода и самого электролита. Нерастворимые аноды в процессе электролиза не окисляются, тогда как растворимые аноды разрушаются и в виде ионов переходят в раствор.
Рассмотрим процессы, происходящие на инертном (нерастворимом) аноде:
- При электролизебескислородных кислот и их солей (исключение HF и фториды) на аноде окисляются их анионы.
2Cl — -2e — = Cl2
- При электролизекислородсодержащих кислот и их солей c максимальной степенью окисления на аноде происходит окисление воды, в связи с тем, что потенциал окисления воды меньше, чем для таких анионов.
2H2O -4e — = O2 + 4H +
- При электролизе кислородсодержащих кислот и их солей c промежуточной степенью окисления на аноде происходит окисление анионов кислот
SO3 2- + H2O -2e — = SO4 2- + 2H +
В таблице ниже представлены наиболее типичные случаи электролиза с химической точки зрения
| Водный раствор соли малоактивного металла и бескислородной кислоты с инертным анодом | CuBr2 + H2O = Cu + Br2 + H2O K: Cu 2+ + 2e — = Cu |
| Водный раствор соли активного металла и кислородсодержащей кислоты с инертным анодом | K2SO4 + 2H2O = K2SO4 + 2H2 + O2 Т.е. происходит разложение воды |
| Водный раствор соли активного металла и бескислородной кислоты с инертным анодом | KI + H2O = 2KOH + H2 + I2 |
| Водный раствор соли малоактивного металла с анодом из того же металла | CuSO4 K: Cu 2+ + 2e — = Cu A: Cu — 2e — = Cu 2+ Электролиз солей — количественные аспектыСвязь между количеством вещества, выделившегося при электролизе соли и количеством прошедшего через него электричества отражена в законах Фарадея. 1 закон Фарадея
где k – коэффициент пропорциональности или электрохимический эквивалент, численно равный массе вещества, которое выделяется при прохождении 1 кулона электричества. 2 закон Фарадея
Т.е. чтобы выделился один химический эквивалент любого соединения необходимо приложить одинаковое количество электричества, которое равно 96484,56 Кл/моль. Это величина называется постоянной Фарадея. m – масса вещества, Э – электрохимический эквивалент, t – время электролиза. Законы Фарадея имеют большое значение при проведении расчетов, связанных с электролизом. Задачи с решениями на составление уравнений электродных реакций, протекающих при электролизе, а также на применение законов Фарадея приведены в разделе Задачи к разделу Электролиз солей 29. Электролиз расплавов и растворовЭлектролиз расплавов и растворов (солей, щелочей, кислот) 1 .Установите соответствие между формулой соли и уравнением процесса, протекающего на аноде при электролизе её водного раствора. ФОРМУЛА СОЛИ УРАВНЕНИЕ АНОДНОГО ПРОЦЕССА А) KCl 1) 2H 2 O – 4e → O 2 + 4H + В ) CuSO 4 3) 2Cl — -2e → Cl 2 0 Г ) AgNO 3 4) 2Br — — 2e → Br 2 0 2. Установите соответствие между формулой соли и продуктом, образующимся на инертном аноде при электролизе её водного раствора. ФОРМУЛА СОЛИ ПРОДУКТ, ОБРАЗУЮЩИЙСЯ НА АНОДЕ А) RbSO 4 1) метан Б) CH 3 COOK 2) сернистый газ В) BaBr 2 3) кислород Г) CuSO 4 4) водород 6) этан и углекислый газ 3. Установите соответствие между формулой соли и уравнением процесса, протекающего на катоде при электролизе её водного раствора. ФОРМУЛА СОЛИ УРАВНЕНИЕ КАТОДНОГО ПРОЦЕССА Б ) CuCl 2 2) 2H 2 O + 2e → H 2 + 2OH — В ) SbCl 3 3) Cu 2+ + 2e → Cu 0 Г ) Cu(NO 3 ) 2 4) Cu 2+ + 1e → Cu + 4. Установите соответствие между названием вещества и способом его получения. НАЗВАНИЕ ВЕЩЕСТВА ПОЛУЧЕНИЕ ЭЛЕКТРОЛИЗОМ А) литий 1) раствора LiF Б) фтор 2) расплава LiF В) серебро 3) раствора MgCl 2 Г) магний 4) раствора AgNO 3 5) расплава Ag 2 O 6) расплава MgCl 2 5. Установите соответствие между названием вещества и продуктами электролиза его водного раствора НАЗВАНИЕ ВЕЩЕСТВА ПРОДУКТЫ ЭЛЕКТРОЛИЗА А) бромид калия 1) водород, бром, гидроксид калия Б) сульфат меди ( II) 2) натрий, углекислый газ В) бромид меди ( II) 3) медь, оксид серы ( IV) 4) медь, кислород, серная кислота 6. Установите соответствие между названием вещества и основными газообразными продуктами электролиза его водного раствора. НАЗВАНИЕ ВЕЩЕСТВА ГАЗООБРАЗНЫЕ ПРОДУКТЫ ЭЛЕКТРОЛИЗА А) хлорид кальция 1) кислород, водород Б) нитрат кальция 2) водород, хлор В) фторид серебра 3) оксид азота ( IV) Г) нитрат серебра 4) кислород 7. Установите соответствие между названиями вещества и электролитическим способом его получения. НАЗВАНИЕ ВЕЩЕСТВА ЭЛЕКТ РОЛИЗ А) хлор 1) водного раствора хлорида меди Б) этан 2) водного раствора бромида натрия В) натрий 3) водного раствора ацетата калия Г) бром 4) расплава фторида натрия 5) водного раствора перхлората калия 6) водного раствора этановой кислоты 8. Установите соответствие между формулой вещества и продуктами электролиза его водного раствора на инертных электродах. ФОРМУЛА ВЕЩЕСТВА ПРОДУКТЫ ЭЛЕКТРОЛИЗА А) натрий 1) водного раствора солей Б) алюминий 2) водного раствора гидроксида В) серебро 3) расплава поваренной соли Г) медь 4) расплавленного оксида 5) раствора оксида в расплавленном криолите 9. Установите соответствие между формулой вещества и продуктами электролиза его водного раствора на инертных электродах. ФОРМУЛА ВЕЩЕСТВА ПРОДУКТЫ ЭЛЕКТРОЛИЗА А) AlCl 3 1) металл, галоген Б) RbOH 2) гидроксид металла, хлор, водород В) Hg(NO 3 ) 2 3) металл, кислород Г) AuCl 3 4) металл, кислота, кислород 5) водород, кислород 6) водород, галоген 10. Установите соответствие между формулой соли и реакцией ее водного раствора Химия, Биология, подготовка к ГИА и ЕГЭЭлектролиз водных растворов солейТема электролиза довольна большая, формул в ней много и, как мне кажется, больше ее изучают на уроках физики… Я хочу рассмотреть ту часть, которая касается химии, и при этом только формат ЕГЭ — электролиз водных растворов солей. Электролиз водных растворов солей Для начала давайте представим себе систему, в которой происходит электролиз.
Электроды — это такие пластинки или стержни, опущенные в раствор, они подключены к источнику тока.
Мы будем рассматривать случай инертных электродов — т.е. они не будут вступать ни в какие химические реакции. При пропускании электрического тока, вещество раствора будет претерпевать химические изменения, т.е. буду образовываться новые химические вещества. Они будут притягиваться к электродам следующим образом:
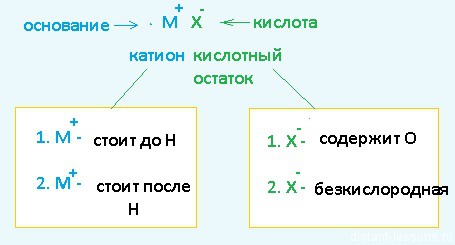
Теперь рассмотрим электролиз водных растворов различных солей Разберем сначала катионы :
Теперь анионы-кислотные остатки :
Примеры: 1 .1. Катион стоит в ряду до Н, кислотный остаток содержит кислород О: 1.2. Катион стоит в ряду до Н, кислотный остаток беcкислородный: анод (+): Cl − — 1e = Cl 0 ; Cl 0 +Cl 0 =Cl2 2.1. Катион стоит в ряду после Н, кислотный остаток содержит кислород О: K(-): Cu 2+ + 2e = Cu 0 2.2. Катион стоит в ряду после Н, кислотный остаток беcкислородный: катод (-): Cu 2+ + 2e = Cu 0 анод (+): 2Cl − — 2e = 2Cl 0 Электролиз водных растворов солей отличается от электролиза расплавов.
Обсуждение: «Электролиз водных растворов солей»Здравствуйте. Очень благодарна вам за такое понятное объяснение темы. Водород — правильный ответ. В ответах к тренировочным тестам ЕГЭ очень часто бывают ошибки. Да и не только в ответах. В этом году, например, в заданиях пробных ЕГЭ быди ошибки! 1. Запишите все возможные процессы на аноде, установите потенциалы процессов. 2. Сравните потенциалы анодных процессов и определите, какой из них протекает в первую очередь? 3. Выясните, меняется ли среда около анода, если да, то как и почему? 4. Запишите все возможные процессы на катоде, установите потенциалы процессов. 5. Сравните потенциалы катодных процессов и определите, какой из них протекает в первую очередь. 6. Установите, меняется ли среда около катода, если да, то как и почему? 7. Запишите итоговую схему процесса электролиза. 0,1 M раствор CuSO4 pH = 5, катод – Al, анод – Сu здесь решают задачи школьного уровня. Не сможем вам помочь источники: http://maratakm.narod.ru/index2.files/b3.htm http://distant-lessons.ru/ximiya/elektroliz |