Запишите уравненеие реакции электролиза (инертный электрод ) нитрата никеля, гидроксида никеля, азотной кислоты
Запишите уравненеие реакции электролиза (инертный электрод ) нитрата никеля, гидроксида никеля, азотной кислоты
Электролиз нитрата никеля в водном растворе:
2NI(NO3)2 + 2H2O = 2Ni + O2 + 4HNO3
На катоде (+): Ni(2+) + 2e = Ni—————x2
на аноде (-): 2H2O — 4e = O2 + 4H(+)——x1
———————————
NI(OH)2 + H2O = H2 + O2 + Ni(OH)2
здесь гидроксид никеля не будет участвовать в электролизе, поскольку он не растворим в воде. Вместо него электролизу подвергается вода
—————————
С азотной кислотой та же ситуация, электролизу подвергается вода
Электролиз раствора нитрата никеля уравнение
Одним из способов получения металлов является электролиз. Активные металлы встречаются в природе только в виде химических соединений. Как выделить из этих соединений в свободном состоянии?
Растворы и расплавы электролитов проводят электрический ток. Однако при пропускании тока через раствор электролита могут происходить химические реакции. Рассмотрим, что будет происходить, если в раствор или расплав электролита поместить две металлические пластинки, каждая из которых соединена с одним из полюсов источника тока. Эти пластинки называются электродами. Электрический ток представляет собой движущийся поток электронов. В результате того, что электроны в цепи движутся от одного электрода к другому, на одном из электродов возникает избыток электронов. Электроны имеют отрицательный заряд, поэтому этот электрод заряжается отрицательно. Его называют катодом. На другом электроде создается недостаток электронов, и он заряжается положительно. Этот электрод называют анодом. Электролит в растворе или расплаве диссоциирует на положительно заряженные ионы — катионы и отрицательно заряженные ионы — анионы. Катионы притягиваются к отрицательно заряженному электроду — катоду. Анионы притягиваются к положительно заряженному электроду — аноду. На поверхности электродов может происходить взаимодействие между ионами и электронами.
Электролизом называются процессы, происходящие при пропускании через растворы или расплавы электролитов электрического тока.
Процессы, происходящие при электролизе растворов и расплавов электролитов, достаточно сильно отличаются. Рассмотрим подробно оба этих случая.
В качестве примера рассмотрим электролиз расплава хлорида натрия. В расплаве хлорид натрия диссоциирует на ионы Na +
и Cl — : NaCl = Na + + Cl —
Катионы натрия перемещаются к поверхности отрицательно заряженного электрода — катода. На поверхности катода имеется избыток электронов. Поэтому происходит передача электронов от поверхности электрода к ионам натрия. При этом ионы Na + превращаются в атомы натрия, то есть происходит восстановление катионов Na + . Уравнение процесса:
Хлорид-ионы Cl — перемещаются к поверхности положительно заряженного электрода — анода. На поверхности анода создан недостаток электронов и происходит передача электронов от анионов Cl — к поверхности электрода. При этом отрицательно заряженные ионы Cl — превращаются в атомы хлора, которые сразу же соединяются в молекулы хлора С l 2 :
2С l — -2е — = Cl 2
Хлорид-ионы теряют электроны, то есть происходит их окисление.
Запишем вместе уравнения процессов, происходящих на катоде и аноде
2 С l — -2 е — = Cl2
В процессе восстановления катионов натрия участвует один электрон, а в процессе окисления ионов хлора — 2 электрона. Однако должен соблюдаться закон сохранения электрического заряда, то есть общий заряд всех частиц в растворе должен быть постоянным Следовательно, число электронов, участвующих в восстановлении катионов натрия, должно быть равно числу электронов, участвующих в окислении хлорид-ионов Поэтому первое уравнение умножим на 2:
2С l — -2е — = Cl 2 1
Сложим вместе оба уравнения и получим общее уравнение реакции.
2 Na + + 2С l — = 2 Na + Cl 2 (ионное уравнение реакции), или
2 NaCl = 2 Na + Cl 2 (молекулярное уравнение реакции)
Итак, на рассмотренном примере мы видим, что электролиз является окислительно-восстановительной реакцией. На катоде происходит восстановление положительно заряженных ионов — катионов, на аноде окисление отрицательно заряженных ионов – анионов. Запомнить, какой процесс где происходит, можно с помощью «правила Т»:
каТод — каТион – воссТановление.
Пример 2. Электролиз расплава гидроксида натрия.
Гидроксида натрия в растворе диссоциирует на катионы и гидроксид-ионы .
Катод (-) Na + + OH — à Анод (+)
На поверхности катода происходит восстановление катионов натрия, при этом образуются атомы натрия:
катод (-) Na + +e à Na
На поверхности анода окисляются гидрокисд-ионы, при этом выделяется кислород и образуются молекулы воды:
анод (+) 4 OH — – 4 e à 2 H 2 O + O 2
Запишем вместе уравнения процессов, происходящих на катоде и аноде:
катод (-) Na + + e à Na
анод (+) 4 OH — – 4 e à 2 H 2 O + O 2
Число электронов, участвующих в реакции восстановления катионов натрия и в реакции окисления гидроксид-ионов, должно быть одинаковым. Поэтому умножим первое уравнение на 4:
катод (-) Na + + e à Na 4
анод (+) 4 OH — – 4 e à 2 H 2 O + O 2 1
Сложим вместе оба уравнения и получим уравнение реакции электролиза:
4 NaOH à 4 Na + 2 H 2 O + O 2
Пример 3. Рассмотрим электролиз расплава Al 2 O 3
При помощи этой реакции получают алюминий из боксита – природного соединения, в котором содержится много оксида алюминия. Температура плавления оксида алюминия очень высокая (более 2000º С), поэтому к нему добавляют специальные добавки, понижающие температуру плавления до 800-900º С. В расплаве оксид алюминия диссоциирует на ионы Al 3+ и O 2- . H а катоде восстанавливаются катионы Al 3+ , превращаясь в атомы алюминия:
На аноде окисляются анионы O 2- , превращаясь в атомы кислорода. Атомы кислорода сразу же соединяются в молекулы О2:
2 O 2- – 4 e à O 2
Число электронов, участвующих в процессах восстановления катионов алюминия и окисления ионов кислорода, должно быть равно, поэтому умножим первое уравнение на 4, а второе на 3:
Al 3+ +3 e à Al 0 4
2 O 2- – 4 e à O 2 3
Сложим оба уравнения и получим общее уравнение электролиза:
4 Al 3+ + 6 O 2- à 4 Al 0 +3 O 2 0 (ионное уравнение реакции)
В случае пропускания электрического тока через водный раствор электролита дело осложняется тем, что в растворе присутствуют молекулы воды, которые также могут взаимодействовать с электронами. Вспомним, что в молекуле воды атомы водорода и кислорода связаны полярной ковалентной связью. Электроотрицательность кислорода больше, чем электроотрицательность водорода, поэтому общие электронные пары смещены к атому кислорода. На атоме кислорода возникает частичный отрицательный заряд, его обозначают δ-, а на атомах водорода -частичный положительный заряд, его обозначают δ+.
Благодаря такому смещению зарядов молекула воды имеет положительный и отрицательный «полюса». Поэтому молекулы воды могут положительно заряженным полюсом притягиваться к отрицательно заряженному электроду — катоду, а отрицательным полюсом — к положительно заряженному электроду — аноду. На катоде может происходить восстановление молекул воды, при этом выделяется водород:
На аноде может происходить окисление молекул воды с выделением кислорода:
Поэтому на катоде могут восстанавливаться либо катионы электролита, либо молекулы воды. Эти два процесса как бы конкурируют между собой. Какой процесс в действительности происходит на катоде, зависит от природы металла. Будут ли на катоде восстанавливаться катионы металла или молекулы воды, зависит от положения металла в ряду напряжений металлов.
Li K Na Ca Mg Al ¦¦ Zn Fe Ni Sn Pb (H2) ¦¦ Cu Hg Ag Au
Если металл находится в ряду напряжений правее водорода, на катоде восстанавливаются катионы металла и выделяется свободный металл. Если металл находится в ряду напряжений левее алюминия, на катоде восстанавливаются молекулы воды и выделяется водород. Наконец, в случае катионов металлов от цинка до свинца может происходить либо выделение металла, либо выделение водорода, а иногда одновременно выделяются и водород, и металл. Вообще это довольно сложный случай, многое зависит от условий реакции: концентрации раствора, сипы электрического тока и других.
На аноде также может происходить один из двух процессов — либо окисление анионов электролита, либо окисление молекул воды. Какой именно процесс будет протекать на самом деле, зависит от природы аниона. При электролизе солей бескислородных кислот или самих кислот на аноде окисляются анионы. Единственным исключением является фторид-ион F — . В случае кислородсодержащих кислот на аноде окисляются молекулы воды и выделяется кислород.
Пример 1. Давайте рассмотрим электролиз водного раствора хлорида натрия.
В водного растворе хлорида натрия будут находиться катионы натрия Na + , анионы хлора Cl — и молекулы воды.
2 NaCl à 2 Na + + 2 Cl —
2Н2О à 2 H + + 2 OH —
катод (-) 2 Na + ; 2 H + ; 2Н + + 2е à Н 0 2
анод (+) 2 Cl — ; 2 OH — ; 2 Cl — – 2е à 2 Cl 0
Химическая активность анионов в ряду уменьшается.
Пример 2. А если в состав соли входит SO 4 2- ? Рассмотрим электролиз раствора сульфата никеля ( II ). Сульфата никеля ( II ) диссоциирует на ионы Ni 2+ и SO 4 2- :
Катионы никеля находятся между ионами металлов Al 3+ и Pb 2+ , занимающих в ряду напряжения среднее положение, процесс восстановления на катоде происходит по обеим схемам:
катод (-) Ni 2+ ; H + ; Ni 2+ + 2е à Ni 0
Анионы кислородсодержащих кислот не окисляются на аноде ( ряд активности анионов), происходит окисление молекул воды:
анод (+) SO4 2- ; OH — ; 2H2O – 4 е à O2 + 4H +
Запишем вместе уравнения процессов, происходящих на катоде и аноде:
катод (-) Ni 2+ ; H + ; Ni 2+ + 2е à Ni 0
анод (+) SO4 2- ; OH — ; 2H2O – 4 е à O2 + 4H +
В процессах восстановления участвуют 4 электрона и в процессе окисления тоже участвуют 4 электрона. Сложим вместе эти уравнения и получим общее уравнение реакции:
Ni 2+ +2 H 2 О + 2 H 2 О à Ni 0 + H 2 + 2ОН — + O 2 + 4 H +
В правой части уравнения находятся одновременно ионы Н + и OH — , которые соединяются с образованием молекул воды:
Н + + OH — à H 2 О
Поэтому в правой части уравнения вместо 4 ионов Н + и 2 ионов OH — запишем 2 молекулы воды и 2 иона Н + :
Ni 2+ +2 H 2 О + 2 H 2 О à Ni 0 + H 2 +2 H 2 О + O 2 + 2 H +
Сократим по две молекулы воды в обеих частях уравнения:
Ni 2+ +2 H 2 О à Ni 0 + H 2 + O 2 + 2 H +
Это краткое ионное уравнение. Чтобы получить полное ионное уравнение, нужно добавить в обе части по сульфат-иону SO 4 2- , образовавшиеся при диссоциации сульфата никеля ( II ) и не участвовавшие в реакции:
Таким образом, у нас при электролизе раствора сульфата никеля ( II ) на катоде выделяется водород и никель, а на аноде – кислород.
Пример 3. Написать уравнения процессов, происходящих при электролизе водного раствора сульфата натрия с инертным анодом.
Стандартный электродный потенциал системы Na + + e = Na 0 значительно отрицательнее потенциала водного электрода в нейтральной водной среде (-0,41 В).Поэтому на катоде будет происходить электрохимическое восстановление воды, сопровождающееся выделением водорода
2Н2О à 2 H + + 2 OH —
а ионы Na + , приходящие к катоду, будут накапливаться в прилегающей к нему части раствора (катодное пространство).
На аноде будет происходить электрохимическое окисление воды, приводящее к выделению кислорода
2 H 2 O – 4е à O 2 + 4 H +
поскольку отвечающий этой системе стандартный электродный потенциал (1,23 В) значительно ниже, чем стандартный электродный потенциал (2,01 В), характеризующий систему
Ионы SO 4 2- , движущиеся при электролизе к аноду, будут накапливаться в анодном пространстве.
Умножая уравнение катодного процесса на два, и складывая его с уравнением анодного процесса, получаем суммарное уравнение процесса электролиза:
6 H 2 O = 2 H 2 + 4 OH — + O 2 + 4 H +
Приняв во внимание, что одновременно происходит накопление ионов в катодном пространстве и ионов в анодном пространстве, суммарное уравнение процесса можно записать в следующей форме:
Таким образом, одновременно с выделением водорода и кислорода образуется гидроксид натрия (в катодном пространстве) и серная кислота (в анодном пространстве).
Пример 4. Электролиз раствора сульфата меди ( II ) CuSO 4 .
Катод (-) 2+ + SO4 2- à анод (+)
катод (-) Cu 2+ + 2e à Cu 0 2
анод (+) 2H2O – 4 е à O2 + 4H + 1
В растворе остаются ионы Н + и SO 4 2- , т. к. накапливается серная кислота.
Пример 5. Электролиз раствора хлорида меди ( II ) CuCl 2 .
Катод (-) 2+ + 2Cl — à анод (+)
катод (-) Cu 2+ + 2e à Cu 0
анод (+) 2Cl — – 2e à Cl 0 2
В обоих уравнениях участвуют по два электрона.
Cu 2+ + 2e à Cu 0 1
2Cl — -– 2e à Cl2 1
Cu 2+ + 2 Cl — à Cu 0 + Cl 2 (ионное уравнение)
CuCl 2 à Cu + Cl 2 (молекулярное уравнение)
Пример 6. Электролиз раствора нитрата серебра AgNO 3 .
Катод (-) + + NO3 — à Анод (+)
катод (-) Ag + + e à Ag 0
Ag + + e à Ag 0 4
4 Ag + + 2 H 2 O à 4 Ag 0 + 4 H + + O 2 (ионное уравнение)
4 Ag + + 2 H 2 O à 4 Ag 0 + 4 H + + O 2 + 4 NO 3 — (полное ионное уравнение)
4 AgNO 3 + 2 H 2 O à 4 Ag 0 + 4 HNO 3 + O 2 (молекулярное уравнение)
Пример 7. Электролиз раствора соляной кислоты HCl .
Катод (-) H + + Cl — à анод (+)
катод (-) 2 H + + 2 e à H 2
анод (+) 2 Cl — – 2 e à Cl 2
2 H + + 2 Cl — à H 2 + Cl 2 (ионное уравнение)
2 HCl à H 2 + Cl 2 (молекулярное уравнение)
Пример 8. Электролиз раствора серной кислоты H 2 SO 4 .
Катод (-) + + SO4 2- à анод (+)
катод (-) 2H+ + 2e à H2
Пример 9. Электролиз раствора гидроксида калия KOH .
Катод (-) K + + OH — à анод (+)
Катионы калия не будут восстанавливаться на катоде, так как калий находится в ряду напряжения металлов левее алюминия, вместо этого будет происходить восстановление молекул воды:
катод (-) 2H2O + 2e à H2 +2OH — 2
анод (+) 4OH — — 4e à 2H2O +O2 1
Пример 10. Электролиз раствора нитрата калия KNO 3 .
катод (-) 2H2O + 2e à H2 + 2OH- 2
анод (+) 2H2O – 4 е à O2 + 4H+ 1
При пропускании электрического тока через растворы кислородосодержащих кислот, щелочей и солей кислородсодержащих кислот с металлами, находящимися в ряду напряжения металлов, левее алюминия, практически происходит электролиз воды. При этом на катоде выделяется водород, а на аноде кислород.
Выводы. При определении продуктов электролиза водных растворов электролитов можно в простейших случаях руководствоваться следующими соображениями:
1. Ионы металлов с малой алгебраической величиной стандартного потенциала – от Li + до Al 3+ включительно – обладают весьма слабой тенденцией к обратному присоединению электронов, уступая в этом отношении ионам H + (см. Ряд активности катионов). При электролизе водных растворов соединений, содержащих эти катионы, функцию окислителя на катоде выполняют ионы H + , восстанавливаясь при этом по схеме:
2 H 2 O + 2 е à H 2 + 2OH —
2. Катионы металлов с положительными значениями стандартных потенциалов ( Cu 2+ , Ag + , Hg 2+ и др.) обладают большой тенденцией к присоединению электронов по сравнению с ионами. При электролизе водных растворов их солей функцию окислителя на катоде выделяют эти катионы, восстанавливаясь при этом до металла по схеме, например:
Cu 2+ +2 e à Cu 0
3. При электролизе водных растворов солей металлов Zn , Fe , Cd , Ni и др., занимающих в ряду напряжения среднее положение между перечисленными группами, процесс восстановления на катоде происходит по обеим схемам. Масса, выделившегося металла не соответствует в этих случаях количеству протекшего электрического тока, часть которого расходуется на образование водорода.
4. В водных растворах электролитов функцию восстановителей по отношению к аноду-окислитею могут одноатомные анионы ( Cl — , Br — , J — ), кислородосодержащие анионы ( NO 3 — , SO 4 2- , PO 4 3- и другие), а также гидроксильные ионы воды. Более сильными восстановительными свойствами из них обладают галогенид ионы, за исключением F . Ионы OH занимают промежуточное положение между ними и многоатомными анионами. Поэтому при электролизе водных растворов HCl , HBr , HJ или их солеей на аноде происходит окисление галогенид-ионов по схеме:
2 X — -2 e à X 2 0
При электролизе водных растворов сульфатов, нитратов, фосфатов и т.п. функцию восстановителя выполняют ионы , окисляясь при этом по схеме:
4 HOH – 4 e à 2 H 2 O + O 2 + 4 H +
З а дача 1. При электролизе раствора сульфата меди на катоде выделилось 48 г меди. Найдите объем газа, выделившегося на аноде, и массу серной кислоты, образовавшейся в растворе.
Сульфат меди в растворе диссоциирует ни ионы Си 2+ и S 04 2 ‘.
Запишем уравнения процессов, происходящих на катоде и аноде. На катоде восстанавливаются катионы Си , на аноде происходит электролиз воды:
2H20-4e- = 4H + + 02 
Общее уравнение электролиза:
2Cu2+ + 2H2O = 2Cu + 4H+ + O2 (краткоеионное уравнение)
Добавим в обе части уравнения по 2 сульфат-иона, которые образуются при диссоциации сульфата меди, получим полное ионное уравнение:
2Си2+ + 2S042″ + 2Н20 = 2Cu + 4Н+ + 2SO4 2′ + О2
Перепишем уравнение в молекулярном виде:
2CuSO4 + 2H2O = 2Cu + 2H2SO4 + О2
Газ, выделяющийся на аноде — кислород. В растворе образуется серная кислота.
Молярная масса меди равна 64 г/моль, вычислим количество вещества меди:
По уравнению реакции при выделении на катоде 2 моль меди ла аноде выделяется 1 моль кислорода. На катоде выделилось 0,75 моль меди, пусть на аноде выделилось х моль кислорода. Составим пропорцию:
На аноде выделилось 0,375 моль кислорода,
Вычислим объем выделившегося кислорода:
V(O2) = v(O2)«VM = 0,375 моль«22,4 л/моль = 8,4 л
По уравнению реакции при выделении на катоде 2 моль меди в растворе образуется 2 моль серной кислоты, значит, если на катоде выделилось 0,75 моль меди, то в растворе образовалось 0,75 моль серной кислоты, v(H2SO4) = 0,75 моль. Вычислим молярную массу серной кислоты:
M(H2SO4) = 2-1+32+16-4 = 98 г/моль.
Вычислим массу серной кислоты:
m(H2S04) = v(H2S04>M(H2S04) = = 0,75 моль«98 г/моль = 73,5 г.
Ответ: на аноде выделилось 8,4 л кислорода; в растворе образовалось 73,5 г серной кислоты
Задача 2. Найдите объем газов, выделившихся на катоде и аноде, при электролизе водного раствора, содержащего 111,75 г хлорида калия. Какое вещество образовалось в растворе? Найдите его массу.
Хлорид калия в растворе диссоциирует на ионы К+ и Сl:
Ионы калия не восстанавливаются на катоде, вместо этого происходит восстановление молекул воды. На аноде окисляются хлорид-ионы и выделяется хлор:
2Н2О + 2е’ = Н2 + 20Н- |1
Общее уравнение электролиза:
2СГl+ 2Н2О = Н2 + 2ОН» + С12 (краткое ионное уравнение) В растворе присутствуют также ионы К+, образовавшиеся при диссоциации хлорида калия и не участвующие в реакции:
2К+ + 2Сl + 2Н20 = Н2 + 2К+ + 2ОН’ + С12
Перепишем уравнение в молекулярном виде:
2КС1 + 2Н2О = Н2 + С12 + 2КОН
На катоде выделяется водород, на аноде хлор, в растворе образуется гидроксид калия.
В растворе содержалось 111,75 г хлорида калия.
Вычислим молярную массу хлорида калия:
М(КС1) = 39+35,5 = 74,5 г/моль
Вычислим количество вещества хлорида калия:

По уравнению реакции при электролизе 2 моль хлорида калия выделяется 1 моль хлора. Пусть при электролизе 1,5 моль хлорида калия выделяется х моль хлора. Составим пропорцию:


Выделится 0,75 моль хлора, v(C!2) = 0,75 моль. По уравнению реакции при выделении 1 моль хлора на аноде на катоде выделяется 1 моль водорода. Следовательно, если на аноде выделится 0,75 моль хлора, то на катоде выделится 0,75 моль водорода, v(H2) = 0,75 моль.
Вычислим объем хлора, выделившегося на аноде:
V(C12) = v(Cl2)-VM = 0,75 моль«22,4 л/моль = 16,8 л.
Объем водорода равен объему хлора:
По уравнению реакции при электролизе 2 моль хлорида калия образуется 2 моль гидроксида калия, значит, при электролизе 0,75 моль хлорида калия образуется 0,75 моль гидроксида калия. Вычислим молярную массу гидроксида калия:
М(КОН) = 39+16+1 — 56 г/моль.
Вычислим массу гидроксида калия:
m(KOH) = v(KOH>M(KOH) = 0,75 моль-56 г/моль = 42 г.
Ответ: на катоде выделилось 16,8 л водорода, на аноде выделилось 16,8 л хлора, в растворе образовалось 42 г гидроксида калия.
Задача 3. При электролизе раствора 19 г хлорида двухвалентного металла на аноде выделилось 8,96 л хлора. Определите, хлорид какого металла подвергли электролизу. Вычислите объем водорода, выделившегося на катоде.
Обозначим неизвестный металл М, формула его хлорида МС12. На аноде окисляются хлорид-ионы и выделяется хлор. В условии сказано, что на катоде выделяется водород, следовательно, происходит восстановление молекул воды:
2Н20 + 2е- = Н2 + 2ОH |1
Общее уравнение электролиза:
2Сl + 2Н2О = Н2 + 2ОН» + С12 (краткое ионное уравнение)
В растворе присутствуют также ионы М2+, которые при реакции не изменяются. Запишем полное ионное уравнение реакции:
2СГ + М2+ + 2Н2О = Н2 + М2+ + 2ОН- + С12
Перепишем уравнение реакции в молекулярном виде:
МС12 + 2Н2О — Н2 + М(ОН)2 + С12
Найдем количество вещества выделившегося на аноде хлора:
По уравнению реакции при электролизе 1 моль хлорида неизвестного металла выделяется 1 моль хлора. Если выделилось 0,4 моль хлора, то электролизу подвергли 0,4 моль хлорида металла. Вычислим молярную массу хлорида металла:
Молярная масса хлорида неизвестного металла 95 г/моль. На два атома хлора приходится 35,5»2 = 71 г/моль. Следовательно, молярная масса металла равна 95-71 = 24 г/моль. Этой молярной массе соответствует магний.
По уравнению реакции на 1 моль выделившегося на аноде хлора приходится 1 моль выделившегося на катоде водорода. В нашем случае на аноде выделилось 0,4 моль хлора, значит, на катоде выделилось 0,4 моль водорода. Вычислим объем водорода:
V(H2) = v(H2>VM = 0,4 моль«22,4 л/моль = 8,96 л.
Ответ: электролизу подвергли раствор хлорида магния; на катоде выделилось 8,96 л водорода.
*3адача 4. При электролизе 200 г раствора сульфата калия с концентрацией 15% на аноде выделилось 14,56 л кислорода. Вычислите концентрацию раствора по окончании электролиза.
В растворе сульфата калия и на катоде, и на аноде реагируют молекулы воды:
2Н20 + 2е’ = Н2 + 20Н- |2
2Н2О — 4е’ = 4Н+ + О2 ! 1
Сложим вместе оба уравнения:
6Н2О = 2Н2 + 4ОН» + 4Н+ + О2, или
6Н2О = 2Н2 + 4Н2О + О2, или
Фактически при электролизе раствора сульфата калия происходит электролиз воды.
Концентрация растворенного вещества в растворе определяется по формуле:
С=m(растворенного вещества) 
Чтобы найти концентрацию раствора сульфата калия по окончании электролиза, необходимо знать массу сульфата калия и массу раствора. Масса сульфата калия при реакции не изменяется. Вычислим массу сульфата калия в исходном растворе. Обозначим концентрацию исходного раствора Сь
m(K2S04) = C2 (K2S04 ) 

Масса раствора во время электролиза изменяется, так как часть воды превращается в водород и кислород. Вычислим количество вещества выделившегося кислорода:

По уравнению реакции из 2 моль воды образуется 1 моль кислорода. Пусть 0,65 моль кислорода выделяется при разложении х моль воды. Составим пропорцию:
Разложилось 1,3 моль воды, v(H2O) = 1,3 моль.
Вычислим молярную массу воды:
М(Н2О) =1-2+16=18 г/моль.
Вычислим массу разложившейся воды:
m(H2O) = v(H2O>M(H2O) = 1,3 моль* 18 г/моль = 23,4 г.
Масса раствора сульфата калия уменьшилась на 23,4 г и стала равна 200-23,4 = 176,6 г. Вычислим теперь концентрацию раствора сульфата калия по окончании электролиза:
С2 (K2 SO4 )=m(K2 SO4 ) 

Ответ: концентрация раствора по окончании электролиза равна 17%.
*3адача 5. 188,3 г смеси хлоридов натрия и калия растворили в воде и пропустили через полученный раствор электрический ток. При электролизе на катоде выделилось 33,6 л водорода. Вычислите состав смеси в процентах по массе.
После растворения смеси хлоридов калия и натрия в воде в растворе содержатся ионы К+, Na+ и Сl-. Ни ионы калия, ни ионы натрия не восстанавливаются на катоде, восстанавливаются молекулы воды. На аноде окисляются хлорид-ионы и выделяется хлор:
2Н2О + 2е’ = Н2 + 2ОН» ] 1
Общее уравнение электролиза:
2СГ + 2Н2О = Н2 + 2ОН» + С12 (краткое ионное уравнение)
Полные ионные уравнения реакций электролиза хлорида натрия и хлорида калия.
2К+ + 2Cl 

2Na+ + 2С1 

Перепишем уравнения в молекулярном виде:
2КС1 + 2Н20 = Н2 + С12 + 2КОН
2NaCl + 2Н2О = Н2 + С12 + 2NaOH
Обозначим количество вещества хлорида калия, содержащегося в смеси, х моль, а количество вещества хлорида натрия у моль. По уравнению реакции при электролизе 2 моль хлорида натрия или калия выделяется 1 моль водорода. Поэтому при электролизе х моль хлорида калия образуется х/2 или 0,5х моль водорода, а при электролизе у моль хлорида натрия 0,5у моль водорода. Найдем количество вещества водорода, выделившегося при электролизе смеси:
Составим уравнение: 0,5х + 0,5у =1,5
Вычислим молярные массы хлоридов калия и натрия:
М(КС1) = 39+35,5 = 74,5 г/моль
M(NaCl) = 23+35,5 = 58,5 г/моль
Масса х моль хлорида калия равна:
m(KCl) = v(KCl)-M(KCl) = х моль-74,5 г/моль = 74,5х г.
Масса у моль хлорида натрия равна:
m(KCl) = v(KCl)-M(KCl) = у моль-74,5 г/моль = 58,5у г.
Масса смеси равна 188,3 г, составим второе уравнение:
74,5х + 58,5у= 188,3
Итак, решаем систему из двух уравнений с двумя неизвестными:
Из первого уравнения выразим х:
Подставим это значение х во второе уравнение, получим:
74,5-(3-у) + 58,5у= 188,3
223,5-74,5у + 58,5у= 188,3
Найдем теперь значение х:
В смеси содержится 0,8 моль хлорида калия и 2,2 моль хлорида натрия.
Вычислим массу хлорида калия и хлорида натрия:
m(KCl) = v(KCl) 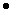
m(KCl) = v(KCl) 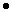
Вычислим массовую долю хлорида калия в смеси:
w(KCl)=m(KCl) 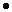
Вычислим массовую долю хлорида натрия:
w(NaCl) = 100% — w(KCl) = 68,35%
Ответ: в смеси содержится 31,65% хлорида калия и 68,35% хлорида натрия.
Электролиз
По этой ссылке вы найдёте полный курс лекций по математике:
Электролизом называется окислительно-восстанови-тельный процесс, протекающий на электродах при прохождении постоянного электрического тока через раствор или расплав электролита. Химические реакции протекают на электродах за счет электрической энергии. При электролизе катод является восстановителем, так как он отдает электроны, а анод — окислителем, так как он принимает электроны от анионов.
Например, если в раствор хлорида меди опустить электроды и пропустить постоянный электрический ток, то ионы меди будут двигаться к катоду, а ионы хлора — к аноду. На катоде происходит процесс восстановления: Cu2f + 2ё « Си, а на аноде — окисления: 2СГ — 2ё- С12. В итоге на катоде будет выделяться медь, а на аноде — хлор. Восстановительное и окислительное действие электрического тока во много раз сильнее химических восстановителей и окислителей.
Ни один химический окислитель не может отнять у иона фтора его электрон. Окислить ион фтора удалось лишь при электролизе расплава смеси безводного жидкого фтороводорода с фторидом калия. На угольном аноде выделяется фтор: 2F» — 2ё = F2, а на никелевом катоде — водород: 2Н+ + 2ё = Н2. Различают электролиз расплавов и растворов электролитов. Процессы в расплавленных электролитах — наи- более простой случай электролиза.
Так, в расплаве хлорида натрия содержатся ионы Na+ и С Г. При пропускании через него электрического тока ионы Na+ у катода присоединяют электроны и восстанавливаются до атомов натрия, ионы хлора СГу анода отдают электроны и окисляются до атомов хлора, которые затем образуют молекулы. Пример 1 Схема электролиза расплава NaCl расплав 2 процесс восстановления 1 процесс окисления электролиз 2NaCl -Г 2Na + CLf. Пример 2 Схема электролиза расплава СаВг2 1 процесс восстановления 1 процесс окисления электролиз СаВг2 Са + Вг2. Пример 3
Схема электролиза расплава КОН КОН К+ + ОН». расплав 4 процесс восстановления 1 процесс окисления электролиз — ионное уравнение электролиз — молекулярное урав- нение Если электролизу подвергается расплав, который содержит несколько различных катионов, то в этом случае последовательность восстановления определяется электродным потенциалом металла в данных условиях. В первую очередь восстанавливаются катионы металлов, обладающие большим значением электродного потенциала.
Более сложные процессы протекают при электролизе водных растворов электролитов, поскольку в этих процессах принимает участие вода. Рассмотрим электролиз концентрированного раствора хлорида натрия. В этом случае в растворе, кроме гидратированных ионов натрия и хлора, присутствуют молекулы воды и продукты ее диссоциации, которые участвуют в электродных реакциях. При прохождении тока через раствор к катоду будут двигаться катионы натрия и водород, а к аноду — хлорид и гидроксид-ионы. По этой причине реакции, протекающие на электродах, будут существенно отличаться от реакций, идущих в расплаве соли.
Возможно вам будут полезны данные страницы:
На катоде, вместо ионов натрия, будут восстанавливаться молекулы воды и ионы водорода, поскольку они обладают большей окислительной способностью с ионами натрия. На аноде происходит окисление хлорид-ионов (обладающих большей восстановительной способностью по сравнению с гидроксид-ионами). Пример 4 Схема электролиза раствора NaCl , расплав 1 процесс восстановления 1 процесс окисления электролиз электролиз 2NaCl + 2Н20 — Н2| + С12| + 2NaOH — молекулярное уравнение.
Последовательность, в которой происходит разряд ионов на катоде из растворов солей, определяется рядом стандартных электродных потенциалов, в котором металлы располагаются в ряд по нарастанию алгебраической величины их нормальных электродных потенциалов. Поясним, как образуется ряд стандартных электродных потенциалов. Погружение металла в раствор одноименной соли приводит к процессам перехода ионов металла с поверхности металла в раствор — растворение металла, или из раствора в металл — осаждение металла.
Вследствие этих процессов поверхность металла (электрода) приобретает положительный или отрицательный заряд, причем его величина и знак будут определяться природой металла, концентрацией соли в растворе и температурой. Гидратированные катионы и анионы, находящиеся в растворе, притягиваются заряженными поверхностями металлов, в результате чего на поверхности раздела металл-раствор образуется два слоя с противоположными зарядами — так называемый двойной электрический слой.
Разность потенциалов этого слоя носит название электродного потенциала. Непосредственно измерить величину потенциала отдельного электрода не представляется возможным. Поэтому электродные потенциалы измеряют путем сопоставления с потенциалом принятого для сравнения электрода. В качестве последнего обычно применяют стандартный водородный электрод, величину потенциала которого условно принимают за ноль. Этот электрод состоит из платиновой пластинки, покрытой платиновой чернью (электролитически осажденной платиной), которая погружена в 1 М раствор серной кислоты и омывается струей газообразного водорода под давлением 1 атм.
Если теперь пластинку любого металла, погруженную в раствор его соли, содержащий 1 моль ионов металла в 1000 г воды, соединить с водородным электродом с помощью так называемого «электролитического ключа», то получится гальванический элемент, электродвижущую силу которого (ЭДС) легко измерить. Эта ЭДС, измеренная при 25 °С, называется стандартным электродным Ряд стандартных электродных потенциалов металлов потенциалом данного металла.
Располагая металлы в порядке возрастания алгебраической величины их стандартных электродных потенциалов, получают ряд стандартных электродных потенциалов металлов.- Чем левее металл в ряду стандартных потенциалов, тем труднее его ион разряжается при электролизе. При этом возможны три случая: (TJ Катионы металлов, имеющих стандартный потенциал больший, чем у водорода (от Си2+ до Аи3+), прн электролизе практически полностью восстанавливаются на катоде.
(Т) Катионы металлов, имеющих малую величину стандартного электродного потенциала (от Li+ до А13+ включительно), не восстанавливаются на катоде, а вместо них восстанавливаются молекулы воды. [з] Катионы металлов, имеющих стандартный электродный потенциал меньший, чем у водорода, но больший, чем у алюминия (от А13+ до Н2), при электролизе на катоде восстанавливаются одновременно с молекулами воды. Если же водный раствор содержит катионы различных металлов, то при электролизе выделение их на катоде протекает в порядке уменьшения алгебраической величины стандартного электродного потенциала соответствующего металла.
Так, из смеси катионов Ag+, Cu2+, Zn2+ сначала будут восстанавливаться катионы серебра, затем катионы меди и последними — катионы цинка. Характер реакций, протекающих на аноде, зависит как от присутствия молекул воды, так и от вещества, из которого сделан анод. Аноды бывают нерастворимые и растворимые. Первые изготавливаются из угля, графита, платины (в процессе электролиза они не переходят в раствор в виде ионов); вторые — из меди, серебра, цинка, кадмия, никеля и др. металлов (в процессе электролиза переходят в раствор в виде ионов, т. е. разрушаются).
На нерастворимом аноде в процессе электролиза происходит окисление анионов или молекул воды. При этом анионы бескислородных кислот и их солей (СГ, Br», I», S2″) окисляются у анода. При электролизе водных растворов щелочей кислоро-досодержащих кислот и их солей (S042
), а также фторидов на аноде происходит электрохимическое окисление воды с выделением кислорода. Рассмотрим возможные случаи электролиза раствора солей на угольных электродах (электроды не участвуют в окислительно-восстановительных реакциях). Электролиз раствора соли, образованной активным металлом, стоящим в ряду напряжений до алюминия и кислотным остатком кислородосодержащей кислоты сводится к электролизу воды.
Пример 5 Схема электролиза водного раствора MgS04 MgS04 т± Mg2+ + SO2″, раствор электролиз Учитывая, что 4Н+ + 40Н» — 4Н20, электролиз 2Н20 — 2H2t+02|. Электролиз раствора соли, образованной малоактивным металлом, стоящим в ряду напряжений после водорода, и кислотным остатком кислородосодержащей кислоты. В данном случае при электролизе получается металл, кислород, а в катодно-анодном пространстве образуется соответствующая кислота. Пример 6 Схема электролиза водного раствора CuS04 CuS04 Cu2+ + SO2″, процесс восстановления 1 процесс окисления K(-): Cu2+ + 2ё Си0 электролиз электролиз 2CuS04 + 2Н20 — 2Cu + 021 + 2H2S04.
Электролиз раствора соли, образованной активным металлом (до А1) и кислотным остатком галогено-водородной кислоты. При электролизе получается водород, галоген, в катодно-анодном пространстве — щелочь. Пример 7 Схема электролиза водного раствора СаС12 СаС12 Са2+ + 2СГ, раствор НОН Н+ + ОН
. 1 процесс восстановления 1 процесс окисления электролиз , электролиз Электролиз раствора соли, образованный малоактивным металлом и кислотным остатком галоге-новодородной кислоты.
При электролизе получается металл и галоген. Пример 8 Схема электролиза водного раствора , раствор 1 процесс восстановления А(+): 2С1 — 2ё С12 1 процесс окисления лектролиз электролиз Если соль образована металлом, стоящим в ряду напряжения от алюминия до водорода и в процессе восстановления принимает участие вода, то процесс электролиза идет в зависимости от концентрации раствора соли. Чем менее концентрированный раствор, тем менее интенсивно восстанавливается металл. P^J Пример 9 Схема электролиза водного раствора Ni(N03)2 раствор 1 процесс окисления электролиз ‘2 2 1 1 ‘ электролиз P^l Пример 10 I
Схема элек электролиза водного раствора NaOH NaOH Na+ 4- ОН», раствор НОН Н+ 4- ОН». > 1 процесс восстановления / электролиз электролиз 2Н20 -V 2H?t + 0„t • 2 процесс восстановления 1 процесс окисления Пример 11 Схема электролиза водного раствора HgSC^ H2S04 2Н* + so;-, раствор НОН Н+ + ОН». nsr 2 процесс восстановления 1 процесс окисления электролиз электролиз 2На0 — 2H2t+02t-Растворимый анод при электролизе сам подвергается окислению (растворению), т. е. посылает электроны во внешнюю цепь.
Так, при электролизе раствора сульфата никеля с никелевым анодом процесс сводится к выделению никеля на катоде и постепенному растворению анода. Количество сульфата никеля в растворе остается неизменным. Пример 12 Схема электролиза водного раствора NiS04 с растворимым анодом раствор Количественно процесс электролиза описывается законами Фарадея: |Т) Количество вещества, восстановленного на катоде или окисленного на аноде, пропорционально количеству прошедшего через раствор или расплав электричества: m-kM^Q, где т — масса окисленного или восстановленного вещества; его молярная масса эквивалента;.
Q — количество электричества, прошедшего через электролит; к — коэффициент пропорциональности. [2] Количество окисляющихся или восстанавливающихся на электродах веществ при пропускании одного и того же количества электричества пропорциональны их молярным массам эквивалентов. Оба закона Фарадея можно выразить общей формулой: где F — число Фарадея. Учитывая, что количество электричества Q равно произведению силы тока J в амперах на время т в секундах, формулу можно написать так:
Величина Е называется электрохимическим эквивалентом вещества и характеризует собой массу вещества, которое восстанавливается на катоде или окисляется на аноде при прохождении через электролит одного кулона электричества. Молярная масса эквивалента связана с электрохимическим эквивалентом отношением: — EF.
Пример 13 Вычислите объем кислорода, выделившегося на угольном аноде при пропускании через разбавленный раствор серной кислоты тока силой 5 А в течение часа.
Дано: Найти: У(02) Решение: 1) Уравнение электролиза: электролиз 2) Находим количество электричества: ? = /• г; Q = 5 • 3600 = 18 ООО Кл. 3) Определим массу кислорода, выделившегося на аноде: 4) Найдем, какой объем при н. у. займет 1,492 г кислорода. Для этого сначала найдем количество вещества: 1,492 Y(Oz) — 32 — 0,047 моль. Откуда V(02) = 0,047 • 22,4 = 1,044 л. Ответ: V(02) = 1,044 л. Пример 14 Рассчитайте время, необходимое для полного выделения хлора, содержащегося в 2 л 0,5 Н раствора хлорида калия при электролизе этого раствора током силой 5 А. Дано: V(C\2) — 2 л СН(КС1) = 0,5 1=5 А
Найти: Решение: Определяем, что в 2 л 0,5 Н раствора хлорида калия содержится: 2 • 0,5 e 1 моль • экв. соли, для разложения которой требуется 96 500 Кл. Исходя из этого: Q 96 500 т = —, т = ——— = 321,8 мин = 5,3 ч. • I 5 • 1 Ответ: т= 5,3 час. Пример 15 Между какими из следующих попарно взятых веществ, формулы которых даны ниже (электролит берется в виде водного раствора), будет протекать реакция замещения: а) А1 + Cu(N03)2; б) Zn + MgS04.
Напишите уравнения реакции в ионной форме. Решение: В рассматриваемых реакциях замещения свободный металл будет вытеснять металл из соли в раствор в том случае, если он обладает большей восстановительной способностью по сравнению с металлом, образующим соль. Сравнивая пары металлов— А1 и Си; Zn и Mg, мы видим из их положения в электрохимическом ряду напряжений, что реакция замещения возможна только в первом случае и она отразится следующим уравнением: 2А1° + 3Cu2f — 3Cu° + 2AI8*. Применение электролиза расплавов и растворов огромно.
Такие ценные металлы, как алюминий, натрий, цинк, олово, свинец, кадмий, серебро, золото, получают исключительно путем электролиза. В производстве никеля, магния, меди, белой жести электрохимическая продукция составляет 80-90 %. Хлор и его кислородные соединения в промышленности получают также электрохимически. Все шире развиваются электрохимические методы получения органических соединений. Электролиз начинают применять для обессоливания воды, для укрепления грунтов за счет удаления воды (электроосмос).
Его развитие тесно связано с проблемой получения чистых и особо чистых материалов. Ни одна отрасль машиностроения не может обойтись без электрохимических методов обработки поверхности металлических изделий. Электрохимическим методом наносят металлические покрытия, которые предохраняют металл от ржавчины. Электролиз используют для получения точных копий с различных предметов — гальванопластика. Предмет, с которого хотят получить копию, покрывают воском и получают матрицу.
| Поверхность восковой матрицы покрывают |
тонким слоем графита, делая ее проводящей электрический ток. Графитовый катод опускают в ванну с раствором сульфата меди, анодом служит медь. При электролизе медный анод растворяется, а на катоде осаждается медь. С помощью гальванопластики изготавливаются клише для печати матрицы грампластинок, металлизируют различные предметы. Электролиз используют для очистки металлов от примесей. Рафинирование (очистка) меди основано на анодном растворении металла.
В больших ваннах подвешивают ряд пластин из черновой меди, а между ними — тонкие пластинки чистой меди, заливают электролит и пропускают ток. Анод — черновая медь — растворяется, а на пластинках из чистой меди, которые служат катодом, нарастает слой очищенной меди. Электролитическая медь содержит 99,97 % чистой меди. Вопросы и задачи для самостоятельного решения 1. Укажите отличие проводников первого рода от проводников второго рода.
2. Укажите, от каких факторов зависит последователь- ность расположения металлов по величинам их электродных потенциалов. 3. Объясните, почему электродные потенциалы металлов имеют положительный или отрицательный знак. 4 Объясните, почему последовательность изменения активности металлов в ряду стандартных электродных потенциалов не совпадает с последовательностью изменения активности металлов в группах и периодах периодической системы.
5. Цинковые пластинки опущены в растворы нитратов калия, кальция, никеля и свинца. В каких случаях будут протекать химические реакции? Напишите соответствующие уравнения процессов в молекулярной и ионно-молекулярной формах. 6. Какая масса технического цинка, содержащего 2 % примесей, требуется для вытеснения из раствора нитрата меди (II) 6,35 г меди? Ответ: 6,67 г. 7. Какие процессы, протекающие на электродах, объединяются общим названием * электролиз*?
8. Чем вызвана необходимость пространственного разделения процессов, протекающих на электродах? 9. Объясните, чем определяется последовательность восстановления катионов на катоде при электролизе растворов электролитов? 10. Какие факторы предопределяют выбор материала для электродов при проведении процесса электролиза? 11. Какими показателями оценивается эффективность процессов электролиза?
12. При получении каких веществ в народном хозяйстве используется электролиз? 13. Составьте схемы электролиза водного раствора нитрата цинка, если: а) анод угольный; б) анод цинковый. 14. Какие химические процессы происходят у катода и у анода при электролизе раствора иодида натрия. 15. Чем отличается электролиз расплава едкого натра «От электролиза его раствора? Какие вещества и в каком количестве выделяются при электролизе раствора едкого натра, если через раствор пропускают ток силой 10 А в течение 10 ч 44 мин? Ответ: 44,8 л Н2 и 22,4 л 02 (н. у.).
16. Какое количество продуктов будет получено при электролизе расплава едкого натра током силой 0,6 А в течение Зч? Ответ: 1,54 г Na; 0,38 л 02 (н. у.). 17. Будет ли меняться в ходе электролиза водного раствора гидроксида калия: масса гидроксида калия в растворе; концентрация раствора? Почему? 18. Какое количество электричества необходимо пропустить через раствор поваренной соли для получения 1 г едкого натра? Ответ: 2412,5 Кл. 19. С каким полюсом батареи — положительным или отрицательным — должна быть соединена металлическая деталь при ее хромировании?
20. Определите объем водорода, выделившегося на катоде (н. у.) при электролизе водного раствора серной кислоты, если известно, что при этом вступило в реакцию 1,505′ 1024 электронов. Ответ: 28 л. 21. При прохождении через раствор соли трехвалентного металла тока силой ЗА в течение 15 мин на катоде выделилось 1,071 г металла. Определите атомную массу металла. Ответ: 114,9. 22.
При электролизе раствора нитрата хрома (III) током силой 1 А масса хромового катода возросла на 10 г. Какое количество электричества было пропущено через раствор и в течение какого времени? Ответ: 55700 Кл; 15 ч 28 мин. 23. Через раствор нитрата никеля (II) в течение 2 ч 27 мин пропускали ток силой 3,5 А. Определите, на сколько граммов за это время уменьшилась масса никелевого анода. Ответ: 9,4 г. 24. При электролизе током силой 2 А в течение 40 мин на катоде выделилось 4,542 г некоторого металла. Определите молярную массу эквивалента этого металла. Ответ: 91,3 г.
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.
http://school6.tgl.ru/old/ximiya/sait/tema/elek.html
http://natalibrilenova.ru/elektroliz/