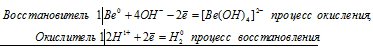Свойства s-элементов на примере бериллия, кальция и магния
Задание 329
Гидроксид какого из s-элементов проявляет амфотерные свойства? Составьте молекулярные и ионно-молекулярные уравнения реакций этого гидроксида: а) с кислотой; б) со щелочью.
Решение:
Гидроксид бериллия Ве(ОН)2 проявляет амфотерные свойства в кислой и щелочной средах он образует комплексы:
а) реакция с кислотами:
б) реакция со щёлочью:
Be(OH)2 + 2NaOH = Na2[Be(OH)4] (молекулярная форма);
Be(OH)2 + 2OH- = [Be(OH)4] 2- (ионно-молекулярная форма)
Задание 330
При пропускании диоксида углерода через известковую воду [раствор Са(ОН)2] образуется осадок, который при дальнейшем пропускании СО2 растворяется. Дайте объяснение этому явлению. Составьте уравнения реакций.
Решение:
При пропускании диоксида углерода через известковую воду [раствор Са(ОН)2] образуется осадок CaCO3:
При дальнейшем пропускании СО2 осадок карбоната кальция растворяется, так как образуется растворимый гидрокарбонат кальция:
Гидрокарбонат кальция существует только в водном растворе в виде ионов Са 2+ и НСО3 — :
Задание 331
Составьте электронные и молекулярные уравнения реакций: а) бериллия с раствором щелочи; б) магния с концентрированной серной кислотой, учитывая, что окислитель приобретает низшую степень окисления.
Решение:
а) бериллий реагирует со щелочами с образованием комплексного иона [Be(OH)4] 2 -:
Be 0 + 2H + + 4OH — = [Be(OH)4] 2- + H2 0
После приведения уравнения получим:
б) Взаимодействие магния с концентрированной серной кислотой сопровождается образованием сульфата магния и сульфида магния:
4Mg 0 + 8H + + SO4 2- = 4Mg 2+ +S 2- + 4H2O
Задание 332
При сплавлении оксид бериллия взаимодействует с диоксидом кремния и с оксидом натрия. Напишите уравнения соответствующих реакций. О каких свойствах ВеО говорят эти реакции?
Решение:
При сплавлении оксид бериллия взаимодействует с оксидом кремния и оксидом натрия:
Эти реакции говорят о том, что оксид бериллия проявляет амфотерные свойства, реагируя с кислотным оксидом SiO2 и основным оксидом Na2O.
Бериллий: способы получения и химические свойства
Бериллий Be — это cветло-серый, легкий, хрупкий металл. На воздухе покрывается оксидной пленкой. Восстановитель.
Относительная молекулярная масса Mr = 9,012; относительная плотность для твердого и жидкого состояния d = 1,85; tпл = 1287º C; tкип = 2507º C.
Способ получения
1. В результате электролиза расплава хлорида бериллия образуются бериллий и хлор :
2. Расплав фторида бериллия подвергают электролизу , в результате чего на выходе образуется бериллий и фтор:
3. Оксид бериллия легко восстанавливается магнием при 700 — 800º С, образуя бериллий и оксид магния:
BeO + Mg = MgO + Be
4. Фторид бериллия также легко восстанавливается магнием при 700 — 750º С с образованием бериллия и фторида магния:
BeF2 + Mg = Be + MgF2
Качественная реакция
Качественная реакция на бериллий — окрашивание пламени горелки в коричнево — красный цвет.
Химические свойства
1. Бериллий — сильный восстановитель . Поэтому он реагирует почти со всеми неметаллами :
1.1. Бериллий взаимодействует с азотом при 700 — 900º С образуя нитрид бериллия:
1.2. Бериллий сгорает в кислороде (воздухе) при 900º С с образованием оксида бериллия:
2Be + O2 = 2BeO
1.3. Бериллий активно реагирует при комнатной температуре с фтором (комнатная температура) , хлором (250º С), бромом (480º С) и йодом (480º С) . При этом образуются фторид бериллия, хлорид бериллия, бромид бериллия, йодид бериллия :
Be + Br2 = BeBr2
1.4. С серой бериллий реагирует при температуре 1150º C с образованием сульфида бериллия:
Be + S = BeS
1.5. С углеродом бериллий реагирует при 1700 — 1900º С и вакууме, образуя карбид бериллия:
2Be + C = Be2C
2. Бериллий активно взаимодействует со сложными веществами:
2.1. Бериллий при кипении реагирует с водой . Взаимодействие бериллия с водой приводит к образованию гидроксида бериллия и газа водорода:
2.2. Бериллий взаимодействует с кислотами:
2.2.1. Бериллий реагирует с разбавленной соляной кислотой, при этом образуются хлорид бериллия и водород :
Be + 2HCl = BeCl2 + H2 ↑
2.2.2. Реагируя с разбавленной и горячей азотной кислотой бериллий образует нитрат бериллия, газ оксид азота (II) и воду:
2.2.3. В результате реакции концентрированной фтороводородной кислоты и бериллия образуется осадок тетрафторобериллат водорода и газ водород:
2.3. Бериллий может взаимодействовать с основаниями:
2.3.1. Бериллий взаимодействует с гидроксидом натрия в расплаве при температуре 400 — 500º С, при этом образуется бериллат натрия и водород:
Бериллий взаимодействует с гидроксидом натрия в растворе , при этом образуется тетрагидроксобериллат натрия и водород:
2.4. Бериллий вступает в реакцию с газом аммиаком при 500 — 700º С. В результате данной реакции образуется нитрид бериллия и водород:
2.5. Бериллий может вступать в реакцию с оксидами :
В результате взаимодействия бериллия и оксида магния при температуре 1075º С образуется оксид бериллия и магний:
Be + MgO = BeO + Mg
3. Бериллий взаимодействует с органическими веществами :
Бериллий может вступать в реакцию с ацетиленом при 400 — 450º С, образуя карбид бериллия и водород:
HTTP Status 400 – Bad Request
Type Exception Report
Message Invalid character found in the request target [/ru/?s=H2O+++NaOH+++Be+=+H2+++Na2[Be(OH)4] ]. The valid characters are defined in RFC 7230 and RFC 3986
Description The server cannot or will not process the request due to something that is perceived to be a client error (e.g., malformed request syntax, invalid request message framing, or deceptive request routing).
Note The full stack trace of the root cause is available in the server logs.
http://chemege.ru/berillij/
http://chemequations.com/ru/?s=H2O+++NaOH+++Be+=+H2+++Na2[Be(OH)4]