Реакция получения полиэтилена
Реакция получения полиэтилена – это процесс, в котором происходит расщепление π-связи алкенов и образование линейной макромолекулы. Разрыв двойной связи олефинов обусловлен жестким влиянием среды, которое выражается в увеличении значений давления и температуры по сравнению с величинами, характерными для нормальных условий.
Тип реакции получения полиэтилена из этилена – классическая полимеризация непредельных углеводородов, свойственная всем алкенам.
Разновидности синтеза
Существует два основных варианта проведения реакции синтеза полиэтилена. Они отличаются условиями и аппаратным исполнением. В обеих ситуациях процесс проходит при повышенном давлении, температуре, в присутствии катализаторов.
Получение ПЭВД
Полиэтилен получают из этилена в результате реакции, при которой мономер переходит в активное состояние.
При воздействии температуры, значения которой достигают 320 °С, давления, повышенного до 320 мПа, инициирование вызывают образующиеся из пероксидных соединений радикалы. Полиэтилен, реакция полимеризации которого идет по радикальному механизму, имеет низкую плотность, называется продуктом высокого давления, обозначается в международном сообществе аббревиатурой LDPE.
Маленькая плотность упаковки макромолекул обусловлена присутствием разветвлений, как это отображено в уравнении реакции получения полиэтилена.
Процесс проводят в автоклавах при идеальном перемешивании или трубчатых реакторах при идеальном вытеснении продуктов.
Получение ПЭНД
При увеличении давления до 5 мПа образование полиэтилена из этилена — результат реакции без участия радикалов. Активацию мономеров обеспечивают комплексные катализаторы.
Температура до 95 °С позволяет проводить процесс в суспензии, каталитическое действие выполняют сложные неорганические соединения титана.
Реакция полимеризации полиэтилена при температуре до 120 °С проходит с участием оксидов хрома, нанесенных на силикагель.
Комплексные соединения хрома, зафиксированные на силикагеле, позволяют проводить процесс в газовой фазе при температуре, не достигающей 100 °С.
Если полиэтилен получают, используя реакцию с катализаторами, продукт представляет собой линейную макромолекулу без разветвлений, имеет большую плотность, в международной литературе обозначается аббревиатурой HDPE.
Реакция синтеза полиэтилена с комплексными катализаторами приводит к получению продукта, который можно перерабатывать из б/у состояния.
Полимер из вторичного сырья
Полиэтиленовые отходы утилизируют по технологии, включающей очистку вторичного сырья, измельчение, образование агломератов, гранул, последующую экструзию. Графическое уравнение реакции полиэтилена б/у идентично схеме получения ПЭНД потому, что повторная полимеризация не осуществляется.
Реакция получения полиэтилена б/у, по существу, является физическим процессом, при котором происходит изменения агрегатного состояния.
Реакции полимеризации
Синтетические полимеры (произведенные искусственным путем) химическая промышленность получает при помощи реакций полимеризации и поликонденсации.
В основе реакции полимеризации лежит процесс соединения (при помощи ковалентных связей) друг с другом мономеров (молекул низкомолекулярного соединения), которые и формируют высокомолекулярное соединение (синтетический полимер).
В ходе процесса полимеризации происходит раскрытие двойных связей в молекулах непредельных углеводородов, которые затем соединяются друг с другом в одну макромолекулу гигантских размеров. При разрыве двойной связи высвобождается атом с высокой реакционной активностью, называемый радикалом, у которого имеется непарный электрон. После этого, радикал соединяется с другим радикалом (при этом оба они получают парные электроны), давая тем самым старт образованию полимерной цепи.
Полиэтилен
Рассмотреть процесс полимеризации удобнее всего на примере полиэтилена, являющегося самым простым синтетическим полимером.
На первом этапе выполняется реакция дегидрирования, когда при высокой температуре в присутствии металлического катализатора этан превращается в этилен (от молекулы этана отщепляется два атома водорода, в результате чего формируется двойная связь):
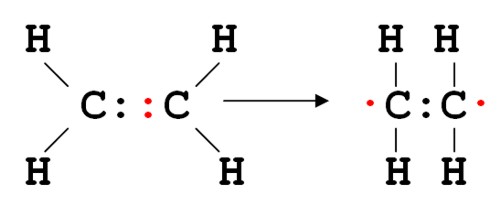
Образовавшийся этилен является мономером, который в дальнейшем будет использован для построения полимера (полиэтилена). Для этого этилен в присутствии катализатора подвергается высокому нагреву без доступа воздуха, что приводит к разрыву двойной углеродной связи, с образованием двух радикалов (на рисунке изображены красным цветом):
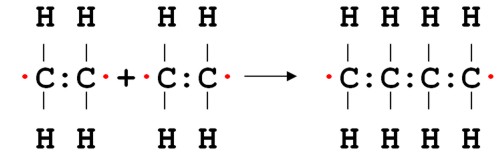
Образовашиеся радикалы тут же начинают «поиск» еще одного электрона, чтобы восстановить разорвавшуюся связь, что приводит к соединению двух радикалов друг с другом с образованием ковалентной связи. Данный процесс идет с обеих концов молекулы, что приводит к росту цепи (молекулярная масса молекулы полиэтилена достигает 10 000 — 1 000 000 г/моль):
Виды полиэтилена, которые можно получить путем реакции полимеризации:
- ПЭВД (полиэтилен высокого давления) или ПЭНП (полиэтилен низкой плотности), молекулярная масса 10 000 — 45 000. Состоит из сложной сети разветвленных полимерных нитей, поэтому, не упакован так плотно, как линейный полимер, являясь мягким и гибким. Основная область применения: упаковочный материал, обладающий высокой химической стойкостью.
- ПЭНД (полиэтилен низкого давления) или ПЭВП (полиэтилен высокой плотности), молекулярная масса 70 000 — 400 000. Состоит из линейных цепей, которые очень тесно упакованы, поэтому, обладает более высокой твердостью и прочностью. Основная область применения: изготовление детских игрушек, различных технических изделий, шлангов, труб и проч.
- ПЭПС (полиэтилен с поперечными связями). Состоит из линейных нитей, состоящих из мономеров, которые соединены друг с другом, что придает материалу высокую прочность. Открывая пластиковую бутылку Кока-Колы, будьте уверены, что крышечка, которой закрыта бутылка, сделана из ПЭПС.
Полипропилен
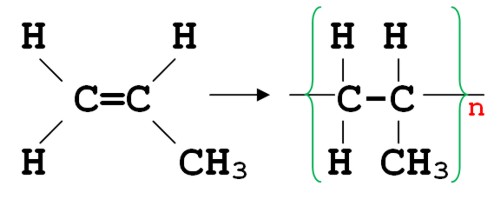
В структурной формуле пропилена один атом водорода замещен метиловой группой. Поскольку молекула пропилена имеет двойную связь, она также может участвовать в реакциях полимеризации (по аналогии с этиленом), образуя полипропилен.
Коэффициент n указывает число мономерных звеньев, из которых образована макромолекула. Говорят, что n выражает степень полимеризации.
В полипропилене CH3 является функциональной группой. Меняя условия полимеризации, можно создавать молекулы с функциональными группами, которые будут располагаться по-разному(с одной стороны молекулы; по обе ее стороны; в случайном порядке), получая, таким образом, молекулы пропилена с различными свойствами. Свойства полипропилена настолько сильно зависят от расположения в его молекуле метиловой группы, что из данного полимера получаются самые разные изделия, используемые для внутренней и внешней отделки помещений, изготовления корпусов для аккумуляторных батарей, бутылок, канатов и проч.
Поливинилхлорид
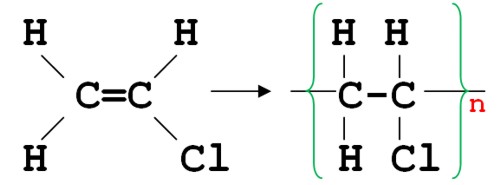
В структурной формуле винилхлорида один из атомов водорода заменен атомом хлора. Из винилхлорида путем реакции полимеризации получают поливинилхлорид (ПВХ):
ПВХ является очень прочным полимером, нашедшим широкое применение при изготовлении линолеума, игрушек, садовых шлангов, различных труб.
Полистирол
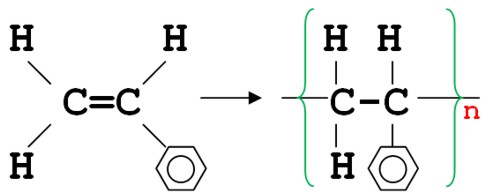
В молекуле стирола один атом водорода заменен бензольным кольцом. Из стирола при помощи реакции полимеризации получают полистирол (бесцветную твердую пластмассу с хорошими диэлектрическими свойствами):
Основное применение полистирола: изготовление посуды, пуговиц, упаковочных и электроизоляционных материалов. Полистирол трудно поддается рециркуляции, поэтому, «зеленые» активно выступают против его применения.
Политетрафторэтилен
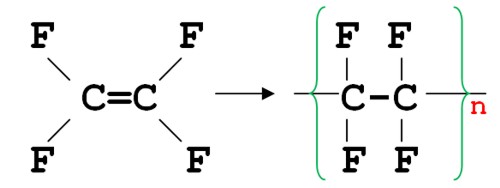
В молекуле тетрафторэтилена вместо атомов водорода присутствуют атомы фтора. При помощи реакции полимеризации из тетрафторэтилена получают политетрафторэтилен (тефлон или фторопласт):
Политетрафторэтилен обладает высокой стойкостью к щелочным и кислым средам, высокой жаропрочностью и очень гладкой поверхностью. Основное применение: изготовление подшипников, в качестве антипригарного покрытия сковородок и кастрюль.
Некоторые другие синтетические полимеры, получаемые при помощи полимеризации:
- Акрилонитрил → Полиакрилонитрил: парики, пряжа, ковры.
- Винилацетат → Поливинилацетат: текстильные покрытия, жевательная резинка, краска, латекс, клеющие средства.
- Метилметакрилат → Полиметилметакрилат: органическое стекло, контактные линзы.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Этилен в полиэтилен уравнение реакции
• Широкий ассортимент и выгодные цены на анкер клиновой на https://dominant-krep.ru/catalog/. .
Архив статей > Химия > Опыты без взрывов > Этилен из полиэтилена
Этилен из полиэтилена
А. Н. Шугаев, учитель химии, п. Октябрьский Калужской области
Химия и Жизнь №10, 1987 г., с. 113
Чтобы продемонстрировать на уроке химии свойства этилена, его надо для начала получить. Обычно это делают, восстанавливая спирт. Но есть более простой путь, позволяющий к тому же использовать отходы из полиэтилена.
Возьмите пакеты, пленку и другие полиэтиленовые изделия, измельчите, засыпьте в колбу, затем залейте содержимое концентрированной серной кислотой (осторожно! работать в перчатках!) так, чтобы ее уровень был немного выше слоя полиэтилена, и нагревайте на огне. Бурно выделяющийся этилен надо отводить по стеклянной трубке.
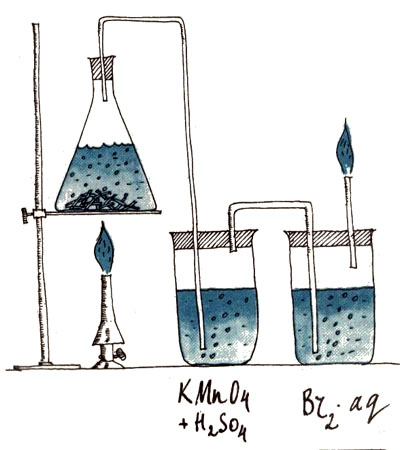
Можно собрать небольшую установку (см. рис.), с помощью которой легко демонстрировать свойства этилена. Для этого образующийся газ надо отводить в химические стаканы с растворами перманганата калия, подкисленного серной кислотой, и бромной водой. В обоих случаях растворы будут обесцвечиваться, поскольку перман-ганат калия окисляет этилен до этиленгликоля, а бром присоединяется по двойной связи. Из последнего стаканчика можно сделать отвод и поджечь выходящий газ, чтобы не было сомнений в его органической природе.
Эта методика может пригодиться учителям химии и для практических работ в 10-м классе, и для занятий химического кружка.
http://prosto-o-slognom.ru/chimia/39_reaktsii_polimerizatsii.html
http://www.nts-lib.ru/Online/opt/etilen.html