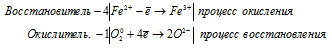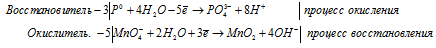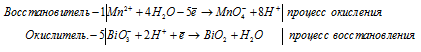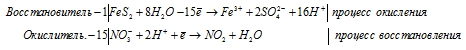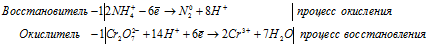Запись окислительно-восстановительного процесса в молекулярной и ионной форме
4Fe 2+ + O2 0 = 4Fe 3+ + 2O 2- .
б) P + KMnO4 + H2O ⇒ KH2HO4 + K2HO4
Уравнения полуреакций:
3P 0 + 5MnO4 — + 22H2O = 3PO4 3- + 5MnO2 + 20OH — + 24H + .
После приведения членов в обеих частях равенства получим ионно-молекулярную форму:
Молекулярная форма процесса с учётом того, что продуктами являются KH2HO4 и K2HO4:
Подставив коэффициент 2 к K2HO4 чтобы уравнять атомы калия и водорода, получим:
в) Mn(NO3)2 + NaBiO3 + HNO3 ⇒ HMnO4 +
Уравнения полуреакций:
Напишем молекулярную форму реакции с учётом данных задачи, получим:
Добавим в левую часть равенства одну молекулу HNO3 для уравнивания, получим окончательную молекулярную форму процесса:
Mn 2+ + 5NO3 — + 5Na + + 5BiO3 — + 3H + = MnO4 — + H + + 5BiO2 + 5Na + + 5NO3 — + H2O
Mn 2+ + 5BiO 3 — + 3H + = MnO 4 — + H + + 5BiO + H2O.
г) FeS2 + HNO3(конц.) ⇒ H2SO4 +
Уравнения полуреакций:
Приведём члены в обеих частях равенства, получим:
Напишем молекулярную форму реакции с учётом данных задачи, получим:
Для полного уравнивания добавим в левую часть равенства 3 моля HNO3, получим:
Приведём члены в обеих частях равенства, получим:
Для уравнивания водорода отнимем 6 ионов Н + и 3 молекулы Н2О, подставим 3 иона О 2- к 2 ионам Cr 3+ , получим:
Полное ионно-молекулярное уравнение, оно же будет и сокращенным ионным уравнением:
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6dfb00068ec9c867 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
FeS2 + O2
FeS2 + O2 ? Fe2O3 + SO2 FeII – 1e– = FeIII 2S–I – 10e– = 2SIV O2 + 4e– = 2O–II 4FeS2 + 11O2 = 2Fe2O3 + 8SO2. Подбор коэффициентов в уравнениях ОВР Метод электронного баланса. 4. –11e–. +4e–. 11.
Слайд 21 из презентации «Типы химических реакций»
Размеры: 720 х 540 пикселей, формат: .jpg. Чтобы бесплатно скачать слайд для использования на уроке, щёлкните на изображении правой кнопкой мышки и нажмите «Сохранить изображение как. ». Скачать всю презентацию «Типы химических реакций.ppt» можно в zip-архиве размером 1415 КБ.
Реакции
«Закон сохранения массы веществ Ломоносова» — Алгоритм составления уравнений химических реакций. Назовите признак химической реакции. Формулировка закона сохранения массы веществ. Элементы. Решаем задачи по уравнениям. Михаил Васильевич Ломоносов. Основные понятия. Составление уравнений химических реакций. Какое явление представлено в фильме. Что показывает химическое уравнение.
«Уравнение окислительно-восстановительной реакции» — Укажите окислительно- восстановительные реакции. Окислительно-восстановительные реакции в природе и жизни человека. Уравнения окислительно- восстановительных реакций. Окислитель. Фотосинтез. Опусти меня в раствор, в медный купорос. Оптимальный вариант. Уравнение. Как по уравнению можно определить окислительно- восстановительную реакцию.
«Энергия химической реакции» — Следствие из закона Гесса. Связь. Влияние катализатора на равновесие химической реакции. Энергия Гиббса. Энтальпии образования простых веществ равны нулю. Единицы измерения. Состояние равновесия. NO, NO2. Теплота. Количество теплоты, которое выделяется или поглощается. Факторы неизолированных систем.
«Химические реакции» — Кипячение воды в чайнике. Самостоятельная работа. Лабораторный опыт. Актуализация знаний. Проверка. Реакция разложения. Кислотные дожди. Разминка. Вопросов полон мир. Брожение глюкозы в дрожжевом тесте. Основные типы химических реакций. Значение реакций соединения и разложения.
«Классификация химических реакций» — Разложение. Процесс изменения веществ. Химия. Гомогенные реакции. Классификация химических реакций. Решетовская средняя общеобразовательная школа. Экзотермические реакции. Реакции соединения. Реакции замещения. Характеристика химической реакции. Реакция разложения. Реакции обмена. Каталитические реакции.
«Типы химических реакций» — Реакция, протекающая между простыми и сложными веществами, при которой атомы простого вещества замещают атомы одного из элементов в сложном веществе, называется реакцией замещения. Все реакции сопровождаются тепловыми эффектами. Источники. Обратимые реакции -химические реакции, протекающие одновременно в двух противоположных направлениях (прямом и обратном) Например: 3H2 + N2 ? 2NH3 Лабораторная работа.
http://gomolog.ru/reshebniki/9-klass/eremin-2019/26/10.html
http://900igr.net/prezentacija/khimija/tipy-khimicheskikh-reaktsij-140473/fes2-o2-21.html