Йодид фосфора III
| Йодид фосфора III | |||
|---|---|---|---|
| |||
| Систематическое наименование | Йодид фосфора | ||
| Традиционные названия | Трийодид фосфора, йодистый фосфор | ||
| Хим. формула | PI3 | ||
| Состояние | ярко-красные кристаллы | ||
| Молярная масса | 411,69 г/моль | ||
| Плотность | 4,18 г/см³ | ||
| Температура | |||
| • плавления | 61,0 °C | ||
| Энтальпия | |||
| • образования | -46,0 кДж/моль | ||
| Рег. номер CAS | 13455-01-1 | ||
| PubChem | 83485 | ||
| Рег. номер EINECS | 236-647-2 | ||
| SMILES | |||
| Номер ООН | 3260 | ||
| ChemSpider | 75323 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
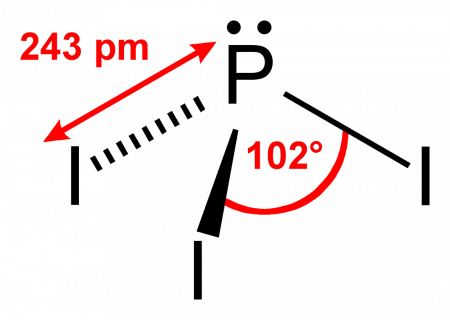
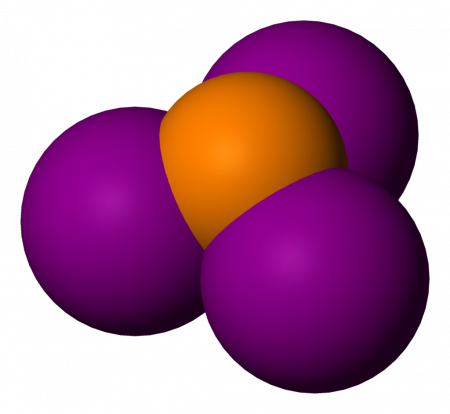
Йодид фосфора III — бинарное неорганическое соединение йода и фосфора с формулой PI3, ярко-красные кристаллы, реагируют с водой.
Содержание
- 1 Получение
- 2 Физические свойства
- 3 Химические свойства
- 4 Применение
Получение
- Иодирование раствора белого фосфора в сероуглероде:
2 P + 3 I2 →46oC 2 PI3
Физические свойства
Йодид фосфора III образует ярко-красные кристаллы гексагональной сингонии, пространственная группа P 63, параметры ячейки a = 0,711 нм, c = 0,742 нм, Z = 2.
Йод нагрели с избытком фосфора?
Химия | 10 — 11 классы
Йод нагрели с избытком фосфора.
Продукт реакции обработали небольшим количеством воды при нагревании при этом выделился бесцветный газ.
Он взаимодействует с нитратом серебра.
Оставшийся раствор добавили в подкисленный серной кислотой раствор перманганата калия св результате последний обесцветилмя.
Запишите 4 реакции.
1) 2P + 3I2 = 2PI3 ;
2) PI3 + 3H2O (нагр.
3) HI + AgNO3 = AgI↓ + HNO3 ;
4а) 5H3PO3 + 2KMnO4 + 3H2SO4 = 5H3PO4 + K2SO4 + 2MnSO4 + 3H2O или
4б) 10H3PO3 + 4KMnO4 + 2H2SO4 = 4Mn(H2PO4)2 + 2K2SO4 + 2H3PO4 + 6H2O.
Хлорат калия нагрели в присутствии катализатора?
Хлорат калия нагрели в присутствии катализатора.
Выделившийся бесцветный газ прореагировал с раскалённым железом с образованием железной окалины.
Твёрдый остаток растворили в необходимом количестве концентрированной серной кислоты, при этом наблюдали выделение газа с резким запахом.
К полученному прозрачному раствору добавили раствор карбоната калия и наблюдали образование бурого осадка и выделение газа.
Напишите уравнения четырёх описанных реакций.
1))Порошок магния нагрели в атмосфере азота?
1))Порошок магния нагрели в атмосфере азота.
При взаимодействии полученного вещества с водой выделился газ.
Газ пропустили через водный раствор сульфата хрома(3), в результате чего образовался серый осадок.
Осадок отделили и обработали при нагревании раствором, содержащим пероксид водорода и гидроксид калия.
Напишите уравнения четырёх описанных реакций.
2)) Оксид хрома(6) прореагировал с гидроксидом калия.
Полученное вещество обработали серной кислотой, из образовавшегося раствора выделили соль оранжевого цвета.
Эту соль обработали бромоводородной кислотой.
Полученное простое вещество вступило в реакцию с сероводородом.
Напишите уравнения четырёх описанных реакций.
3)) При взаимодействии оксида серы(6) с водой получили кислоту.
При обработке порошкообразного иодида калия концентрированным раствором этой кислоты образовались серые кристаллы простого вещества.
Это вещество прореагировало с алюминием.
Полученную соль растворили в воде и смешали с раствором карбоната натрия, в результате чего образовался осадок и выделился газ.
Напишите уравнения четырёх описанных реакций.
4)) Оксид меди(2) обработали раствором серной кислоты.
При электролизе образовавшегося раствора на инертном аноде выделился газ.
Газ смешали с оксидом азота(4) и поглотили водой.
К разбавленному раствору полученной кислоты добавили магний, в результате чего в растворе образовалось две соли, а выделения газообразных продуктов не происходило.
Напишите уравнения четырёх описанных реакций.
(Помогите ) Карбид двухвалентного металла обработали водой?
(Помогите ) Карбид двухвалентного металла обработали водой.
Газообразный продукт гидролиза смешали с равным объемом хлороводорода.
К образовавшемуся веществу добавили раствор гидроксида калия в спирте, смесь нагрели.
Продукт реакции обесцветил подкисленный раствор перманганата калия.
В процессе последней реакции образовался газообразный продукт, который не является органическим веществом.
Составьте уравнения описанных превращений, используя структурные формулы органических соединений.
Аммиак пропустили через бромоводородную кислоту?
Аммиак пропустили через бромоводородную кислоту.
К полученному раствору добавили раствор нитрата серебра.
Выпавший осадок отделили и нагрели с порошком цинка.
На образовавшийся в ходе реакции металл подействовали концентрированным раствором серной кислоты, при этом выделился газ с резким запахом.
Напишите уравнение четырёх описанных реакций.
Газ, выделившийся при нагревании раствора хлористого водородс оксидом марганца (4), ввели вовзаимодействие с алюминием?
Газ, выделившийся при нагревании раствора хлористого водород
с оксидом марганца (4), ввели во
взаимодействие с алюминием.
Продукт реакции растворили в воде и добавили
сначала избыток раствора гидроксида натрия, а затем соляную кислоту (избыток).
уравнения четырех описанных реакций.
Газ, образовавшийся пропускании хлористого водорода через горячий раствор хромата калия взаимодействует с железом?
Газ, образовавшийся пропускании хлористого водорода через горячий раствор хромата калия взаимодействует с железом.
Продукт реакции растворили в воде и добавили к нему сульфид натрия.
Более легкое из образовавшихся нерастворимых веществ отделили и ввели в реакцию с концентрированной серной кислотой.
К твердому веществу которое образуется при сжигании фосфора в избытке хлора добавили фосфор и смесь нагрели?
К твердому веществу которое образуется при сжигании фосфора в избытке хлора добавили фосфор и смесь нагрели.
Продукт реакции обработали небольшим количеством горячей воды и вполученный раствор добавили подкисленный раствор перманганата калия.
Написать уравнения 4 реакций.
Нитрат калия нагрели с порошкообразным свинцом до прекращения реакции?
Нитрат калия нагрели с порошкообразным свинцом до прекращения реакции.
Смесь продуктов обработали водой, а затем полученный раствор профильтровали.
Фильтрат подкислили серной кислотой и обработали йодидом калия.
Выделившееся простое вещество нагрели с концентрированной азотной кислотой.
В атмосфере образовавшегося при этом бурого газа сожгли красный фосфор.
Хлорат калия нагрели в присутствии катализатора?
Хлорат калия нагрели в присутствии катализатора.
бесцветный газ прореагировал с раскалённым железом с образованием
Твёрдый остаток растворили в необходимом количестве
концентрированной серной кислоты, при этом наблюдали выделение газа
с резким запахом.
К полученному прозрачному раствору добавили раствор
карбоната калия и наблюдали образование бурого осадка и выделение газа.
Напишите уравнения четырёх описанных реакций.
Газ, выделившегося при взаимодействие твердого хлорида натрия с коцентрированной серной кислотой , растворить в воде и добавили и добавили к нему нитрат серебра ?
Газ, выделившегося при взаимодействие твердого хлорида натрия с коцентрированной серной кислотой , растворить в воде и добавили и добавили к нему нитрат серебра .
При этом выпал белый осадок .
Напишите уравнения описанных реакций .
На этой странице сайта вы найдете ответы на вопрос Йод нагрели с избытком фосфора?, относящийся к категории Химия. Сложность вопроса соответствует базовым знаниям учеников 10 — 11 классов. Для получения дополнительной информации найдите другие вопросы, относящимися к данной тематике, с помощью поисковой системы. Или сформулируйте новый вопрос: нажмите кнопку вверху страницы, и задайте нужный запрос с помощью ключевых слов, отвечающих вашим критериям. Общайтесь с посетителями страницы, обсуждайте тему. Возможно, их ответы помогут найти нужную информацию.
Тренажер задания 31 по химии галогенов
Тренажер задания 31 из ЕГЭ по химии галогенов, задачи на неорганическую химию (мысленный эксперимент) из экзамена ЕГЭ по химии, задания 31 по химии галогенов с текстовыми решениями и ответами.
- Вещество, полученное на аноде при электролизе расплава иодида натрия с инертными электродами, выделили и ввели во взаимодействие с сероводородом. Газообразный продукт последней реакции растворили в воде и к полученному раствору добавили хлорное железо. Образовавшийся осадок отфильтровали и обработали горячим раствором гидроксида натрия. Напишите уравнения описанных реакций.
- Вещество, полученное на аноде при электролизе раствора иодида натрия с инертными электродами, ввели в реакцию с калием. Продукт реакции нагрели с концентрированной серной кислотой и выделившийся газ пропустили через горячий раствор хромата калия. Напишите уравнения описанных реакций.
- Хлорная вода имеет запах хлора. При подщелачивании запах исчезает, а при добавлении соляной кислоты – становится более сильным, чем был ранее. Напишите уравнения описанных реакций.
HCl + NaOH = NaCl + H2O
HClO + NaOH = NaClO + H2O
NaClO + 2HCl = NaCl + Cl2 + H2O
- Бесцветные газы выделяются при выдерживании концентрированной кислоты, как с хлоридом натрия, так и с иодидом натрия. При пропускании этих газов через водный раствор аммиака образуются соли. Напишите уравнения описанных реакций.
- При термическом разложении соли А в присутствии диоксида марганца образовались бинарная соль Б и газ, поддерживающий горение и входящий в состав воздуха, при нагревании этой соли без катализатора образуются соль Б и соль кислородсодержащей кислоты. При взаимодействии соли А с соляной кислотой выделяется жёлто-зелёный газ (простое вещество) и образуется соль Б. соль Б окрашивает пламя в фиолетовый цвет, при её взаимодействии с раствором нитрата серебра выпадает осадок белого цвета. Напишите уравнения описанных реакций.
6) При добавлении раствора кислоты А к диоксиду марганца происходит выделение ядовитого газа жёлто-зелёного газа. Пропустив выделившийся газ через горячий раствор едкого кали, получают вещество, которое используется при изготовлении спичек и некоторых других зажигательных составов. При термическом разложении последнего в присутствии диоксида марганца образуется соль, из которой при взаимодействии с концентрированной серной кислотой можно получить исходную кислоту А, и бесцветный газ , входящий в состав атмосферного воздуха. Напишите уравнения описанных реакций.
7) Йод нагрели с избытком фосфора, и продукт реакции обработали небольшим количеством воды. Газообразный продукт реакции полностью нейтрализовали раствором едкого натра и добавили в полученный раствор нитрат серебра. Напишите уравнения описанных реакций.
HI + NaOH = NaI + H2O
8) Газ, выделившийся при нагревании твердой поваренной соли с концентрированной серной кислотой, пропустили через раствор перманганата калия. Газообразный продукт реакции поглотили холодным раствором едкого натра. После добавления в полученный раствор йодоводородной кислоты появляется резкий запах и раствор приобретает тёмную окраску. Напишите уравнения описанных реакций.
NaClO + 2HI = NaCl + I2 + H2O
9) Через раствор бромида натрия пропустили газ, выделяющийся при взаимодействии соляной кислоты с перманганатом калия. После окончания реакции раствор выпарили, остаток растворили в воде и подвергли электролизу с графитовыми электродами. Газообразные продукты реакции смешали друг с другом и осветили. В результате произошел взрыв. Напишите уравнения описанных реакций.
10) К пиролюзиту осторожно прибавили раствор соляной кислоты, и выделившийся газ пропустили в химический стакан, наполненный холодным раствором едкого кали. После окончания реакции стакан накрыли картонкой и оставили, при этом стакан освещали солнечные лучи; через некоторое время в стакан внесли тлеющую лучинку, которая ярко вспыхнула. Напишите уравнения описанных реакций.
11) Вещество, выделяющееся на катоде и аноде при электролизе раствора йодида натрия с графитовыми электродами, реагируют друг с другом. Продукт реакции взаимодействуют с концентрированной серной кислотой с выделением газа, который пропустили через раствор гидроксида калия. Напишите уравнения описанных реакций.
http://himia.my-dict.ru/q/1752448_jod-nagreli-s-izbytkom-fosfora/
http://chemege.ru/zadanie-31-galogeny/