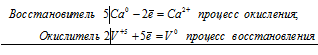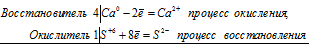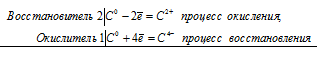Гидроксид кальция: способы получения и химические свойства
Гидроксид кальция Ca(OH)2 — неорганическое соединение. Белый, при нагревании разлагается без плавления. Проявляет основные свойства.
Относительная молекулярная масса Mr = 74,09; относительная плотность для тв. и ж. состояния d = 2,08.
Способы получения
1. Гидроксид кальция получают в результате взаимодействия гидрида кальция и воды , на выходе образуется водород и гидроксид кальция :
2 . При взаимодействии кальция с водой при комнатной температуре образуется гидроксид кальция и водород:
3. Оксид кальция при взаимодействии с водой при комнатой температуре образует гидроксид кальция:
Качественная реакция
Качественная реакция на гидроксид кальция — окрашивание фенолфталеина в малиновый цвет .
Химические свойства
1. Гидроксид кальция вступает в реакцию с простыми веществами :
1.1. Холодный гидроксид кальция (суспензия) взаимодействует с хлором и образует гипохлорит кальция, хлорид кальция и воду:
если с хлором реагирует горячий гидроксид кальция (суспензия), то в итоге образуется хлорат кальция, хлорид кальция и вода:
2. Гидроксид кальция взаимодействует со сложными веществами :
2.1. Гидроксид кальция реагирует с кислотами:
2.1.1. В результате реакции между гидроксидом кальция и разбавленной соляной кислотой образуется хлорид кальция и вода:
2.1.2. Гидроксид кальция взаимодействует с серной кислотой, образуя сульфат кальция и воду:
2.1.3. В результате взаимодействия гидроксида кальция и разбавленной фосфорной кислоты образуется фосфат кальция и вода:
если с гидроксидом кальция будет взаимодействовать концентрированная фосфорная кислота , то в результате реакции образуется гидрофосфат кальция и вода:
2.1.4. С гидроксидом кальция реагирует сероводородная кислота , образуя гидросульфид кальция и воду:
2.2. Гидроксид кальция взаимодействует с оксидами:
2.2.1. В результате взаимодействия гидроксида кальция и углекислого газа образуется карбонат кальция и вода:
если с углекислым газом реагирует карбонат кальция в виде суспензии, то образуется гидрокарбонат кальция в растворе:
2.2.2. Гидроксид кальция вступает в реакцию с оксидом серы (IV) , образуя на выходе сульфит кальция и воду:
если с оксидом серы (IV) взаимодействует гидроксид кальция в виде суспензии, то на выходе происходит образование гидросульфита кальция в растворе:
2.4. Гидроксид кальция реагирует с солями :
2.4.1. Гидроксид кальция (суспензия) взаимодействует с холодным гипохлоритом натрия , образуя гипохлорит кальция и гидроксид натрия:
Ca(OH)2 + 2NaClO = Ca(ClO)2↓ + 2NaOH
2.5. Гидроксид кальция взаимодействует с пероксидом водорода при 40 — 50º С с образованием пероксида кальция и воды:
3. Гидроксид кальция разлагается при температуре 520 — 580º С, образуя на выходе оксид кальция и воду:
Характеристика химических свойств кальция
Задание 337
Какое свойство кальция позволяет применять его в металлотермии для получения некоторых металлов из их соединений? Составьте электронные и молекулярные уравнения реакций кальция: а) с V2O5; б) СаSO4. В каждой из этих реакций окислитель восстанавливается максимально, приобретая низшую степень окисления.
Решение:
Благодаря большому отрицательному значению 
Уравнения реакций кальция:
5Ca 0 + 2V +5 = 5Ca 2+ + 2V 0
б) Ca + СаSO4 = CaO + CaS
4Ca 0 + S +6 = 4Ca 2+ + S 2-
4Са + CaSO4 = 4СаО + CaS
Задание 338
Какие соединения называют негашеной и гашеной известью? Составьте уравнения реакций их получения. Какое соединение образуется при прокаливании негашеной извести с углем? Что является окислителем и восстановителем в последней реакции? Составьте электронные и молекулярные уравнения.
Решение:
СаО – оксид кальция называют «негашеная известь». Са(ОН)2 – гидроксид кальция называют «гашённая известь».
а) Оксид кальция получают при термическом разложении известняка СаСО3:
Этот процесс протекает при температуре 1000 0 С (промышленный метод получения СаО).
б) При спекании известняка и графита получают оксид кальция:
Гашённую известь получают при действии воды на оксид кальция:
При прокаливании негашеной извести с углём образуется карбид кальция:
СаО + 3С СаС2 + СО
2Ca 0 + С 0 = 2Ca 2+ + С 4-
Таким образом, углерод является и окислителем, и восстановителем в данной реакции. Эта реакция является реакцией самоокисления-самовосстановления (реакцией диспропорционирования, дисмутации), потому что протекает с одновременным уменьшением и увеличением степени окисления одного и того же элемента (С – уголь).
Задание 339
Составьте электронные и молекулярные уравнения реакций: а) кальция с водой; б) магния с азотной кислотой, учитывая, что окислитель приобретает низшую степень окисления.
Решение:
Решение. 1 Согласно уравнению реакции находим теоретический выход
Главная > Решение
| Информация о документе | |
| Дата добавления: | |
| Размер: | |
| Доступные форматы для скачивания: |
Пояснения к решению задач
На гашеную известь, взятую в необходимом количестве, подействовали 3,15 г чистой азотной кислоты. Какую массу нитрата кальция Са(NО 3 ) 2 получили, если практический выход в массовых долях составляет 0,98 (или 98%) по сравнению с теоретическим?
Решение. 1) Согласно уравнению реакции находим теоретический выход:
Са(ОН) 2 + 2HNO 3

126 г 164 г m(HNO 3 ) = 2*63 = 126г
3.15 г х 1 М(Са(NO 3 ) 2 ) = 164г/моль
m(Са(NO 3 ) 2 ) =164г
126:3,15 = 164:х 1; х 1 = 

3) Находим 98%-ный выход:
4,1 г Ca(NO 3 ) 2 соответствуют 100%-ному выходу
Х 2 « « 98%-ному выходу
4,1 : х 2 = 100:98; х 2 =
http://buzani.ru/zadachi/khimiya-shimanovich/977-svojstva-kaltsiya-zadachi-337-339
http://gigabaza.ru/doc/35640.html