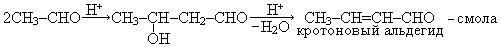I (старая). Гидратация ацетилена.
Реакция гидратации ацетилена сильно экзотермична
При низких температурах она необратима, при повышении температуры Кр быстро уменьшается и выше 300°С равновесие уже смещается влево. Гидратация по указанному уравнению идет с приемлемой скоростью только в присутствии катализаторов. Используется катализатор Кучерова – соли Нg 2+ в кислой среде. Реакция ускоряется при повышении температуры и концентрации Н2SO4, но при этом возрастает скорость побочной реакции альдольной конденсации
Чаще всего процесс проводят при 75-95 о С с 10-20% Н2SO4 и 0,5-1% катализатора (в пересчете на НgО).
В данном процессе полученный альдегид, являясь сильным восстановителем, окисляет соли Нg 2+ , поэтому для предотвращения дезактивации катализатора отдувают образующийся альдегид ацетиленом, который подается в реактор в некотором избытке, и добавляют в раствор соли Fe 3+ .
Fe 3+ + Hg + = Hg 2+ + Fe 2+
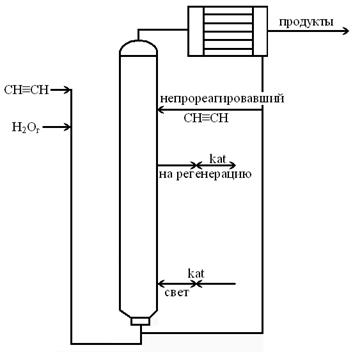
Процесс ведут в пустотелой стальной колонне (гидрататоре), гуммированной из нутрии или отфутированной керамикой, на 70-80% заполненной раствором, содержащим 150-200 г/л H2SO4, 0,8-1 г/л HgSO4 и 50 г/л Fe2(SO4)3.
Ацетилен смешивается с водяным паром и барботируется через раствор с образованием ацетильдегида и побочных продуктов, причем степень его конверсии составляет 40-50%.
Гидрататор не имеет поверхностей теплообмена и в нем устанавливается автотермический режим, при котором тепло реакции отводится за счет испарения воды. Ацетальдегид абсорбируется из продуктов водой и поступает на ректификацию с получением технического продукта. Не прореагировавший ацетилен возвращается в гидрататор. Для непрерывной работы системы происходит постоянная регенерация части катализатора и возвращением свежего катализатора в систему.
Гидратация алкинов по Кучерову
Вы будете перенаправлены на Автор24
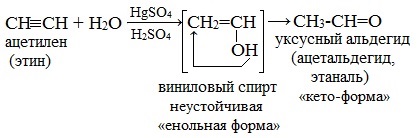
Алкины при наличии катализаторов присоединяют воду и образуют карбонильные соединения. Промышленное значение приобрела реакция гидратации ацетилена, открытая в 1881 г. М. Г. Кучеровым, который установил, что присоединение воды к ацетилену происходит в среде 10%-го раствора $H_2SO_4$ при наличии 5% сульфата ртути. Продуктом реакции является уксусный альдегид:
Механизм гидратации ацетилена
Гидратацию ацетилена называют реакцией Кучерова. Механизм этой реакции еще не полностью выяснен. Считают, что сначала к тройной углерод-углеродной связи присоединяется катализатор и образует с ним продукт присоединения (І). Продукт (І) далее гидролизуется в енол — неустойчивый виниловый спирт (II), который сразу же изомеризуется (таутомеризуеться) в термодинамически устойчивое соединение (в карбонильную форму) — уксусный альдегид (III):
Установлено, что кроме солей ртути гидратацию алкинов катализируют соли трехвалентного золота, одновалентной меди, одновалентного серебра и трехвалентного рутения. Механизм реакций Кучерова достаточно сложен, до конца не изучен и содержит еще много неясных моментов. В частности, неясна роль ионов металлов (йонов ртути в классической реакции) и путь образования винил-катионов в качестве промежуточных частиц.
Енолы
Органические соединения, в молекулах которых $OH$-группа соединена с атомом углерода с двойной связью, как например, в виниловом спирте (II), называют енолами («ен-» означает наличие в молекуле двойной $C = C$-связи, «-ол» — означает $OH$-группы спирта).
А. П. Эльтеков в 1877 сформулировал правило, согласно которому ненасыщенные спирты с группой -$OH$ у атома углерода с двойной связью являются неустойчивыми и самовольно изомеризуются в устойчивые карбонильные соединения. Это правило выполняется преимущественно для простых енольных систем.
Готовые работы на аналогичную тему
Исследования химиков показали, что всегда при извлечении соединения с енольной структурой получают изомерные ей соединения с карбонильной структурой. Между енольной и карбонильной структурами существует равновесие:
Такая перегруппировка енольной структуры в карбонильную происходит особенно легко и поэтому равновесие этого процесса сильно смещено в сторону карбонильной структуры. Причина такой изомеризации заключается в том, что вследствие высокой полярности связи $O-H$ атом водорода этой группы енола может легко отщеплятся от атома кислорода в виде иона. При обратном присоединении этот ион водорода может присоединятся как к атому кислорода, так и к атому углерода с двойной связью. Если $H^+$ присоединится к кислороду, то очень легко сможет снова отщепиться. Если этот ион присоединится к углероду, то уже останется соединенным с ним, поскольку полярность связи $C-H$ достаточно мала. В результате происходит перегруппировка, при которой сильная кислота превращается в значительно более слабую:
Структурные изомеры, между которыми существует равновесие, называют таутомерами, а явление существования такой изомерии называют таутомерия.
Гидратация гомологов ацетилена
Гидратация гомологов ацетилена приводит к образованию кетонов. Присоединение воды к алкинам-1 происходит по правилу Марковникова. Например, при гидратации пропина образуется диметилкетон (ацетон):
Из терминальных алкинов $R-CHC-H$ при гидратации получают почти всегда метилкетоны $R-CO-CH_3$, а из двцзамещенныих $R»-CH_2-R’$ ($R»$ и $R’$ — различные по строению алкильные группы) — кетоны, образование которых подчиняется такой такой тенденции: для первичного $R$ ($CH_3$- или $CH_3-CH_2-$) и вторичного или третичного $R$ ($-CH(CH_3)_2$ или $-C(CH_3)_3$) карбонильная группа $C =O$ образуется в основном в $\alpha$-положении к вторичному или третичному атому углерода алкиле $R$. Так, при гидратации метилизопропилацетилена в реакционной смеси будет преобладать етилизопропилкетон по сравнению изобутилметилкетоном:
Катализируемые кислотами и ионами ртути (II) реакции присоединения воды по месту тройной связи алкинов протекает строго по правилу Марковникова. Следовательно, гидратация как терминальноых, так и нетерминальных алкинов всегда приводит к кетонам, например для циклических и линейных алкинов:
Гидратация ацетилена реакция уравнение гидролиза
Реакция Кучерова (гидратация алкинов) – гидратация ацетилена с образованием ацетальдегида и гомологов ацетилена с образованием кетонов в присутствии солей ртути в качестве катализатора.
Реакция гидратации ацетилена (присоединение воды) была открыта в 1881 г. русским ученым М.Г. Кучеровым, который пытался получить непредельный спирт (виниловый), а затем его полимеризовать. Вместо ожидаемого спирта Кучеров выделил легкокипящую жидкость с характерным запахом – уксусный альдегид.
Реакция идет в присутствии солей ртути (обычно HgSO4) в серной кислоте и идет через образование неустойчивого непредельного спирта (енола), который изомеризуется в уксусный альдегид (в случае ацетилена):
На первой стадии образуются енолы (соединения, в молекулах которых гидроксогруппы соединены с атомом углерода при двойной связи).
Т.к. образующийся на промежуточном этапе виниловый спирт неустойчив, то происходит перегруппировка в термодинамически белее стабильную изомерную структуру – уксусный альдегид. Эта перегруппировка получила название перегруппировка Эльтекова-Эрленмейера.
Реакция имеет большое практическое значение, т. к. уксусный альдегид применяется в технике для получения уксусной кислоты и этилового спирта.
При гидратации гомологов ацетилена образуются кетоны, т.к. присоединение воды по тройной связи происходит в соответствии с правилом Марковникова, и группа -ОН оказывается не у концевого, а у центрального углеродного атома:
http://spravochnick.ru/himiya/aldegidy_i_ketony/gidrataciya_alkinov_po_kucherovu/
http://himija-online.ru/imennye-reakcii/reakciya-kucherova.html