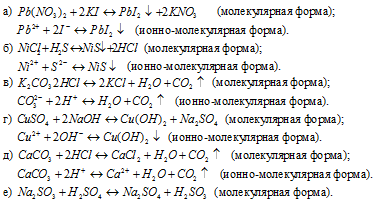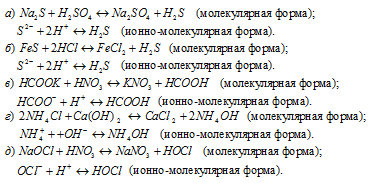Cоставление ионно-молекулярных форм уравнений реакций
Задача 580.
Написать в ионно-молекулярной форме уравнения реакций, приводящих к образованию малорастворимых осадков или газов: 
Решение:
Так как реакция протекает с образованием сернистой кислоты – слабого электролита и при этом не выпадает осадок и не выделяется газ, то, по условию задачи, ионно-молекулярное уравнение не пишем.
Задача 581.
Написать в ионно-молекулярной форме уравнения реакций, приводящих к образованию малодиссoциированных соединений: 
Решение:
Задача 582.
Написать в ионно-молекулярной форме уравнения реакций нейтрализации: 
Указать, какие из этих реакций протекают обратимо, а какие необратимо.
Решение:
а) 2HCl + Ba(OH)2 ⇔ BaCl2 + 2H2O (молекулярная форма);
2H + + 2OH — ⇔ 2H 2 O (ионно-молекулярная форма).
Реакция протекает до конца, так как в реакцию вступают сильные электролиты соляная кислота и гидроксид бария образуется слабый электролит вода.
б) HF + KOH ⇔ KF + H2O (молекулярная форма);
H + + OH — ⇔ H2O (ионно-молекулярная форма).
В реакции участвуют два слабых электролита фтороводород и вода, согласно принципу Ле Шателье, равновесие реакции будет смещено в сторону более слабого электролита, т.е. вправо в сторону образования воды. Реакция обратима.
в) Fe(OH)3 + 3HNO3 ⇔ Fe(NO3)3 + 3H2O (молекулярная форма);
3H + + 3OH — ⇔ 3H2O (ионно-молекулярная форма).
В реакции участвуют слабое малорастворимое основание и сильная кислота, равновесие будет смещено в сторону образования более слабого электролита воды. Реакция будет протекать до конца.
г) CH3COOH + NH4OH ⇔ CH3COONH4 + H2O (молекулярная форма);
H + + OH — ⇔ H2O (ионно-молекулярная форма).
Реакция обратима, так как в реакции участвуют три слабых электролита уксусная кислота, гидроксид аммония и вода. Согласно принципу Ле Шателье равновесие системы будет смещено в сторону образования самого слабого электролита, вправо, в сторону образования воды.
д) HNO2 + NH4OH ⇔ NH4NO2 + H2O (молекулярная форма);
H + + OH — ⇔ H2O (ионно-молекулярная форма).
Реакция обратима, так как в реакции участвуют три слабых электролита уксусная кислота, гидроксид аммония и вода. Согласно принципу Ле Шателье равновесие системы будет смещено в сторону образования самого слабого электролита, вправо, в сторону образования воды.
е) H2S + 2NH4OH ⇔ (NH4)2S + 2H2O (молекулярная форма);
2H + + 2OH — ⇔ 2H2O (ионно-молекулярная форма).
Реакция обратима, так как в реакции участвуют три слабых электролита сероводородная кислота, гидроксид аммония и вода. Согласно принципу Ле Шателье равновесие системы будет смещено в сторону образования самого слабого электролита, вправо, в сторону образования воды.
Таким образом, реакции нейтрализации, в которых участвуют слабые кислоты или основания, — обратимы, т.е. могут протекать как в прямом так и в обратном направлении.
Гидроксид аммония + серная кислота?
Химия | 1 — 4 классы
Гидроксид аммония + серная кислота.
В результате реакции гидроксида аммония (NH4OH) с серной кислотой (H2SO4) образуется сульфат аммония ((NH4)2SO4) и вода (H2O).
Что общего между сернистой кислотой и гидроксидом аммония?
Что общего между сернистой кислотой и гидроксидом аммония.
Напишите уравнения осуществимых реакций между ; а) селикатом натрия и хлоридом кальция б) сульфидом натрия и серной кислотой в) гидроксидом меди (II) и серной кислотой г) оксидом меди (II) и соляной к?
Напишите уравнения осуществимых реакций между ; а) селикатом натрия и хлоридом кальция б) сульфидом натрия и серной кислотой в) гидроксидом меди (II) и серной кислотой г) оксидом меди (II) и соляной кислотой д) нитратом калия и гидроксидом натрия е) нитратом аммония и азотной кислотой.
Напишите молекулярное и ионно — молекулярное уравнение реакции взаимодействия :ортофосфорной кислоты с одним моль гидроксида калия ;гидроксида калия с ортофосфорной кислотой ;серной кислоты с хлоридом?
Напишите молекулярное и ионно — молекулярное уравнение реакции взаимодействия :
ортофосфорной кислоты с одним моль гидроксида калия ;
гидроксида калия с ортофосфорной кислотой ;
серной кислоты с хлоридом бария ;
серной кислоты с гидроксидом аммония ;
сульфата меди с гидроксидом натрия ;
нитрата серебра и хлорида натрия.
GaOHSO4 + H2SO4 = N2O5 + Ca(OH)2 = SnO + NaOH = сульфид лития + серная кислота = сероводород + гидроксид аммония = нитрат цинка + серная кислота = гидроксосульфат хрома (III) + серная кислота = уксусн?
GaOHSO4 + H2SO4 = N2O5 + Ca(OH)2 = SnO + NaOH = сульфид лития + серная кислота = сероводород + гидроксид аммония = нитрат цинка + серная кислота = гидроксосульфат хрома (III) + серная кислота = уксусная кислота + гидроксид аммония = помогите плизззз.
С образованием осадка протекает реакция между растворами : А) сульфата аммония и гидроксида натрия Б) хлорида бария и нитрата серебра В) гидроксида натрия и серной кислоты Г) карбоната натрия и азотно?
С образованием осадка протекает реакция между растворами : А) сульфата аммония и гидроксида натрия Б) хлорида бария и нитрата серебра В) гидроксида натрия и серной кислоты Г) карбоната натрия и азотной кислоты.
Рассчитайте массовые доли элементов, входящих в состав : а)серной кислоты б)ортофосфорной кислоты в)гидроксида меди 2 г)бромида аммония?
Рассчитайте массовые доли элементов, входящих в состав : а)серной кислоты б)ортофосфорной кислоты в)гидроксида меди 2 г)бромида аммония.
1 гидроксид кальция + соляная кислота — 2 фосфорная кислота + гидроксид калия — 3 гидроксид железа (III) + соляная кислота — 4 гидроксид цынка + серная кислота — 5 серная кислота + гидроксид алюминия ?
1 гидроксид кальция + соляная кислота — 2 фосфорная кислота + гидроксид калия — 3 гидроксид железа (III) + соляная кислота — 4 гидроксид цынка + серная кислота — 5 серная кислота + гидроксид алюминия — 6 гидроксид магния + фосфорная кислота — 7 серная кислота + гидроксид лития -.
Все соли аммония одинаковым образом реагируют с раствором : а) нитрата серебра б) гидроксида натрия в) хлорида бария г) серной кислоты?
Все соли аммония одинаковым образом реагируют с раствором : а) нитрата серебра б) гидроксида натрия в) хлорида бария г) серной кислоты.
Напишите молекулярные и ионные уравнения между растворами?
Напишите молекулярные и ионные уравнения между растворами.
1)гидроксида лития и серной кислоты.
2)бромида аммония и гидроксида натрия.
3)нитрата алюминия и гидроксида калия.
4)карбоната лития и азотной кислоты.
Напишите молекулярные и ионные уравнения между растворами?
Напишите молекулярные и ионные уравнения между растворами.
1)гидроксида лития и серной кислоты.
2)бромида аммония и гидроксида натрия.
3)нитрата алюминия и гидроксида калия.
4)карбоната лития и азотной кислоты.
На этой странице вы найдете ответ на вопрос Гидроксид аммония + серная кислота?. Вопрос соответствует категории Химия и уровню подготовки учащихся 1 — 4 классов классов. Если ответ полностью не удовлетворяет критериям поиска, ниже можно ознакомиться с вариантами ответов других посетителей страницы или обсудить с ними интересующую тему. Здесь также можно воспользоваться «умным поиском», который покажет аналогичные вопросы в этой категории. Если ни один из предложенных ответов не подходит, попробуйте самостоятельно сформулировать вопрос иначе, нажав кнопку вверху страницы.
Чистые в — ва нефть . Руда, алюминий, углекислый газ однород смеси лимонад, морская вода неоднород смеси воздух гранит кровь пыль.
Cu + O = CuO + 155Кдж Наверное так.
CH₄ + 3O₂ = CO₂ + 2H₂O количество вещества углекислого газа n(CO₂) = n(CH₄) = v(CH₄) / v₀ n(CO₂) = 4, 48 / 22, 4 = 0, 2 моль количество вещества гидроксида натрия n(NaOH) = m(NaOH) / M(NaOH) = vpw / M(NaOH) n(NaOH) = 100 * 1, 31 * 0, 28 / 40 = 0, 917..
Держи характеристику калия.
1) 2Cu + 2H2O→2CuOH + H2 2) Re + Pb(NO3)2→Fe(NO3)2 + Pb 3) Zn + S→ZnS 4) 2Al + 6HCl→2AlCl3 + 3H2.
Б)Na2CO3 + CuS = Na2S + CuCO3(осадок) в)K2CO3 + Ba(NO3)2 = 2KNO3 + BaCO3(осадок).
Ag — золото, благородный металл, который не хочет взаимодействовать с другими элементами.
Соли аммония: получение и химические свойства
Соли аммония
Соли аммония – это соли, состоящие из катиона аммония и аниона кислотного остатка .
Способы получения солей аммония
1. Соли аммония можно получить взаимодействием аммиака с кислотами . Реакции подробно описаны выше.
2. Соли аммония также получают в обменных реакциях между солями аммония и другими солями.
Например , хлорид аммония реагирует с нитратом серебра:
3. Средние соли аммония можно получить из кислых солей аммония . При добавлении аммиака кислая соль переходит в среднюю.
Например , гидрокарбонат аммония реагирует с аммиаком с образованием карбоната аммония:
Химические свойства солей аммония
1. Все соли аммония – сильные электролиты , почти полностью диссоциируют на ионы в водных растворах:
NH4Cl ⇄ NH4 + + Cl –
2. Соли аммония проявляют свойства обычных растворимых солей –вступают в реакции обмена с щелочами, кислотами и растворимыми солями , если в продуктах образуется газ, осадок или образуется слабый электролит.
Например , карбонат аммония реагирует с соляной кислотой. При этом выделяется углекислый газ:
Соли аммония реагируют с щелочами с образованием аммиака.
Например , хлорид аммония реагирует с гидроксидом калия:
NH4Cl + KOH → KCl + NH3 + H2O
Взаимодействие с щелочами — качественная реакция на ионы аммония. Выделяющийся аммиак можно обнаружить по характерному резкому запаху и посинению лакмусовой бумажки.
3. Соли аммония подвергаются гидролизу по катиону , т.к. гидроксид аммония — слабое основание:
4. При нагревании соли аммония разлагаются . При этом если соль не содержит анион-окислителя, то разложение проходит без изменения степени окисления атома азота. Так разлагаются хлорид, карбонат, сульфат, сульфид и фосфат аммония:
Если соль содержит анион-окислитель, то разложение сопровождается изменением степени окисления атома азота иона аммония. Так протекает разложение нитрата, нитрита и дихромата аммония:
При температуре 250 – 300°C:
При температуре выше 300°C:
Разложение бихромата аммония («вулканчик»). Оранжевые кристаллы дихромата аммония под действием горящей лучинки бурно реагируют. Дихромат аммония – особенная соль, в ее составе – окислитель и восстановитель. Поэтому «внутри» этой соли может пройти окислительно-восстановительная реакция (внутримолекулярная ОВР):
Окислитель – хром (VI) превращается в хром (III), образуется зеленый оксид хрома. Восстановитель – азот, входящий в состав иона аммония, превращается в газообразный азот. Итак, дихромат аммония превращается в зеленый оксид хрома, газообразный азот и воду. Реакция начинается от горящей лучинки, но не прекращается, если лучинку убрать, а становится еще интенсивней, так как в процессе реакции выделяется теплота, и, начавшись от лучинки, процесс лавинообразно развивается. Оксид хрома (III) – очень твердое, тугоплавкое вещество зеленого цвета, его используют как абразив. Температура плавления – почти 2300 градусов. Оксид хрома – очень устойчивое вещество, не растворяется даже в кислотах. Благодаря устойчивости и интенсивной окраске окись хрома используется при изготовлении масляных красок.
Видеоопыт разложения дихромата аммония можно посмотреть здесь.
http://himia.my-dict.ru/q/3327499_gidroksid-ammonia-sernaa-kislota/
http://chemege.ru/soli-ammoniya/