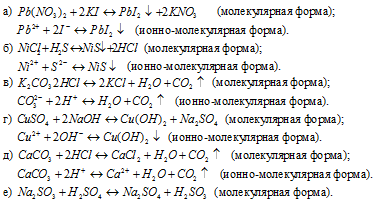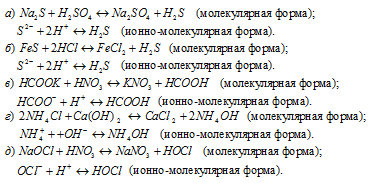Соли аммония: получение и химические свойства
Соли аммония
Соли аммония – это соли, состоящие из катиона аммония и аниона кислотного остатка .
Способы получения солей аммония
1. Соли аммония можно получить взаимодействием аммиака с кислотами . Реакции подробно описаны выше.
2. Соли аммония также получают в обменных реакциях между солями аммония и другими солями.
Например , хлорид аммония реагирует с нитратом серебра:
3. Средние соли аммония можно получить из кислых солей аммония . При добавлении аммиака кислая соль переходит в среднюю.
Например , гидрокарбонат аммония реагирует с аммиаком с образованием карбоната аммония:
Химические свойства солей аммония
1. Все соли аммония – сильные электролиты , почти полностью диссоциируют на ионы в водных растворах:
NH4Cl ⇄ NH4 + + Cl –
2. Соли аммония проявляют свойства обычных растворимых солей –вступают в реакции обмена с щелочами, кислотами и растворимыми солями , если в продуктах образуется газ, осадок или образуется слабый электролит.
Например , карбонат аммония реагирует с соляной кислотой. При этом выделяется углекислый газ:
Соли аммония реагируют с щелочами с образованием аммиака.
Например , хлорид аммония реагирует с гидроксидом калия:
NH4Cl + KOH → KCl + NH3 + H2O
Взаимодействие с щелочами — качественная реакция на ионы аммония. Выделяющийся аммиак можно обнаружить по характерному резкому запаху и посинению лакмусовой бумажки.
3. Соли аммония подвергаются гидролизу по катиону , т.к. гидроксид аммония — слабое основание:
4. При нагревании соли аммония разлагаются . При этом если соль не содержит анион-окислителя, то разложение проходит без изменения степени окисления атома азота. Так разлагаются хлорид, карбонат, сульфат, сульфид и фосфат аммония:
Если соль содержит анион-окислитель, то разложение сопровождается изменением степени окисления атома азота иона аммония. Так протекает разложение нитрата, нитрита и дихромата аммония:
При температуре 250 – 300°C:
При температуре выше 300°C:
Разложение бихромата аммония («вулканчик»). Оранжевые кристаллы дихромата аммония под действием горящей лучинки бурно реагируют. Дихромат аммония – особенная соль, в ее составе – окислитель и восстановитель. Поэтому «внутри» этой соли может пройти окислительно-восстановительная реакция (внутримолекулярная ОВР):
Окислитель – хром (VI) превращается в хром (III), образуется зеленый оксид хрома. Восстановитель – азот, входящий в состав иона аммония, превращается в газообразный азот. Итак, дихромат аммония превращается в зеленый оксид хрома, газообразный азот и воду. Реакция начинается от горящей лучинки, но не прекращается, если лучинку убрать, а становится еще интенсивней, так как в процессе реакции выделяется теплота, и, начавшись от лучинки, процесс лавинообразно развивается. Оксид хрома (III) – очень твердое, тугоплавкое вещество зеленого цвета, его используют как абразив. Температура плавления – почти 2300 градусов. Оксид хрома – очень устойчивое вещество, не растворяется даже в кислотах. Благодаря устойчивости и интенсивной окраске окись хрома используется при изготовлении масляных красок.
Видеоопыт разложения дихромата аммония можно посмотреть здесь.
Cоставление ионно-молекулярных форм уравнений реакций
Задача 580.
Написать в ионно-молекулярной форме уравнения реакций, приводящих к образованию малорастворимых осадков или газов: 
Решение:
Так как реакция протекает с образованием сернистой кислоты – слабого электролита и при этом не выпадает осадок и не выделяется газ, то, по условию задачи, ионно-молекулярное уравнение не пишем.
Задача 581.
Написать в ионно-молекулярной форме уравнения реакций, приводящих к образованию малодиссoциированных соединений: 
Решение:
Задача 582.
Написать в ионно-молекулярной форме уравнения реакций нейтрализации: 
Указать, какие из этих реакций протекают обратимо, а какие необратимо.
Решение:
а) 2HCl + Ba(OH)2 ⇔ BaCl2 + 2H2O (молекулярная форма);
2H + + 2OH — ⇔ 2H 2 O (ионно-молекулярная форма).
Реакция протекает до конца, так как в реакцию вступают сильные электролиты соляная кислота и гидроксид бария образуется слабый электролит вода.
б) HF + KOH ⇔ KF + H2O (молекулярная форма);
H + + OH — ⇔ H2O (ионно-молекулярная форма).
В реакции участвуют два слабых электролита фтороводород и вода, согласно принципу Ле Шателье, равновесие реакции будет смещено в сторону более слабого электролита, т.е. вправо в сторону образования воды. Реакция обратима.
в) Fe(OH)3 + 3HNO3 ⇔ Fe(NO3)3 + 3H2O (молекулярная форма);
3H + + 3OH — ⇔ 3H2O (ионно-молекулярная форма).
В реакции участвуют слабое малорастворимое основание и сильная кислота, равновесие будет смещено в сторону образования более слабого электролита воды. Реакция будет протекать до конца.
г) CH3COOH + NH4OH ⇔ CH3COONH4 + H2O (молекулярная форма);
H + + OH — ⇔ H2O (ионно-молекулярная форма).
Реакция обратима, так как в реакции участвуют три слабых электролита уксусная кислота, гидроксид аммония и вода. Согласно принципу Ле Шателье равновесие системы будет смещено в сторону образования самого слабого электролита, вправо, в сторону образования воды.
д) HNO2 + NH4OH ⇔ NH4NO2 + H2O (молекулярная форма);
H + + OH — ⇔ H2O (ионно-молекулярная форма).
Реакция обратима, так как в реакции участвуют три слабых электролита уксусная кислота, гидроксид аммония и вода. Согласно принципу Ле Шателье равновесие системы будет смещено в сторону образования самого слабого электролита, вправо, в сторону образования воды.
е) H2S + 2NH4OH ⇔ (NH4)2S + 2H2O (молекулярная форма);
2H + + 2OH — ⇔ 2H2O (ионно-молекулярная форма).
Реакция обратима, так как в реакции участвуют три слабых электролита сероводородная кислота, гидроксид аммония и вода. Согласно принципу Ле Шателье равновесие системы будет смещено в сторону образования самого слабого электролита, вправо, в сторону образования воды.
Таким образом, реакции нейтрализации, в которых участвуют слабые кислоты или основания, — обратимы, т.е. могут протекать как в прямом так и в обратном направлении.
Реакция образования солей аммония
Соли аммония — что это такое
Соли аммония являются солями, в состав которых входит катион аммония и анион кислотного остатка.
Соли аммония относятся к сложным веществам. Ион аммония образуется при взаимодействии аммиака с катионом водорода по донорно-акцепторному механизму. Соединения сформированы катионом аммония ( N H 4 ) + и кислотным остатком:
- хлорид аммония N H 4 C l ;
- сульфат аммония ( N H 4 ) 2 S O 4 ;
- нитрат аммония N H 4 N O 3 .
Свойства нелетучих солей аммония схожи со свойствами солей натрия или калия. Соединения характеризуются ионным строением и имеют вид белых кристаллов. Соли аммония обладают хорошей растворимостью в водной среде. Кристаллическая решетка с атомами хлорида аммония изображена на схеме:
Химические и физические свойства
Общие физические свойства солей аммония:
- твердые вещества;
- кристаллическая структура;
- хорошая растворимость в воде;
- отсутствие цвета.
Соли аммония являются сильными электролитами, которые диссоциируют в водных растворах:
N H 4 C l → N H 4 + + C l —
Разложение солей аммония при нагревании в случае летучей кислоты:
N H 4 C l → N H 3 + H C l
N H 4 H C O 3 → N H 3 + H 2 O + C O 2
Разложение солей аммония в условиях термического воздействия, если анион проявляет окислительные свойства:
N H 4 N O 3 → N 2 O + 2 H 2 O
( N H 4 ) 2 C r 2 O 7 → N 2 + C r 2 O 3 + 4 H 2 O
Соли аммония способны вступать в реакции обмена с кислотами:
( N H 4 ) 2 C O 3 + 2 H C l → 2 N H 4 C l + H 2 O + C O 2
Реакции обмена солей аммония с солями:
( N H 4 ) 2 S O 4 + B a C l 2 → B a S O 4 + 2 N H 4 C l
Соли аммония вступают в химические реакции гидролиза (как соль слабого основания и сильной кислоты):
N H 4 C l + H 2 O → N H 4 O H + H C l
Качественная реакция, как реагирует со щелочами
Качественную реакцию на ион аммония можно наблюдать в процессе нагрева солей аммония со щелочами, что приводит к выделению аммиака:
N H 4 C l + N a O H → N a C l + N H 3 + H 2 O
Признаком реакции является выделение газа с резким запахом.
Соли аммония обладают свойствами классических растворимых солей, то есть могут вступать в реакции обмена при образовании газа, осадка, слабого электролита с такими веществами, как:
- щелочи;
- кислоты;
- растворимые соли.
Реакция
Качественная реакция на аммиак: к отверстию сосуда, содержащего аммиак нужно поднести стеклянную палочку, смоченную в концентрированной соляной кислоте, в результате реакции появляется густой белый дым: это выделился хлорид аммония.
N H 3 + H C l = N H 4 C l
Способы получения солей аммония, где применяются
Распространенным методом синтеза солей аммония является химическое взаимодействие аммиака или гидроксида аммония и кислот.
Получают соли аммония при взаимодействии аммиака или гидроксида аммония с кислотами:
2 N H 3 + H 2 S O 4 → ( N H 4 ) 2 S O 4
Химический процесс, при котором аммиак взаимодействует с хлором, приводит к образованию нашатыря:
8 N H 3 + 3 C l 2 → N 2 + 6 N H 4 C l
Области применения солей аммония:
- Нитрат аммония называют аммиачной селитрой. Формула N H 4 N O 3 . Вещество используют в качестве азотного удобрения, как сырье в производстве взрывчатки в виде аммонитов.
- Сульфат аммония. Формула ( N H 4 ) 2 S O 4 . Соль является недорогим азотным удобрением.
- Гидрокарбонат аммония N H 4 H C O 3 и карбонат аммония ( N H 4 ) 2 C O 3 . Вещества выполняют роль разрыхлителей теста — компонентов мучных кондитерских изделий. Данные соли аммония применяют в процессе окрашивания тканых полотен. Соединения используют для производства витаминов и в медицинской отрасли.
- Хлорид аммония носит название нашатырь. Формула N H 4 C l . Данный материал используют при изготовлении гальванических компонентов, то есть сухих батарей. Вещества участвуют в процессе пайки и лужения. Хлорид аммония нашел применение в текстильной промышленности. Такие соединения являются эффективными удобрениями, активно используются в области ветеринарии и медицине.
http://buzani.ru/zadachi/khimiya-glinka/1194-ionno-molekulyarnaya-forma-uravneniya-zadachi-580-582
http://wika.tutoronline.ru/himiya/class/11/reakcziya-obrazovaniya-solej-ammoniya