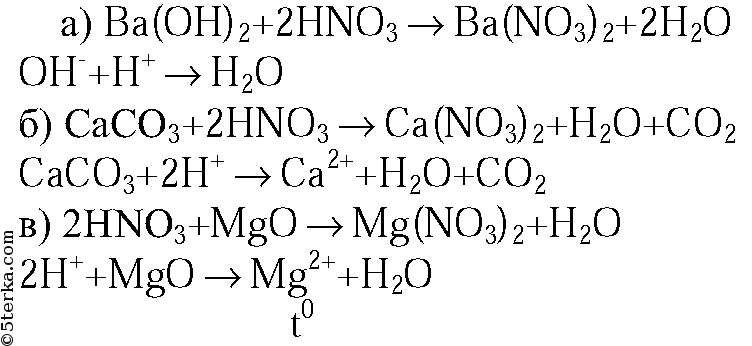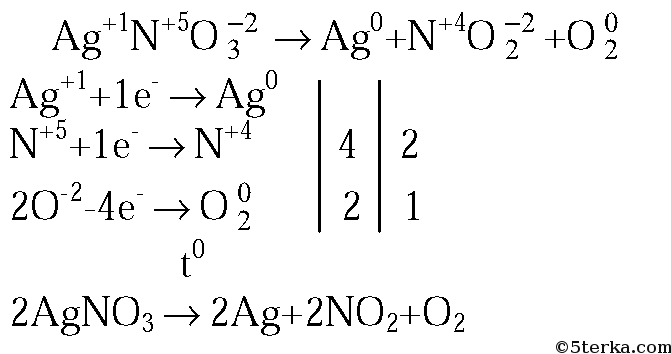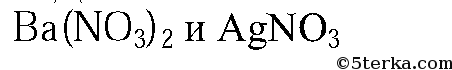Оксиды магния и кальция MgO, CaO
Физические свойства:
- бесцветные кристаллы;
- имеют высокие температуры плавления и кипения;
- хорошо растворяются в воде;
- обладают оснОвными свойствами.
Химические свойства оксидов магния и кальция:
- реагируют с кислотами:
MgO+H2SO4 = MgSO4+H2O - с кислотными оксидами:
CaO+SO3 = CaSO4 - растворяясь в воде, образуют сильнощелочные растворы гидроксидов:
MgO+H2O = Mg(OH)2
Промышленное получение MgO, CaO производят термическим разложением природных карбонатов магния (при температуре 700-900°:C), карбонатов кальция (1000-1200°C):
MgCO3 = MgO+CO2↑
Применение оксида магния MgO (жженая магнезия):
- получение магния;
- производство огнеупорных материалов;
- в производстве резины.
Применение оксида кальция CaO (негашеная известь):
- в строительстве;
- как флюс в металлургии;
- в роли катализатора в органическом синтезе.
Гидроксиды магния и кальция
Физические свойства Mg(OH)2, Ca(OH)2:
- твердые кристаллы;
- гидроксид кальция плохо растворим в воде, образует известковую воду (обладает щелочными свойствами);
- гидроксид магния практически нерастворим в воде.
Гидроксид кальция — сильное основание, гидроксид магния является основанием средней силы.
Химические свойства гидроксидов кальция и магния:
- реагируют с кислотами:
Ca(OH)2+2HCl = CaCl2+2H2O
Mg(OH)2+H2SO4 = MgSO4+2H2O - реагируют с кислотными оксидами:
- Ca(OH)2+CO2 = CaCO3↓+H2O — на первом этапе реакции взаимодействия углекислого газа с известковой водой образуется карбонат кальция, выпадающий в осадок;
- CaCO3+CO2+H2O = Ca(HCO3)2 — на втором этапе образуется растворимая в воде кислая соль.
- разлагаются при термической обработке,образуя оксиды:
Ca(OH)2 = CaO+H2O
Получение:
- Mg(OH)2 получают из морской воды осаждением известью;
- Ca(OH)2 — гашеную известь получают в результате реакции оксида кальция (негашеной извести) с водой:
CaO+H2O = Ca(OH)2; - гашеная известь, приготовленная в виде порошка, носит название пушонки.
Применение гидроксида магния:
- получение жженой магнезии;
- рафинирование сахара;
- очистка воды;
- в зубных пастах.
Применение гидроксида кальция:
- приготовление известкового раствора;
- обессахаривание патоки;
- умягчение воды;
- раскисление почвы;
- изготовление стекла
- получение различных соединений кальция.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
Оксид магния: способы получения и химические свойства
Оксид магния MgO — бинарное неорганическое вещество . Белый, тугоплавкий, термически устойчивый, не реагирует с водой. Проявляет основные свойства.
Относительная молекулярная масса Mr = 40,3; относительная плотность для тв. и ж. состояния d = 3,62; tпл ≈ 2825º C; tкип = 3600º C.
Способ получения
1. Оксид магния получается при разложении карбоната магния при температуре 350 — 650º C. В результате разложения образуется оксид магния и углекислый газ:
2. В результате разложения нитрата магния при температуре выше 300º С образуется оксид магния, оксид азота (IV) и кислород:
3. Гидроксид магния разлагается при 350-480º С с образованием оксида магния и воды:
4. Оксид магния можно получить путем разложения сульфата магния при температуре выше 1200º C, образуется оксид магния, кислород и оксид серы (IV):
5. Оксид магния можно получить сжиганием магния в в кислороде при 600 — 650º С:
2Mg + O2 = 2MgO
Химические свойства
1. Оксид магния реагирует с простыми веществами :
1.1. В результате реакции между оксидом магния и кальцием при температуре выше 400º С образуется магний и оксид кальция:
MgO + Ca = CaO + Mg
1.2. Оксид магния реагирует с углеродом при температуре выше 2000º С и образует магний и угарный газ:
MgO + C = Mg + CO
2. Оксид магния взаимодействует со сложными веществами:
2.1. Оксид магния взаимодействует с кислотами . При этом образуются соль и вода.
2.1.1. О ксид магния с разбавленной соляной кислотой образует хлорид магния и воду:
MgO + 2HCl = MgCl2 + H2O
2.3. Оксид магния взаимодействует с водой при 100 — 125º С, образуя гидроксид магния:
Вариант 4
Вопросы:
1. Напишите молекулярные и ионные уравнения реакций между раствором азотной кислоты и: а) гидроксидом бария; б) карбонатом кальция; в) оксидом магния.
2. Напишите уравнение реакции разложения нитрата серебра при нагревании. Укажите степени окисления элементов и расставьте коэффициенты с помощью метода электронного баланса.
3. В трех пронумерованных пробирках находятся растворы серной, азотной и соляной кислот. Как их можно распознать? Напишите уравнения соответствующих реакций.
Ответы и решения:
3. Данные вещества можно распознать при помощи растворов

задача №4
к главе «Тема III. Подгруппа азота. Работа 2. Азотная кислота и ее соли».
http://chemege.ru/oksid-magniya/
http://5terka.com/node/11425