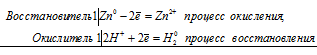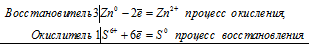Гидроксид цинка
Гидроксид цинка
Способы получения
1. Гидроксид цинка можно получить пропусканием углекислого газа, сернистого газа или сероводорода через раствор тетрагидроксоцинката натрия:
Чтобы понять, как протекает эта реакция, можно использовать несложный прием: мысленно разбить исходное вещество Na2[Zn(OH)4] на составные части: NaOH и Zn(OH)2. Далее мы определяем, как реагирует углекислый газ с каждым из этих веществ, и записываем продукты их взаимодействия. Т.к. Zn(OH)2 не реагирует с СО2, то мы записываем справа Zn(OH)2 без изменения.
2. Гидроксид цинка можно получить действием недостатка щелочи на избыток соли цинка.
Например , хлорид цинка реагирует с недостатком гидроксида калия с образованием гидроксида цинка и хлорида калия:
Химические свойства
1. Гидроксид цинка реагирует с растворимыми кислотами .
Например , гидроксид цинка взаимодействует с азотной кислотой с образованием нитрата цинка:
2. Гидроксид цинка взаимодействует с кислотными оксидами .
Например , гидроксид цинка взаимодействует с оксидом серы (VI) с образованием сульфата цинка:
3. Гидроксид цинка взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—цинкаты, а в растворе – комплексные соли . При этом гидроксид цинка проявляет кислотные свойства.
Например , гидроксид цинка взаимодействует с гидроксидом калия в расплаве с образованием цинката калия и воды:
Гидроксид цинка растворяется в избытке щелочи с образованием тетрагидроксоцинката:
4. Г идроксид цинка разлагается при нагревании :
Реакция взаимодействия цинка и гидроксида натрия
Реакция взаимодействия цинка и гидроксида натрия
Уравнение реакции взаимодействия цинка и гидроксида натрия:
Реакция взаимодействия цинка и гидроксида натрия.
В результате реакции образуются цинкат натрия и водород.
Реакция протекает при условии: при температуре около 550 °C.
Формула поиска по сайту: Zn + 2NaOH → Na2ZnO2 + H2.
Реакция взаимодействия оксида меди (I) и серной кислоты
Реакция разложения оксида азота (V)
Реакция взаимодействия фторида лития и гидроксида кальция
Выбрать язык
Популярные записи
Предупреждение.
Все химические реакции и вся информация на сайте предназначены для использования исключительно в учебных целях — только для решения письменных, учебных задач. Мы не несем ответственность за проведение вами химических реакций.
Химические реакции и информация на сайте
не предназначены для проведения химических и лабораторных опытов и работ.
Электронные и молекулярные уравнения реакций цинка и кадмия
Задание 393
Составьте электронные и молекулярные уравнения реакций цинка: а) с раствором гидроксида натрия; б) с концентрированной серной кислотой, учитывая восстановление серы до нулевой степени окисления.
Решение:
Уравнения реакций цинка
а) с раствором гидроксида натрия
Zn 0 + 2H + = Zn 2+ + H2 0
б) с концентрированной серной кислотой
3Zn 0 + S 6+ = 3Zn 2+ + S 0
Задание: 396
Составьте уравнения реакций, которые надо провести для осуществления следующих превращений:
Cd → Cd(NO3)2 → Cd(OH)2→ [Cd(NH3)6](OH)2→ CdSO4
Решение:
Уравнения реакций, которые надо провести для осуществления следующих превращений:
будут иметь вид:
Задание 398
К какому классу соединений относятся вещества, полученные при действии избытка гидроксида натрия на растворы ZnCl2, CdCl2, HgCl2? Составьте молекулярные и ионно-молекулярные уравнения соответствующих реакций.
Решение:
При действии на растворы ZnCl2 и CdCl2 избытка гидроксида натрия сначала образуются соответственно нерастворимые Zn(OH)2 и Cd(OH):
Осадок гидроксида цинка как амфотерное основание растворяется в избытке гидроксида натрия с образованием комплексного иона [Zn(OH)4] 2- :
Гидроксид кадмия в отличие от гидроксида цинка не обладает ярко выраженными амфотерными свойствами, поэтому в избытке гидроксида натрия не растворяется.
При действии щелочей на растворы солей Hg 2+ выделяется высокодисперсный жёлтый осадок HgO:
Задание 403
На гидроксиды цинка и кадмия подействовали избытком растворов серной кислоты, гидроксида натрия и аммиака. Какие соединения цинка и кадмия образуются в каждой из этих реакций? Составьте молекулярные и ионно-молекулярные уравнения ре-акций?
Решение:
Гидроксиды цинка и кадмия амфотерные соединения, только амфотерные свойства у Cd(OH)2 выражены слабее, чем у Zn(OH)2.
а) При действии кислот на Cd(OH)2 и Zn(OH)2 образуются соответствующие соли:
б) При действии сильного основания на Zn(OH)2 образуется комплексная соль Na2[Zn(OH)4]:
Амфотерные свойства у Cd(OH)2 выражены гораздо слабее, чем у Zn(OH)2, поэтому гидроксид кадмия в избытке щёлочи не растворяется, но при длительном кипячении в растворе щёлочи гидроксид кадмия растворяется с образованием гексагидроксокадмиат(II)-ионы [Сd(OH)6] 4- :
в) При действии избытком раствора аммиака на гидроксиды цинка и кадмия образуются комплексные соединения:
http://chemicalstudy.ru/reaktsiya-vzaimodejstviya-tsinka-i-gidroksida-natriya/
http://buzani.ru/zadachi/khimiya-shimanovich/989-tsink-i-kadmij-zadaniya-393-396-398-403