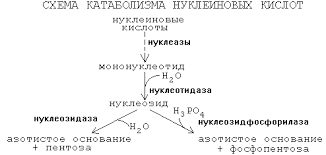
Гидролиз нуклеиновых кислот
Нуклеиновые кислоты способны гидролизоваться по трем механизмам: в кислой и щелочной среде, а также в присутствии ферментов. В первом случае гидролиз протекает частично и избирательно. Так, например, при гидролизе ДНК происходит разрыв связей между пуриновыми основаниями и моносахаридом дезоксирибозой и образуется ДНК, в составе которой нет пуриновых оснований.
В щелочной среде нуклеиновые кислоты гидролизуются полностью, но в несколько этапов: нуклеотиды → нуклеозиды → азотистые основания, моносахарид и ортофосфорная кислота.
Ферментативный гидролиз протекает под действием специальных энзимов – нуклеаз. Происходит разрыв конкретных химических связей.
Как известно, большая часть нуклеиновых кислот в клетке связана с белком в форме нуклеопротеинов. Поступающие с пищей нуклеопротеины разрушается панкреатическими ферментами, а нуклеопротеины ткани — лизосомальными ферментами. Вначале происходит диссоциация компонентов нуклеопротеинов на белки и нуклеиновые кислоты. Этому способствует кислая среда желудка. Белки затем включаются в обмен вместе с другими белками пищи, а нуклеиновые кислоты гидролизуются нуклеазами сока железы (РНКазами и ДНКазами), с образованием смеси полинуклеотидов. Далее в процесс включаются полинуклеотидазы и фосфодиэстеразы (эндонуклеазы) кишечника Они довершают гидролиз нуклеиновых кислот до мононуклеотидов. В кишечнике, как правило, образуются 3′-фосфат нуклеотиды, а под влиянием лизосомальных полинуклеотидаз образуются биологически важные 5′- фосфат нуклеотиды. Нуклеотиды гидролизуются нуклеотидазами, с образованием нуклеозидов и Фн. Нуклеозиды, которые обычно рассматриваются как конечный продукт переваривания нуклеиновых кислот в кишечнике, всасываются.
В клетках некоторых тканей, в том числе и клетках кишечника, нуклеозиды подвергаются фосфоролизу нуклеозид фосфорилазами, с образованием оснований и рибозы 1-Ф (или дезоксирибозы 1-P). Рибоза 1-Ф и рибоза 5-Ф в цитозоле находятся в равновесии и могут быть вновь использованы для синтеза нуклеотидов или вступают в неокислительную часть пенозофосфатного пути. Пуриновые и пиримидиновые основания также или распадаются далее до конечных продуктов или используются повторно для синтеза нуклеотидов. В клетке существует интенсивно обмениваемый пул рибонуклеотидов и РНК. Молекулы ДНК и пул дезоксирибонуклеотидов обменивается значительно медленнее. Тканевые пурины и пиримидины, которые не попадают в пути повторного использования, обычно распадаются и продукты их распада выделяются. Используется лишь очень небольшое количество пищевых пуринов, а основная масса поступивших с пищей пуринов распадается. Катаболизм пуринов и пиримидинов не сопровождается значительным высвобождением энергии в сравнении с обменом аминокислот, однако некоторые продукты распада выполняют определенные физиологические функции, например, конечный продукт катаболизма пуринов у человека мочевая кислота, может служить антиоксидантом, продукт катаболизма пиримидина, β– аланин используется в синтезе активных пептидов мозга и мышц. Парэнтеральное введение нуклеотидов и нуклеозидов нашло применение в исследовательской практике. Меченый 3Н –тимидин включается в синтезируемую ДНК без изменений и используется для введения метки в ДНК различных биологических объектов.
Реакции распада мочевой кислоты млекопитающих имеется фермент уратоксидаза которая превращает мочевую кислоту в более растворимый аллантоин. У человека нет такого фермента, и мочевая кислота, кото- рая образуется преимущественно в печени, выделяется почками как конечный продукт обмена пуриновых нуклеотидов. Превращение мочевой кислоты в аллантоин может протекать неферментативно. Эта реакция рассматривается как один из механизмов антиоксидантной защиты клетки у организмов, утративших способность синтезировать аскорбиновую кислоту, а мочевая кислота как важный антиоксидант, заменивший аскорбиновую кислоту. У некоторых животных аллантоин может распадаться далее до мочевины или аммиака. От нуклеотидов к основаниям. Гуаниновые нуклеотиды гидролизуются с образованием гуанозина, который подвергается фосфоролизу до гуанина и рибоза 1-Ф. Гуанин дезаминируется гуанин дезаминазой с образованием ксантина. Аденозин также можно получить по такому пути, однако внутриклеточные нуклеотидазы у человека не очень активны по отношению к AMФ. АМФ чаще дезаминируется ферментом аденилат (AMФ) дезаминазой с образованием ИМФ. Последний далее гидролизуется нуклеотидазой с образованием инозина и после фосфоролиза превращается в гипоксантин. Некоторое количество аденозина образуется из S -аденозилметионина в процессах переметилирования. Аденозин дезаминируется до инозина аденозин дезаминазой. Недостаточность аденозин дезаминазы или пуриновой нуклеозид фосфорилазы ведет к двум различным болезням иммунодефицита механизмами, которые до конца не раскрыты.
При недостаточности аденозин дезаминазы, страдают T и B-лимфоциты, а при недостаточности фосфорилазы нарушается функция T клеток, а B клетки остаются нормальными. В сентябре 1990 г была успешно применена генинженерная технология для лечения 4-летней девочки с недостаточностью аденозин дезаминазы. Катаболизм метилированных (минорных) пуринов зависит от расположения метильной группы. Если метильная группа связана с группой -NH2, она удаляется вместе с -NH2, и оставшаяся часть обменивается в дальнейшем обычным способом. Если метил связан с атомом азота гетероцикла, соединение выделяется в неизменном виде с мочой. От оснований к мочевой кислоте И адениновые и гуаниловые нуклеотиды превращаются в одно общее промежуточное соединение ксантин. Гипоксантин, возникающий из аденина, окисляется в ксантин ксантиноксидазой . Гуанин дезаминируется с образованием аммиака и ксантина. Образующийся аммиак переносится к печени в составе глутамина, где используется для синтеза мочевины. Ксантин, подобно гипоксантину, окисляется кислородом и ксантиноксидазой в мочевую кислоту с образованием перекиси водорода. У человека, мочевая кислота выделяется, а перекись водорода разрушается каталазой. Высокая активность ксантиноксидазы обнаруживается только в клетках печени и кишечника.
Нуклеиновые кислоты
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Описание презентации по отдельным слайдам:
План лекции
Сформировать представление о взаимосвязи химического строения и биологической роли нуклеиновых кислот
План лекции
Структурные компоненты нуклеиновых кислот;
Строение нуклеиновых оснований. Лактим-лактамная таутомерия;
Строение и химические свойства нуклеозидов;
Строение и химические свойства нуклеотидов;
Строение и биологическая роль АТФ, АДФ, АМФ;
Виды структур нуклеиновых кислот;
Медико-биологические свойства нуклеиновых кислот.
гетероциклическое
основание
(нуклеиновое)
сахар
O-P-O
O
OH
сахар
Структура нуклеиновых кислот
нуклеотид
гетероциклическое
основание
(нуклеиновое)
Классификация нуклеиновых оснований по характеру гетероцикла
пиримидиновые
Урацил (У)
Цитозин (Ц)
Тимин (Т)
пуриновые
Аденин (А)
Гуанин (Г)
Классификация таутомерии нуклеиновых оснований
Лактам-лактимная
Амино-иминная
Азольная
Лактам-лактимная таутомерия
H
H
:
:
лактамная форма
урацила
лактимная форма
урацила
2
1
3
4
5
6
2,4-дигидроксипиримидин
Минорные основания
Дигидро-
урацил
3-N-метил-
урацил
Лактам-лактимная таутомерия
лактамная форма
гуанина
лактимная форма
гуанина
1
2
3
4
5
6
7
8
9
2-амино-6-гидроксипурин
Таутомерия нуклеиновых оснований.
1) лактим-лактамная таутомерия
лактамная
форма
неполная
лактимная
форма
лактимная
форма
2,4-дигидрокси-
пиримидин
урацила
Таутомерия нуклеиновых оснований.
цитозина
лактамная
форма
лактимная
форма
4-амино-2-гидрокси-
пиримидин
Таутомерия нуклеиновых оснований.
1) лактим-лактамная таутомерия
Таутомерия нуклеиновых оснований.
2) амино-иминная таутомерия цитозина
амино-форма
имино-форма
Таутомерия нуклеиновых оснований.
3) Азольная таутомерия
9-Н гуанин
7-Н-гуанин
Нуклеозиды – это N-гликозиды,
образованные нуклеиновыми основаниями и
пентозой (рибозой или дезоксирибозой).
Классификация нуклеозидов
(в зависимости от природы углеводного остатка):
рибонуклеозиды
дезоксирибонуклеозиды
(в РНК)
(в ДНК)
Общая структурная формула нуклеозидов
пентоза в
фуранозной
форме
N-гликозидная
связь
Н- у дезоксирибозы
Пиримидиновые основания образуют нуклеозиды по положению 1.
Пуриновые основания образуют нуклеозиды по положению 9.
Гидролиз нуклеозидов
проходит по N-гликозидной связи.
N-Гликозидная связь устойчива в щелочной среде
и гидролизуется только в кислой среде.
Продукты гидролиза – нуклеиновое основание и моносахарид.
цитидин
b-D-рибо-
фураноза
цитозин
H2O, H
+
+
Нуклеозид с минорным основанием.
b-D-рибо-
фураноза
гипоксантин
ИНОЗИН
b-D-3-дезокси-
рибофураноза
b-D-арабиноза
кордицепин
Антибиотик,
получаемый из грибницы
Cordyceps militaris
противовирусное
средство
аденин
3’
2’
Нуклеотиды – сложные эфиры нуклеозидов и фосфорной кислоты (фосфаты нуклеозидов)
ГИДРОЛИЗ НУКЛЕОТИДОВ
1.Щелочной гидролиз (неполный) – только по
сложно-эфирной связи. Образуются нуклеозид и
соль фосфорной кислоты.
Тимидин-5’-фосфат
5’-тимидиловая кислота
NaOH
Тимидин
NaH2PO4
Дигидро-
фосфат
натрия
+
ГИДРОЛИЗ НУКЛЕОТИДОВ
2.Кислотный гидролиз (полный)– по сложно-эфирной и
гликозидной связям. Образуются фосфорная кислота,
пентоза и нуклеиновое основание.
Тимидин-5’-фосфат
5’-тимидиловая кислота
H3PO4
+
H2O, H+
b-D-дезоксирибо-
фураноза
Фосфорная
кислота
тимин
+
H3PO4
АМФ (аденозинмонофосфат)
АДФ (аденозиндифосфат)
H3PO4
АТФ (аденозинтрифосфат)
N-гликозидная
связь
сложноэфирная
связь
ангидридные
связи (макроэргические)
Биологическая роль АТФ
Участвует в реакциях фосфорелирования как
источник фосфатных групп.
2. Источник энергии для биохимических процессов.
3. Активация аминокислот при биосинтезе белка.
Первичная структура нуклеиновой кислоты-
это последовательность нуклеотидных звеньев,
связанных ковалентными связями в непрерывную
цепочку полинуклеотида.
Её определяют две характеристики:
1.Нуклеотидный состав -набор и соотношение нуклеотидов.
2.Нуклеотидная последовательность -порядок чередования
нуклеотидных звеньев.
Нуклеиновые кислоты – высокомолекулярные полимеры, мономерами которых являются нуклеотиды.
Вторичная структура нуклеиновых кислот – пространственная организация полинуклеотидных цепей, т.е. определенное расположение полинуклеотидной цепи в пространстве
А
Т
Пары комплементарных оснований
Пары комплементарных оснований
Г
Ц
Курс повышения квалификации
Охрана труда
- Сейчас обучается 115 человек из 42 регионов
Курс профессиональной переподготовки
Охрана труда
- Сейчас обучается 233 человека из 54 регионов
Курс профессиональной переподготовки
Библиотечно-библиографические и информационные знания в педагогическом процессе
- Сейчас обучается 351 человек из 63 регионов
Ищем педагогов в команду «Инфоурок»
Дистанционные курсы для педагогов
«Взбодрись! Нейрогимнастика для успешной учёбы и комфортной жизни»
Свидетельство и скидка на обучение каждому участнику
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
5 585 042 материала в базе
Самые массовые международные дистанционные
Школьные Инфоконкурсы 2022
33 конкурса для учеников 1–11 классов и дошкольников от проекта «Инфоурок»
Другие материалы
- 15.11.2020
- 1449
- 10
- 12.11.2020
- 116
- 0
- 06.11.2020
- 136
- 0
- 20.10.2020
- 89
- 0
- 20.10.2020
- 135
- 0
- 16.10.2020
- 132
- 1
- 26.09.2020
- 164
- 0
- 26.08.2020
- 521
- 5
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Добавить в избранное
- 12.11.2020 473
- PPTX 876.5 кбайт
- 1 скачивание
- Оцените материал:
Настоящий материал опубликован пользователем Федотова Наталья Ивановна. Инфоурок является информационным посредником и предоставляет пользователям возможность размещать на сайте методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайт
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Автор материала
- На сайте: 1 год и 1 месяц
- Подписчики: 0
- Всего просмотров: 24614
- Всего материалов: 203
Московский институт профессиональной
переподготовки и повышения
квалификации педагогов
Дистанционные курсы
для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы
установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
В Курганской области дистанционный режим для школьников продлили до конца февраля
Время чтения: 1 минута
Университет им. Герцена и РАО создадут портрет современного школьника
Время чтения: 2 минуты
В Забайкалье в 2022 году обеспечат интернетом 83 школы
Время чтения: 1 минута
Школьник из Сочи выиграл международный турнир по шахматам в Сербии
Время чтения: 1 минута
Инфоурок стал резидентом Сколково
Время чтения: 2 минуты
В Ростовской и Воронежской областях организуют обучение эвакуированных из Донбасса детей
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Лекция № 25 нуклеиновые кислоты (45 минут)
Лекция № 25
Нуклеиновые кислоты (45 минут)
1. Компоненты нуклеиновых кислот
а) азотистые основания
б) углеводы
в) фосфорная кислота
2. Нуклеозиды
3. Нуклеотиды
а) мононуклеотиды
б) олиго — и полинуклеотиды
4. Вторичная структура ДНК
5. Химические свойства нуклеиновых кислот.
а) кислотный гидролиз
б) щелочной гидролиз
в) ферментативный гидролиз
Нуклеиновые кислоты — это водорастворимые высокомолекулярные соединения, макромолекулы которых состоят из многократно повторяющихся звеньев — нуклеотидов. Поэтому их также называют полинуклеотидами.
Впервые они были обнаружены в 1868 году швейцарским врачом Мишером в ядрах погибших лейкоцитов, что и определило их название (от лат. nucleus — ядро).
По химическому строению нуклеиновые кислоты — биологические полимеры, состоящие из остатков фосфорной кислоты, моносахарида и одного из пуриновых или пиримидиновых гетероциклических оснований. Входящие в состав нуклеиновых кислот гетероциклические соединения пуринового и пиримидинового ряда называют нуклеиновыми основаниями или просто основаниями.
В общем виде молекулу нуклеиновой кислоты можно представить следующим образом:
Фрагмент макромолекулы нуклеиновой кислоты моносахарид-основание называется нуклеозидом, а фрагмент моносахарид-основание-фосфат — нуклеотидом.
Нуклеиновые кислоты присутствуют в клетках всех живых организмов и выполняют важнейшие функции по хранению, передаче и реализации наследственной информации.
Особенность нуклеиновых кислот заключается в том, что обычно «неделимое» мономерное звено в полинуклеотидах может быть разделено на составные части: нуклеотиды и нуклеозиды, которые помимо того, что служат строительными блоками при синтезе нуклеиновых кислот, играют и вполне самостоятельную роль в процессах обмена веществ, а также участвуют в качестве коферментов в реакциях переноса остатков сахаров, аминов и других биомолекул.
1. Компоненты нуклеиновых кислот
Азотистые основания.
В состав нуклеиновых кислот входят гетероциклические основания пиримидинового ряда: урацил, тимин, цитозин и пуринового ряда: аденин и гуанин.
Для удобства используют однобуквенные обозначения (символы) гетероциклических оснований (русские или латинские):
Пиримидиновые основания
Пуриновые основания
Нумерация атомов производится в указанном порядке. Отметим также, что в физиологических условиях нуклеиновые основания существуют только в лактамной и аминной формах. Во всех формах гетероциклы сохраняют ароматичность и имеют плоское строение, благодаря чему отличаются высокой термодинамической стабильностью.
Углеводы.
Углеводным компонентом нуклеиновых кислот являются пентозы: D-рибоза или 2-дезокси-D-рибоза. Обе пентозы всегда находятся в фуранозной форме и имеют β-конфигурацию аномерного атома С-1′ (в формулах нуклеотидов и нуклеозидов атомы углерода моносахаридов нумеруются цифрой со штрихом):
Фосфорная кислота.
Остатки фосфорной кислоты (H3PO4) входят в состав нуклеотидов и этерифицируют D-рибозу и 2-дезокси-D-рибозу в положениях 3′ и 5′. В этой связи нуклеотиды и полинуклеотиды можно рассматривать, с одной стороны, как сложные эфиры нуклеозидов (фосфаты), а с другой — как кислоты.
Остатки моносахаридов и фосфорной кислоты выполняют структурную функцию и являются носителями гетероциклических оснований.
2. Нуклеозиды
Нуклеозиды состоят из гетероциклических оснований, связанных с моносахаридом N-гликозидной связью. В образовании этой связи участвуют аномерный атом углерода моносахарида и атомы азота N-1 (у пиримидинового основания) и N-9 (у пуринового основания):
В зависимости от углеводного остатка нуклеозиды делятся на рибонуклеозиды и дезоксирибонуклеозиды. Номенклатурные названия нуклеозидов строятся аналогично названиям гликозидов, например, β-аденинрибофуранозид и т. д. Однако чаще используются названия с суффиксами — идин у пиримидиновых и — озин у пуриновых нуклеозидов и приставкой дезокси — у дезоксирибонуклеозидов:
цитозин + рибоза = цитидин;
цитозин + дезоксирибоза = дезоксицитидин;
аденин + рибоза = аденозин;
аденин + дезоксирибоза = дезоксиаденозин.
Исключением является название тимидин, используемое для дезокситимидина, входящего в состав ДНК.
Кроме того, нуклеозиды обозначают символами, производимыми от входящих в них оснований. В случае дезоксирибонуклеозидов перед символом ставят строчную букву д (лат. d). Символами удобно пользоваться при обозначении первичной структуры ДНК или РНК. Если речь идет только о ДНК, букву d обычно пропускают.
Нуклеозиды значительно лучше растворимы в воде, чем исходные азотистые основания. Подобно всем гликозидам, нуклеозиды устойчивы к действию щелочей, но при нагревании легко подвергаются кислотному гидролизу с разрывом гликозидной связи и образованием основания и пентозы:
Пиримидиновые нуклеозиды значительно более устойчивы к гидролизу, чем пуриновые. В условиях in vivo гидролиз обоих типов нуклеозидов осуществляется при помощи специфических ферментов, называемых нуклеозидазами.
Нуклеотиды
Нуклеотиды — это производные нуклеозидов, которые образуются в результате этерификации пентозного фрагмента фосфорной кислотой. В зависимости от строения пентозы различают рибонуклеотиды (мономерные звенья РНК) и дезоксирибинуклеотиды (мономерные звенья ДНК).
В 2-дезоксирибозе имеются только два положения, по которым может образовываться сложноэфирная связь — а именно 3′- и 5′-положения. В случае рибонуклеотидов фосфатная группа может находиться в положениях 2′, 3′ и 5′. В биологических системах встречаются нуклеотиды всех типов, однако наиболее распространены нуклеозид-5′-фосфаты. За счет фосфатного остатка нуклеотиды проявляют свойства кислот и в физиологических условиях (pH ≈ 7) находятся в практически полностью ионизированном состоянии.
Мононуклеотиды.
Мононуклеотиды — это повторяющиеся мономерные единицы олигонуклеотидов и полинуклеотидов.
Нуклеозидмонофосфаты.
Нуклеозидмонофосфаты содержат только один остаток фосфорной кислоты. Например:
Для мононуклеотидов также используют два вида названий (табл. 3.), отражающих их принадлежность как к сложным эфирам, так и к кислотам. В первом случае название включает наименование нуклеозида с указанием положения в нем фосфатного остатка: аденозин-5′-фосфат*, уридин-5′-фосфат и т. д. Широко используются и тривиальные названия, имеющие окончание «-овая кислота», например, 5′-Уридиловая кислота.
Для удобства введены сокращения: трехбуквенные — АМФ (лат. AMP), УМФ (лат. UMP) и т. д. и однобуквенные — pA, pU и т. д. В биохимической литературе встречаются как русские, так и латинские обозначения, однако более широко используются латинские. Сокращения AMP, GMF и т. д. всегда относятся к 5′-нуклеотидам. У других, например, 3′-производных в сокращенном названии указывается положение фосфатной группы: 3′-AMP, 3′-GMP и т. д.
* вместо «монофосфат» часто пишут просто «фосфат».
В однобуквенных кодах 5′-фосфаты записываются с добавлением латинской буквы «p» перед символом нуклеозида (pA), 3′-фосфаты — после символа нуклеозида (Ap).
Важнейшие нуклеотиды, входящие в состав нуклеиновых кислот.
Входящие в состав РНК
Входящие в состав ДНК
Сложноэфирные связи с фосфатными остатками в мононуклеотидах относительно устойчивы к кислотному гидролизу. Однако фермент 5′-нуклеотидаза способен отщеплять фосфатную группу в положении 5′, не затрагивая при этом N-гликозидную связь.
Нуклеозидмоноциклофосфаты.
Существуют нуклеотиды, в которых фосфорная кислота одновременно этерифицирует две гидроксильные группы пентозного остатка с образованием устойчивого шестичленного цикла. В этой связи в их названиях используют приставку цикло-, например, циклоаденозин-монофосфат (cAMP) или циклогуанозинмонофосфат (cGMP). Эти два нуклеозидциклофосфата присутствуют практически во всех клетках живых организмов:
Биологическая роль циклических нуклеотидов была открыта сравнительно недавно. Так, аденозин-3′, 5′-циклофосфат выполняет роль внутриклеточного «посредника» в процессах, индуцируемых гормоном адреналином.
Нуклеозид-5′-дифосфаты (НДФ) и нуклеозид-5′-трифосфаты (НТФ).
Во всех тканях организма в свободном состоянии содержатся не только моно-, но и ди-, а также трифосфаты нуклеозидов. Наиболее известными являются аденозин-5′-дифосфат (АДФ) аденозин-5′-трифосфат (АТФ).
Нуклеотиды, фосфорилированные в разной степени, способны к взаимопревращениям путем наращивания или отщепления фосфатных групп. Дифосфатная группа содержит одну, а трифосфатная — две ангидридные связи, называемые макроэргическими, поскольку они обладают большим запасом энергии. При расщеплении макроэргической связи Р — О выделяется энергия, приблизительно равная 32 кДж/моль. Этим объясняется важнейшая роль АТФ как «поставщика» энергии во всех живых клетках.
Ангидридные связи могут гидролизоваться либо специфичными ферментами, либо при кипячении в присутствии HCl. Ни сложноэфирная связь, ни N-гликозидная при этом не расщепляются.
Взаимные превращения АМФ, АДФ и АТФ.
Олиго — и полинуклеотиды.
Олигонуклеотидами называют соединения, в которых несколько нуклеозидов (до 20) соединены между собой фосфодиэфирными связями. Нуклеозид со свободной 5′-OH-групой называется
5′-концевым, а со свободной 3′-OH-групой — 3′-концевым.
Полинуклеотиды представляют собой линейные гетерополимеры, также состоящие из последовательности мононуклеозидных единиц, соединенных фосфатным мостиком. Полинуклеотиды, состоящие из ковалентно связанных между собой остатков дезоксирибонуклеозидов, называются дезоксирибонуклеиновыми кислотами (ДНК), а полинуклеотиды, состоящие из остатков рибонуклеозидов — рибонуклеиновыми кислотами (РНК). В обоих случаях мононуклеозиды связаны между собой при помощи фосфодиэфирных мостиков, соединяющих 3′-положение одного мононуклеотида с 5′-положением его соседа.
Нуклеиновые кислоты также различаются и по составу входящих в них гетероциклических оснований: урацил входит только в состав РНК, а тимин — только в состав ДНК. Аденин, цитозин и гуанин являются постоянными компонентами полинуклеотидов.
Молекулярная масса ДНК достигает десятков миллионов. Это самые длинные из известных макромолекул. Значительно меньше молекулярная масса РНК (от нескольких сотен до десятков тысяч). ДНК содержатся в основном в ядрах клеток, РНК — в рибосомах и протоплазме клеток.
Первичная структура нуклеиновых кислот.
Первичная структура нуклеиновых кислот — это нуклеотидный состав и определенная последовательность нуклеотидных звеньев в полимерной цепи..
Для записи первичной структуры ДНК и РНК используют однобуквенные обозначения нуклеозидов. Приведенные фрагменты ДНК и РНК записывают соответственно: d(A-C-G-T) и (A-C-G-U). Часто букву d опускают, если речь идет о ДНК.
Первичная структура цепи ДНК и РНК.
Нуклеотидный состав ДНК различного происхождения находится в соответствии с правилами Э. Чаргаффа:
1) Все ДНК независимо от их происхождения содержат одинаковое число пуриновых и пиримидиновых оснований. Следовательно, в любой ДНК на каждый пуриновый нуклеотид приходится один пиримидиновый.
2) Любая ДНК всегда содержит в равных количествах попарно аденин и тимин, гуанин и цитозин, что обычно обозначают как А = Т и G = C.
3) Количество оснований, содержащих аминогруппы в положении 4 пиримидинового ядра и 6 пуринового (цитозин и аденин), равно количеству оснований, содержащих оксо-группу в тех же положениях (гуанин и тимин), т. е. A + C=G + T.
Наряду с этим было установлено, что для каждого типа ДНК суммарное содержание гуанина и цитозина не равно суммарному содержанию аденина и тимина, т. е. что (G + C)/(A + T), как правило, отличается от единицы (может быть как больше, так и меньше ее). По этому признаку различают два основных типа ДНК: А-Т-тип с преимущественным содержанием аденина и тимина и G-C-тип с преимущественным содержанием гуанина и цитозина.
Для РНК правила Чаргаффа либо не выполняются, либо выполняются с большим приближением.
Вторичная структура нуклеиновых кислот.
Под вторичной структурой нуклеиновых кислот понимают пространственно упорядоченные формы полинуклеотидных цепей.
Вторичная структура ДНК представляет собой две параллельные неразветвленные полинуклеотидные цепи, закрученные вокруг общей оси в двойную спираль.
Вторичная структура ДНК.
Такая пространственная структура удерживается множеством водородных связей, образуемых азотистыми основаниями, направленными внутрь спирали. Эти основания составляют комплементарные пары (от лат. complementum — дополнение). Образование водородных связей между комплементарными парами оснований обусловлено их пространственным соответствием. Так, пиримидиновое основание комплементарно пуриновому:
Водородные связи между другими парами оснований не возникают по пространственным причинам. Таким образом, в ДНК:
ТИМИН (Т) комплементарен АДЕНИНУ (А)
ЦИТОЗИН (C) комплементарен ГУАНИНУ (G)
Комплементарность оснований определяет комплементарность цепей в молекулах ДНК. Водородные связи возникают между пуриновым основанием одной цепи и пиримидиновым основанием другой цепи. Иными словами, пуриновым основаниям аденину и гуанину в одной цепи будут соответствовать пиримидиновые основания тимин и цитозин в другой цепи.
Таким образом, полинуклеотидные цепи, образующие двойную спираль, не идентичны, но комплементарны между собой:
В сдвоенной молекуле ДНК суммарно число групп А равно числу групп Т, а число групп G — числу C.
Комплементарность полинуклеотидных цепей служит химической основой главной функции ДНК — хранения и передачи наследственных признаков. Способность ДНК не только хранить, но и использовать генетическую информацию определяется следующими ее свойствами:
1) Молекулы ДНК способны к репликации (удвоению), т. е. могут обеспечить возможность синтеза других молекул ДНК, идентичных исходным, поскольку последовательность оснований в одной из цепей двойной спирали контролирует их расположение в другой цепи;
2) Молекулы ДНК могут совершенно точным и определенным образом направлять синтез белков, специфичных для организмов данного вида.
Вторичная структура РНК.
В отличие от ДНК, молекулы РНК состоят из одной полинуклеотидной цепи и не имеют строго определенной пространственной формы (рис. 3.), т. к. вторичная структура РНК зависит от их биологических функций. Полимерная цепь РНК приблизительно в десять раз короче, чем у ДНК.
Комплементарными парами в РНК являются цитозин-гуанин и урацил-аденин.
Вторичная структура РНК.
Основная роль РНК — непосредственное участие в биосинтезе белка. Известны три вида клеточных РНК, которые отличаются по местоположению в клетке, составу, размерам и свойствам, определяющим их специфическую роль в образовании белковых макромолекул:
1) Информационные (матричные) РНК передают закодированную в ДНК информацию о структуре белка от ядра клетки к рибосомам, где и осуществляется синтез белка;
2) Транспортные РНК собирают аминокислоты в цитоплазме клетки и переносят их в рибосому; молекулы РНК этого типа «узнают» по соответствующим участкам цепи информационной РНК, какие аминокислоты должны участвовать в синтезе белка;
3) Рибосомные РНК обеспечивают синтез белка определенного строения, считывая информацию с информационной (матричной) РНК.
Химические свойства нуклеиновых кислот.
ДНК и РНК имеют много общих химических и физических свойств. Так, нуклеиновые кислоты хорошо растворимы в воде и плохо растворяются в водных растворах кислот. Существенные различия ДНК и РНК связаны, в основном, с их отношением к гидролизу.
Гидролиз в кислой среде.
Мягкий кислотный гидролиз ДНК оказывает весьма избирательное действие: он приводит к расщеплению N-гликозидных связей между пуриновыми основаниями и дезоксирибозой, связи пиримидин-дезоксирибоза при этом не затрагиваются. В результате образуется ДНК, лишенная пуриновых оснований. Гидролиз РНК, проводимый в аналогичных условиях, приводит к образованию пуриновых оснований и пиримидиновых нуклеозид-2′(3′)-фосфатов.
Кислотный гидролиз в жестких условиях, приводит к разрыву всех N-гликозидных связей как ДНК, так и РНК и образованию смеси пуриновых и пиримидиновых оснований.
Гидролиз в щелочной среде.
В щелочной РНК легко гидролизуются до нуклеотидов, которые в свою очередь, расщепляются с образованием нуклеозидов и остатков фосфорной кислоты. ДНК, в отличие от РНК, устойчивы к щелочному гидролизу.
Ферментативный гидролиз.
Гидролиз ДНК и РНК также протекает и при участии специфических ферментов — нуклеаз. Эти ферменты избирательно действуют на 3′- и 5′-сложноэфирные связи. Так, фосфодиэстераза, выделенная из яда змей, расщепляет все 3′-связи как в ДНК, так и в РНК с образованием нуклеозид-5′-фосфатов. Фосфодиэстераза, выделенная из селезенки быка, наоборот, гидролизует только 5′-связи и высвобождает только нуклеозид-3′-фосфаты. Известны дезокси-рибонуклеазы, расщепляющие связи только между определенными парами мононуклеотидов — их используют для направленного гидролиза РНК.
Гидролиз ДНК И РНК проводят, в основном, для установления их нуклеотидного состава. Далее выделенные смеси анализируют с использованием хроматографических и спектральных методов анализа, а также электрофореза.
http://infourok.ru/nukleinovye-kisloty-4776457.html
http://pandia.ru/text/80/456/45330.php