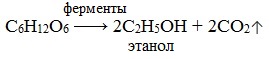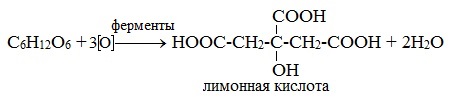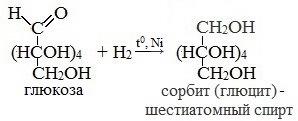Этанол: химические свойства и получение
Этанол C2H5OH или CH3CH2OH, этиловый спирт – это органическое вещество, предельный одноатомный спирт .
Общая формула предельных нециклических одноатомных спиртов: CnH2n+2O.
Строение этанола
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
| Атом кислорода в спиртах находится в состоянии sp 3 -гибридизации. |
В образовании химических связей с атомами C и H участвуют две 2sp 3 -гибридные орбитали, а еще две 2sp 3 -гибридные орбитали заняты неподеленными электронными парами атома кислорода.
Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108 о .
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому этанол – жидкость с относительно высокой температурой кипения (температура кипения этанола +78 о С).
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Этанол смешивается с водой в любых соотношениях.
Изомерия спиртов
Структурная изомерия
Для этанола характерна структурная изомерия – межклассовая изомерия.
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Спирты являются межклассовыми изомерами с простыми эфирами. Общая формула и спиртов, и простых эфиров — CnH2n+2О.
| Например. Межклассовые изомеры с общей формулой С2Н6О этиловый спирт СН3–CH2–OH и диметиловый эфир CH3–O–CH3 |
| Этиловый спирт | Диметиловый эфир |
| СН3–CH2–OH | CH3–O–CH3 |
Химические свойства этанола
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
1. Кислотные свойства
| Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды. |
1.1. Взаимодействие с раствором щелочей
При взаимодействии этанола с растворами щелочей реакция практически не идет, т. к. образующийся алкоголят почти полностью гидролизуется водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому этанол не взаимодействуют с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Этанол взаимодействует с активными металлами (щелочными и щелочноземельными).
| Например, этанол взаимодействует с калием с образованием этилата калия и водорода . |
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
| Например, этилат калия разлагается водой: |
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
| Например, этанол реагирует с бромоводородом. |
2.2. Взаимодействие с аммиаком
Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на катализаторе.
| Например, при взаимодействии этанола с аммиаком образуется этиламин. |
2.3. Этерификация (образование сложных эфиров)
Одноатомные и многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
| Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты): |
2.4. Взаимодействие с кислотами-гидроксидами
Спирты взаимодействуют и с неорганическими кислотами, например, азотной или серной.
| Например, при взаимодействии этанола с азотной кислотой образуется сложный эфир этилнитрат : |
3. Реакции замещения группы ОН
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. Процесс дегидратации протекает по двум возможным направлениям: внутримолекулярная дегидратация и межмолекулярная дегидратация.
3.1. Внутримолекулярная дегидратация
При высокой температуре (больше 140 о С) происходит внутримолекулярная дегидратация и образуется соответствующий алкен.
| Например, из этанола под действием концентрированной серной кислоты при температуре выше 140 градусов образуется этилен: |
В качестве катализатора этой реакции также используют оксид алюминия.
3.2. Межмолекулярная дегидратация
При низкой температуре (меньше 140 о С) происходит межмолекулярная дегидратация по механизму нуклеофильного замещения: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
| Например, при дегидратации этанола при температуре до 140 о С образуется диэтиловый эфир: |
4. Окисление этанола
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
| При окислении первичных спиртов они последовательно превращаются сначала в альдегиды, а потом в карбоновые кислоты. Глубина окисления зависит от окислителя. Первичный спирт → альдегид → карбоновая кислота |
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
4.1. Окисление оксидом меди (II)
Cпирты можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества.
| Например, этанол окисляется оксидом меди до уксусного альдегида |
4.2. Окисление кислородом в присутствии катализатора
Cпирты можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.).
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) первичные спирты окисляются до карбоновых кислот.
| Например, при взаимодействии этанола с перманганатом калия в серной кислоте образуется уксусная кислота |
4.4. Горение спиртов
Образуются углекислый газ и вода и выделяется большое количество теплоты.
| Например, уравнение сгорания этанола: |
5. Дегидрирование этанола
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования.
| Например, при дегидрировании этанола образуется этаналь |
Получение этанола
1. Щелочной гидролиз галогеналканов
При взаимодействии галогеналканов с водным раствором щелочей образуются спирты. Атом галогена в галогеналкане замещается на гидроксогруппу.
| Например, при нагревании хлорэтана с водным раствором гидроксида натрия образуется этанол |
2. Гидратация алкенов
Гидратация (присоединение воды) алкенов протекает в присутствии минеральных кислот. При присоединении воды к алкенам образуются спирты.
| Например, при взаимодействии этилена с водой образуется этиловый спирт. |
3. Гидрирование карбонильных соединений
Присоединение водорода к альдегидам и кетонам протекает при нагревании в присутствии катализатора. При гидрировании альдегидов образуются первичные спирты, при гидрировании кетонов — вторичные спирты, а из формальдегида образуется метанол.
| Например, при гидрировании этаналя образуется этанол |
4. Получение этанола спиртовым брожением глюкозы
Для глюкозы характерно ферментативное брожение, то есть распад молекул на части под действием ферментов. Один из вариантов — спиртовое брожение.
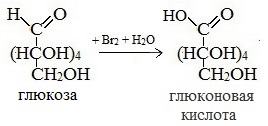
Глюкоза с этанолом уравнение реакции
Химические свойства глюкозы, как и других альдоз, обусловлены присутствием в ее молекуле: а)альдегидной группы; б) спиртовых гидроксилов; в) полуацетального (гликозидного) гидроксила.
Специфические свойства
1. Брожение (ферментация) моносахаридов
Важнейшим свойством моносахаридов является их ферментативное брожение, т.е. распад молекул на осколки под действием различных ферментов. Брожению подвергаются в основном гексозы в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента различают реакции следующих видов:
1) Спиртовое брожение
2) Молочнокислое брожение
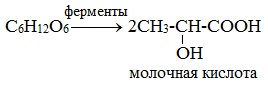
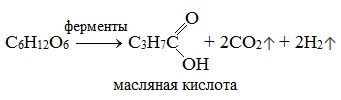
3) Маслянокислое брожение
4) Лимоннокислое брожение
Реакции с участием альдегидной группы глюкозы (свойства глюкозы как альдегида)
1. Восстановление (гидрирование) с образованием многоатомного спирта
В ходе этой реакции карбонильная группа восстанавливается и образуется новая спиртовая группа:
Cорбит содержится во многих ягодах и фруктах, особенно много сорбита в плодах рябины.
2. Окисление
1) Окисление бромной водой
Качественные реакции на глюкозу как альдегид!
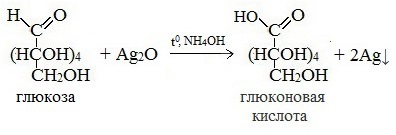
Протекающие в щелочной среде при нагревании реакции с аммиачным раствором Ag2O (реакция серебряного зеркала») и с гидроксидом меди (II) Cu (OH)2 приводят к образованию смеси продуктов окисления глюкозы.
2) Реакция серебряного зеркала
Соль этой кислоты – глюконат кальция – известное лекарственное средство.
Видеоопыт «Качественная реакция глюкозы с аммиачным раствором оксида серебра (I)»
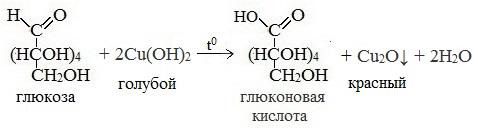
3) Окисление гидроксидом меди (II)
В ходе этих реакций альдегидная группа – СНО окисляется до карбоксильной группы – СООН.
Реакции глюкозы с участием гидроксильных групп (свойства глюкозы как многоатомного спирта)
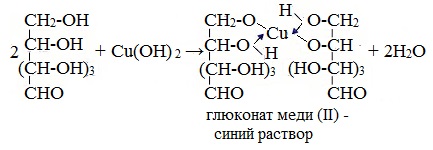
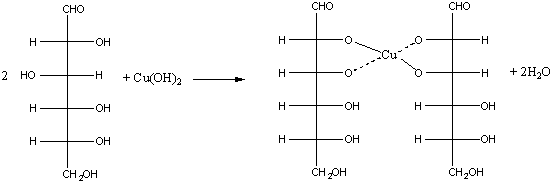
1. Взаимодействие с Cu (ОН)2 с образованием глюконата меди (II)
Качественная реакция на глюкозу как многоатомный спирт!
Подобно этиленгликолю и глицерину, глюкоза способна растворять гидроксид меди (II), образуя растворимое комплексное соединение синего цвета:
Прильём к раствору глюкозы несколько капель раствора сульфата меди (II) и раствор щелочи. Осадка гидроксида меди не образуется. Раствор окрашивается в ярко-синий цвет.
В данном случае глюкоза растворяет гидроксид меди (II) и ведет себя как многоатомный спирт, образуя комплексное соединение.
Видеоопыт «Качественная реакция глюкозы с гидроксидом меди (II)»
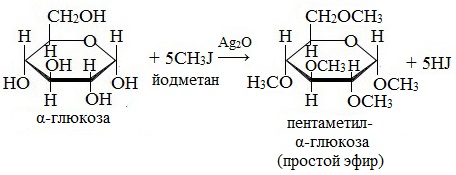
2. Взаимодействие с галогеналканами с образованием простых эфиров
Являясь многоатомным спиртом, глюкоза образует простые эфиры:
Реакция происходит в присутствии Ag2O для связывания выделяющегося при реакции НI.
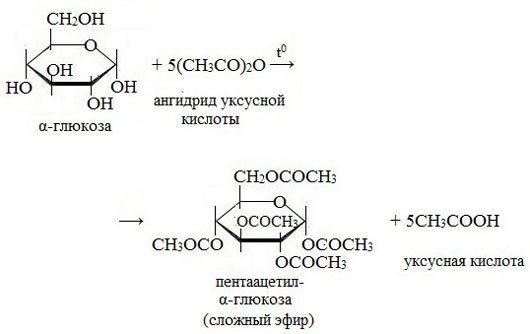
3. Взаимодействие с карбоновыми кислотами или их ангидридами с образованием сложных эфиров.
Например, с ангидридом уксусной кислоты:
Реакции с участием полуацетального гидроксила
1. Взаимодействие со спиртами с образованием гликозидов
Гликозиды – это производные углеводов, у которых гликозидный гидроксил замещен на остаток какого-либо органического соединения.
Содержащийся в циклических формах глюкозы полуацетальный (гликозидный) гидроксил является очень реакционноспособным и легко замещается на остатки различных органических соединений.
В случае глюкозы гликозиды называются глюкозидами. Связь между углеводным остатком и остатком другого компонента называется гликозидной.
Гликозиды построены по типу простых эфиров.
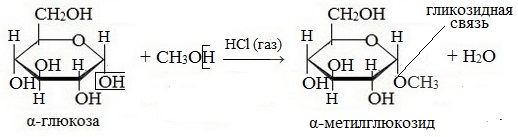
При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу:
В данных условиях в реакцию вступает только гликозидный гидроксил, спиртовые гидроксильные группы в реакции не участвуют.
Гликозиды играют чрезвычайно важную роль в растительном и животном мире. Существует огромное число природных гликозидов, в молекулах которых с атомом С (1) глюкозы остатки самых различных соединений.
Реакции окисления
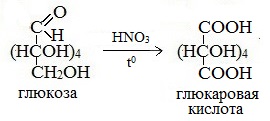
Более сильный окислитель – азотная кислота НNO3 – окисляет глюкозу до двухосновной глюкаровой (сахарной) кислоты:
В ходе этой реакции и альдегидная группа – СНО и первичная спиртовая группа — СН2ОН окисляются до карбоксильных – СООН.
Видеоопыт «Окисление глюкозы кислородом воздуха в присутствии метеленового голубого»
Химические свойства глюкозы.
Химические свойства моносахаридов обусловлены особенностями их строения.
Рассмотрим химические свойства на примере глюкозы.
Моносахариды проявляют свойства спиртов и карбонильных соединений.
I. Реакции по карбонильной группе
а) Как и у всех альдегидов, окисление моносахаридов приводит к соответствующим кислотам. Так, при окислении глюкозы аммиачным раствором гидрата окиси серебра образуется глюконовая кислота (реакция «серебряного зеркала»).
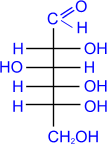 D- глюкоза D- глюкоза | + 2[Ag(NH3)2]OH → | 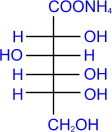 аммониевая соль D- глюконовой кислоты аммониевая соль D- глюконовой кислоты | + 2Ag↓ + 3NH3↑+ H2O |
Эти реакции являются качественными на глюкозу как альдегид.
Соль глюконовой кислоты – глюконат кальция – известное лекарственное средство.
б) Реакция моносахаридов с гидроксидом меди при нагревании так же приводит к альдоновым кислотам.
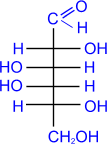 D- галактоза D- галактоза | + 2Cu(OH)2 → | 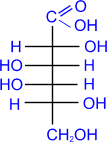 D- галактоновая кислота D- галактоновая кислота | + Cu2O↓ + 2H2O |
Эти реакции являются качественными на глюкозу как альдегид.
в) Более сильные окислительные средства окисляют в карбоксильную группу не только альдегидную, но и первичную спиртовую группы, приводя к двухосновным сахарным (альдаровым) кислотам. Обычно для такого окисления используют концентрированную азотную кислоту.
 D- глюкоза D- глюкоза | HNO3(конц.) –––––––→ | 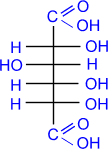 сахарная (D- глюкаровая) кислота сахарная (D- глюкаровая) кислота |
Восстановление сахаров приводит к многоатомным спиртам. В качестве восстановителя используют водород в присутствии никеля, алюмогидрид лития и др.
 D- глюкоза D- глюкоза | LiAlH4 + H2 ––––→ | 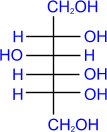 D- сорбит D- сорбит |
3. Несмотря на схожесть химических свойств моносахаридов с альдегидами, глюкоза не вступает в реакцию с гидросульфитом натрия (NaHSO3).
II. Реакции по гидроксильным группам
Реакции по гидроксильным группам моносахаридов осуществляются, как правило, в полуацетальной (циклической) форме.
1. Алкилирование (образование простых эфиров).
При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу.
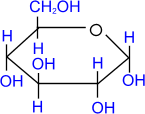 , D- глюкопираноза , D- глюкопираноза | + СH3ОН | HCl(газ) ––––→ | 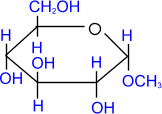 метил-α, D- глюкопиранозид метил-α, D- глюкопиранозид | + H2О |
При использовании более сильных алкилирующих средств, каковыми являются, например, йодистый метил или диметилсульфат, подобное превращение затрагивает все гидроксильные группы моносахарида.
 | СH3I ––––→ NaOH | 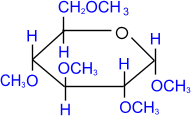 пентаметил-α, D- глюкопираноза пентаметил-α, D- глюкопираноза |
2. Ацилирование (образование сложных эфиров).
При действии на глюкозу уксусного ангидрида образуется сложный эфир – пентаацетилглюкоза.
 | 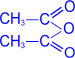 ––––––––→ ––––––––→ | 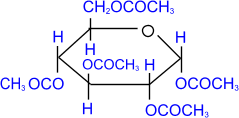 пентаацетил-α,D- глюкопираноза пентаацетил-α,D- глюкопираноза |
3. Как и все многоатомные спирты, глюкоза с гидроксидом меди (II) на холоду с образованием глюконата меди (II) дает интенсивное синее окрашивание – качественная реакция на глюкозу как многоатомный спирт.
ярко синий раствор
III. Специфические реакции
1. Горение (а также полное окисление в живом организме):
C6H12O6 + 6O2 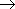
2. Реакции брожения
Кроме приведенных выше, глюкоза характеризуется и некоторыми специфическими свойствами — процессами брожения. Брожением называется расщепление молекул сахаров под воздействием ферментов (энзимов). Брожению подвергаются сахара с числом углеродных атомов, кратным трем. Существует много видов брожения, среди которых наиболее известны следующие:
а) спиртовое брожение
б) молочнокислое брожение
| C6H12O6 → 2CH3– | CH–СОOH(молочная кислота) | OH |
в) маслянокислое брожение
Упомянутые виды брожения, вызываемые микроорганизмами, имеют широкое практическое значение. Например, спиртовое – для получения этилового спирта, в виноделии, пивоварении и т.д., а молочнокислое – для получения молочной кислоты и кисломолочных продуктов.
Фруктоза вступает во все реакции, характерные для многоатомных спиртов, однако реакции альдегидной группы, в отличие от глюкозы, для нее не характерны.
Химические свойства рибозы C5H10O5 аналогичны глюкозе.
Д) Биологическая роль глюкозы.
D-глюкоза (виноградный сахар) широко распространена в природе: содержится в винограде и других плодах, в меде. Она является обязательным компонентом крови и тканей животных и непосредственным источником энергии для клеточных реакций. Уровень глюкозы в крови человека постоянен и находится в пределах 0,08-0,11%. Во всем объеме крови взрослого человека содержится 5-6 г. глюкозы. Такого количества достаточно для покрытия энергетических затрат организма в течение 15 мин. его жизнедеятельности. При некоторых патологиях, например, при заболевании сахарным диабетом, содержание глюкозы в крови повышается, и избыток её выводится с мочой. При этом количество глюкозы в моче может возрасти до 12% против обычного – 0,1%.
3. Дисахариды.
Олигосахариды — углеводы, молекулы которых содержат от 2 до 8-10 остатков моносахаридов, соединенных гликозидными связями. В соответствии с этим различают дисахариды, трисахариды и т. д.
Дисахариды — сложные сахара, каждая молекула которых при гидролизе распадается на две молекулы моносахаридов. Дисахариды наряду с полисахаридами являются одним из основных источников углеводов в пище человека и животных. По своему строению дисахариды являются гликозидами, в которых две молекулы моносахаридов соединены гликозидной связью.
Строение
1. Молекулы дисахаридов могут содержать два остатка одного моносахарида или два остатка разных моносахаридов;
2. Связи, образующиеся между остатками моносахаридов, могут быть двух типов:
а) в образовании связи принимают участие полуацетальные гидроксилы обеих молекул моносахаридов. Например, образование молекулы сахарозы;
б) в образовании связи принимают участие полуацетальный гидроксил одного моносахарида и спиртовый гидроксил другого моносахарида. Например, образование молекул мальтозы, лактозы и целлобиозы.
Для установления строения дисахаридов необходимо знать: из каких моносахаридов он построен, какова конфигурация аномерных центров у этих моносахаридов (- или -), каковы размеры цикла (фураноза или пираноза) и с участием каких гидроксилов связаны две молекулы моносахарида.
Дисахариды подразделяются на две группы: восстанавливающие и невосстанавливающие.
Среди дисахаридов особенно широко известны мальтоза, лактоза и сахароза.
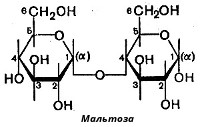
Мальтоза (солодовый сахар), являющаяся α-глюкопиранозил-(1-4)-α-глюкопиранозой, образуется в качестве промежуточного продукта при действии амилаз на крахмал (или гликоген), содержит два остатка α-D-глюкозы. Название сахара, чей полуацетальный гидроксил участвует в образовании гликозидной связи, оканчивается на «ил».
В молекуле мальтозы у второго остатка глюкозы имеется свободный полуацетальный гидроксил. Такие дисахариды обладают восстанавливающими свойствами.
К восстанавливающим дисахаридам относится, в часности, мальтоза (солодовый сахар), содержащаяся в солоде, т.е. проросших, а затем высушенных и измельченных зернах хлебных злаков.
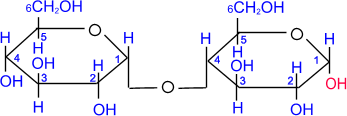
Мальтоза составлена из двух остатков D- глюкопиранозы, которые связаны (1–4) -гликозидной связью, т.е. в образовании простой эфирной связи участвуют гликозидный гидроксил одной молекулы и спиртовой гидроксил при четвертом атоме углерода другой молекулы моносахарида. Аномерный атом углерода (С1), участвующий в образовании этой связи, имеет - конфигурацию, а аномерный атом со свободным гликозидным гидроксилом (обозначен красным цветом) может иметь как α- (α- мальтоза), так и β- конфигурацию (β- мальтоза).
Мальтоза представляет собой белые кристаллы, хорошо растворимые в воде, сладкие на вкус, однако значительно меньше, чем у сахара (сахарозы).
Как видно, в мальтозе имеется свободный гликозидный гидроксил, вследствие чего сохраняется способность к раскрытию цикла и переходу в альдегидную форму. В связи с этим, мальтоза способна вступать в реакции, характерные для альдегидов, и, в частности, давать реакцию «серебряного зеркала», поэтому ее называют восстанавливающим дисахаридом. Кроме того, мальтоза вступает во многие реакции, характерные для моносахаридов, например, образует простые и сложные эфиры.
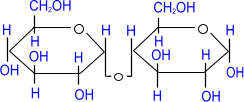 | СH3I ––––→ NaOH | 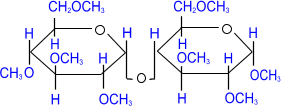 |
| мальтоза | Октаметилмальтоза |
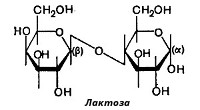
Дисахарид лактоза (молочный сахар) содержится только в молоке и состоит из D-галактозы и D-глюкозы. Это — α-глюкопиранозил-(1-4)-глюкопираноза:
Поскольку в молекуле лактозы имеется свободный полуацетальный гидроксил (в остатке глюкозы), она принадлежит к числу редуцирующих дисахаридов.
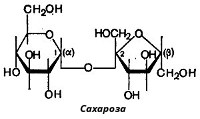
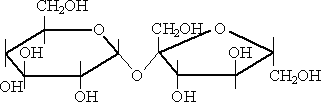
Одним из наиболее распространенных дисахаридов является сахароза (тростниковый или свекольный сахар) − обычный пищевой сахар. Молекула сахарозы состоит из одного остатка D-глюкозы и одного остатка D-фруктозы. Следовательно, это − α-глюкопиранозил-(1-2)-β-фруктофуранозид:
В отличие от большинства дисахаридов сахароза не имеет свободного полуацетального гидроксила и не обладает восстанавливающими свойствами.
К невосстанавливающим дисахаридам относится сахароза (свекловичный или тростниковый сахар). Она содержится в сахарном тростнике, сахарной свекле (до 28% от сухого вещества), соках растений и плодах. Молекула сахарозы построена из α, D- глюкопиранозы и β, D- фруктофуранозы.
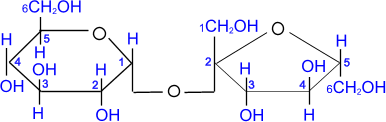
В противоположность мальтозе гликозидная связь (1–2) между моносахаридами образуется за счет гликозидных гидроксилов обеих молекул, то есть свободный гликозидный гидроксил отсутствует. Вследствие этого отсутствует восстанавливающая способность сахарозы, она не дает реакции «серебряного зеркала», поэтому ее относят к невосстанавливающим дисахаридам.
Среди природных трисахаридов важное значение имеют немногие. Наиболее известна рафиноза, содержащая остатки фруктозы, глюкозы и галактозы, которая находится в больших количествах в сахарной свекле и во многих других растениях.
В целом олигосахариды, присутствующие в растительных тканях, разнообразнее по своему составу, чем олигосахариды животных тканей.
Все они имеют ту же эмпирическую формулу С12Н22О11, т.е. являются изомерами.
Сахароза – белое кристаллическое вещество, сладкое на вкус, хорошо растворимое в воде.
Для сахарозы характерны реакции по гидроксильным группам. Как и все дисахариды, сахароза при кислотном или ферментативном гидролизе превращается в моносахариды, из которых она составлена.
Дисахариды – типичные сахароподобные углеводы; это твердые бесцветные кристаллические вещества, очень хорошо растворимое в воде, имеющие сладкие вкус.
Из дисахаридов наибольшее значение имеет сахароза C12H22O11:
Молекула сахарозы состоит из остатков молекул глюкозы и фруктозы.
http://himija-online.ru/organicheskaya-ximiya/uglevody/ximicheskie-svojstva-glyukozy.html
http://helpiks.org/8-88554.html