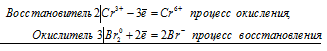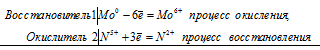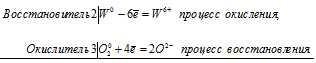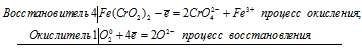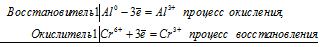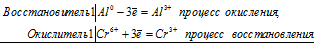Хром. Химия хрома и его соединений
Положение в периодической системе химических элементов
Хром расположен в 6 группе (или в побочной подгруппе VI группы в короткопериодной форме ПСХЭ) и в четвертом периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение атома хрома
Электронная конфигурация хрома в основном состоянии :
+24Cr 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 1 1s 

3s 


Примечательно, что у атома хрома уже в основном энергетическом состоянии происходит провал (проскок) электрона с 4s-подуровня на 3d-подуровень.
Физические свойства
Хром – твердый металл голубовато-белого цвета. Очень чистый хром поддается механической обработке. В природе встречается в чистом виде и широко применяется в различных отраслях науки, техники и производства. Чаще всего хром применяется, как компонент сплавов, которые используются при изготовлении медицинского или химического технологического оборудования и приборов.
Изображение с портала top10a.ru
Температура плавления 1890 о С, температура кипения 2680 о С, плотность хрома 7,19 г/см 3 .
Нахождение в природе
Хром – довольно распространенный металл в земной коре (0,012 масс.%). Основной минерал, содержащий хром – хромистый железняк FeO·Cr2O3 (или Fe(CrO2)2).
Способы получения
Хром получают из хромита железа. Для восстановления используют кокс:
Fe(CrO2)2 + 4C → Fe + 2Cr + 4CO
Еще один способ получения хрома: восстановление из оксида алюминием (алюмотермия):
Качественные реакции
Качественная реакция на ионы хрома +2 – взаимодействие избытка солей хрома (II) с щелочами . При этом образуется коричневый аморфный осадок гидроксида хрома (II).
Например , хлорид хрома (II) взаимодействует с гидроксидом натрия:
CrCl2 + 2NaOH → Cr(OH)2 + 2NaCl
Качественная реакция на ионы хрома +3 – взаимодействие избытка солей хрома (III) с щелочами . При этом образуется серо-зеленый аморфный осадок гидроксида хрома (III).
Например , хлорид хрома (III) взаимодействует с гидроксидом калия:
CrCl3 + 3KOH → Cr(OH)3 + 3KCl
При дальнейшем добавлении щелочи амфотерный гидроксид хрома (III) растворяется с образованием комплексной соли:
Обратите внимание , если мы поместим соль хрома (III) в избыток раствора щелочи, то осадок гидроксида хрома (III) не образуется, т.к. в избытке щелочи соединения хрома (III) сразу переходят в комплекс:
Соли хрома можно обнаружить с помощью водного раствора аммиака. При взаимодействии растворимых солей хрома (II) с водным раствором аммиака также образуется коричневый осадок гидроксида хрома (II).
CrCl2 + 2NH3 + 2H2O → Cr(OH)2↓ + 2NH4Cl
Cr 2+ + 2NH3 + 2H2O → Cr(OH)2↓ + 2NH4 +
При взаимодействии растворимых солей хрома (III) с водным раствором аммиака также образуется серо-зеленый осадок гидроксида хрома (III).
CrCl3 + 3NH3 + 3H2O → Cr(OH)3↓ + 3NH4Cl
Cr 3+ + 3NH3 + 3H2O → Cr(OH)3 ↓ + 3NH4 +
Химические свойства
В соединениях хром может проявлять степени окисления от +1 до +6. Наиболее характерными являются соединения хрома со степенями окисления +3 и +6. Менее устойчивы соединения хрома со степенью окисления +2. Хром образует комплексные соединения с координационным числом 6.
1. При комнатной температуре хром химически малоактивен из-за образования на его поверхности тонкой прочной оксидной пленки. При нагревании оксидная пленка хрома разрушается, и он реагирует практически со всеми неметаллами: кислородом, галогенами, серой, азотом, кремнием, углеродом, фосфором.
1.1. При взаимодействии хрома с галогенами образуются галогениды:
2Cr + 3Cl2 → 2CrCl3
1.2. Хром реагирует с серой с образованием сульфида хрома:
1.3. Хром взаимодействует с фосфором . При этом образуется бинарное соединение – фосфид хрома:
Cr + P → CrP
1.4. С азотом хром реагирует при нагревании до 1000 о С с образованием нитрида:
2Cr + N2 → 2CrN
1.5. Хром не взаимодействует с водородом.
1.6. Хром взаимодействует с кислородом с образованием оксида:
2. Хром взаимодействует и со сложными веществами:
2.1. Хром реагирует с парами воды в раскаленном состоянии:
2.2. В ряду напряжений хром находится левее водорода и поэтому в отсутствии воздуха может вытеснить водород из растворов минеральных кислот (соляной и разбавленной серной кислоты), образуя соли хрома (II).
Например , хром бурно реагирует с соляной кислотой :
Cr + 2HCl → CrCl2 + H2↑
В присутствии кислорода образуются соли хрома (III):
4Cr + 12HCl + 3O2 → 4CrCl3 + 6H2O
2.3. При обычных условиях хром не реагирует с концентрированной серной кислотой из-за пассивации – образования плотной оксидной пленки. При нагревании реакция идет, образуются оксид серы (IV), сульфат хрома (III) и вода:
2.4. Хром не реагирует при обычных условиях с концентрированной азотной кислотой также из-за пассивации.
Только при сильном нагревании концентрированная азотная кислота растворяет хром:
2.5. Растворы щелочей на хром практически не действуют.
2.6. Однако хром способен вытеснять многие металлы , например медь, олово, серебро и др. из растворов их солей.
Например , хром реагирует с хлоридом меди с образованием хлорида хрома (III) и меди:
2Cr + 3CuCl2 → 2CrCl3 + 3Cu
Восстановительные свойства хрома также проявляются при взаимодействии его с сильными окислителями: пероксидом натрия, нитратами и нитритами, хлоратами в щелочной среде.
Например , при сплавлении хрома с хлоратом калия в щелочи хром окисляется до хромата калия:
Хлорат калия и нитрат калия также окисляют хром:
Оксид хрома (III)
Способы получения
Оксид хрома (III) можно получить различными методами :
1. Термическим разложением гидроксида хрома (III):
2. Разложением дихромата аммония:
3. Восстановлением дихромата калия углеродом (коксом) или серой:
Химические свойства
Оксид хрома (III) – типичный амфотерный оксид . При этом оксид химически довольно инертен. В высокодисперсном состоянии с трудом взаимодействует с кислотами и щелочами.
1. При сплавлении оксида хрома (III) с основными оксидами активных металлов образуются соли-хромиты.
Например , оксид хрома (III) взаимодействует с оксидом натрия:
2. Оксид хрома (III) взаимодействует с растворимыми основаниями (щелочами). При этом в расплаве образуются соли—хромиты, а в растворе реакция практически не идет . При этом оксид хрома (III) проявляет кислотные свойства.
Например , оксид хрома (III) взаимодействует с гидроксидом натрия в расплаве с образованием хромита натрия и воды:
3. Оксид хрома (III) не взаимодействует с водой.
4. Оксид хрома (III) проявляет слабые восстановительные свойства . В щелочных расплавах окислителей окисляется до соединений хрома (VI).
Например , оксид хрома (III) взаимодействует с нитратом калия в щелочной среде:
Оксид хрома (III) окисляется бромом в присутствии гидроксида натрия:
Озоном или кислородом:
Нитраты и хлораты в расплаве щелочи также окисляют оксид хрома (III):
5. Оксид хрома (III) в высокодисперсном состоянии при сильном нагревании взаимодействует с сильными кислотами .
Например , оксид хрома (III) реагирует с серной кислотой:
6. Оксид хрома (III) проявляет слабые окислительные свойства при взаимодействии с более активными металлами.
Например , оксид хрома (III) реагирует с алюминием (термит):
Реакция очень экзотермическая, сопровождается выделением большого количества света:

Если сжечь большой объем термита в тигле, то можно получить металлический хром:

7. Оксид хрома (III) – твердый, нелетучий. А следовательно, он вытесняет более летучие оксиды (как правило, углекислый газ) из солей при сплавлении.
Например , из карбоната калия:
Оксид хрома (II)
Химические свойства
Оксид хрома (II) имеет основный характер, ему соответствует гидроксид хрома (II), обладающий основными свойствами.
1. При обычной температуре устойчив на воздухе, выше 100°С окисляется кислородом . Все соединения хрома (II) – сильные восстановители.
2. При высоких температурах оксид хрома (II) диспропорционирует :
3CrO → Cr + Cr2O3
3. Оксид хрома (II) не взаимодействует с водой.
4. Оксид хрома (II) проявляет основные свойства. Взаимодействует с сильными кислотами и кислотными оксидами .
Например , оксид хрома (II) взаимодействует с соляной кислотой:
CrO + 2HCl → CrCl2 + H2O
И с серной кислотой:
Оксид хрома (VI)
Оксид хрома (VI) CrO3 – темно-красное кристаллическое вещество. Гигроскопичен, расплывается на воздухе, малоустойчив, разлагается при нормальных условиях.
Способы получения
Оксид хром (VI) можно получить действием концентрированной серной кислоты на сухие хроматы или дихроматы:
Химические свойства
Оксид хрома (VI) – кислотный. Сильно ядовит. Оксиду хрома (VI) соответствуют хромовая (H2CrO4) и дихромовая (H2Cr2O7) кислоты.

1. При взаимодействии оксида хрома (VI) с водой образуется хромовые кислоты:
2. Оксид хрома (VI) проявляет кислотные свойства. Взаимодействует с основаниями и основными оксидами .
Например , оксид хрома (VI) взаимодействует с гидроксидом калия с образованием хромата калия:
Или с оксидом лития с образованием хромата лития:
3. Оксид хрома (VI) – очень сильный окислитель : окисляет углерод, серу, иод, фосфор, превращаясь при этом в оксид хрома (III).
Например , сера окисляется до оксида серы (IV):
Оксид хрома (VI) также окисляет сложные вещества, например , сульфиты:
И некоторые органические веществ, например , этанол:
Гидроксид хрома (III)
Гидроксид хрома (III) Cr(OH)3 – это твердое вещество серо-зеленого цвета.
Способы получения
1. Гидроксид хрома (III) можно получить действием раствора аммиака на соли хрома (III).
Например , хлорид хрома (III) реагирует с водным раствором аммиака с образованием гидроксида хрома (III) и хлорида аммония:
2. Пропусканием углекислого газа, сернистого газа или сероводорода через раствор гексагидроксохромата калия:
Чтобы понять, как протекает эта реакция, можно использовать несложный прием: мысленно разбить сложное вещество K3[Cr(OH)6] на составные части: KOH и Cr(OH)3. Далее мы определяем, как реагирует углекислый газ с каждым из этих веществ, и записываем продукты их взаимодействия. Т.к. Cr(OH)3 не реагирует с СО2, то мы записываем справа Cr(OH)3 без изменения. Гидроксид калия реагирует с избытком углекислого газа с образованием гидрокарбоната калия
3. Гидроксид хрома (III) можно получить действием недостатка щелочи на избыток соли хрома (III).
Например , хлорид хрома (III) реагирует с недостатком гидроксида калия с образованием гидроксида хрома (III) и хлорида калия:
4. Также гидроксид хрома (III) образуется при взаимодействии растворимых солей хрома (III) с растворимыми карбонатами, сульфитами и сульфидами . Сульфиды, карбонаты и сульфиты хрома (III) необратимо гидролизуются в водном растворе.
Например: бромид хрома (III) реагирует с карбонатом натрия. При этом выпадает осадок гидроксида хрома (III), выделяется углекислый газ и образуется бромид натрия:
Хлорид хрома (III) реагирует с сульфидом натрия с образованием гидроксида хрома (III), сероводорода и хлорида натрия:
Химические свойства
1. Гидроксид хрома (III) реагирует с растворимыми кислотами . При этом образуются средние соли.
Например , гидроксид хрома (III) взаимодействует с соляной кислотой с образованием хлорида хрома (III):
2. Гидроксид хрома (III) взаимодействует с кислотными оксидами сильных кислот .
Например , гидроксид хрома (III) взаимодействует с оксидом серы (VI) с образованием сульфата хрома (III):
3. Гидроксид хрома (III) взаимодействует с растворимыми основаниями (щелочами). При этом в растворе образуются комплексные соли . При этом гидроксид хрома (III) проявляет кислотные свойства.
Например , гидроксид хрома (III) взаимодействует с избытком гидроксидом натрия с образованием гексагидроксохромата:
4. Г идроксид хрома (III) разлагается при нагревании :
5. Под действием окислителей в щелочной среде переходит в хромат.
Например , при взаимодействии с бромом в щелочной среде гидроксид хрома (III) окисляется до хромата:
Гидроксид хрома (II)
Способы получения
1. Гидроксид хрома (II) можно получить действием раствора аммиака на соли хрома (II).
Например , хлорид хрома (II) реагирует с водным раствором аммиака с образованием гидроксида хрома (II) и хлорида аммония:
2. Гидроксид хрома (II) можно получить действием щелочи на соли хрома (II).
Например , хлорид хрома (II) реагирует с гидроксидом калия с образованием гидроксида хрома (II) и хлорида калия:
CrCl2 + 2KOH → Cr(OH)2↓ + 2KCl
Химические свойства
1. Гидроксид хрома (II) проявляет основные свойства . В частности, реагирует с растворимыми кислотами .
Например , гидроксид хрома (II) взаимодействует с соляной кислотой с образованием хлорида хрома (II). Соли хрома (II) окрашивают раствор в синий цвет.
2. Гидроксид хрома (II) взаимодействует с кислотными оксидами сильных кислот .
Например , гидроксид хрома (II) взаимодействует с оксидом серы (VI) с образованием сульфата хрома (II):
3. Гидроксид хрома (II) – сильный восстановитель.
Например , под действием кислорода воздуха гидроксид хрома (II) окисляется до гидроксида хрома (III):
Соли хрома
Соли хрома (II)
Все соли хрома (II) – сильные восстановители. В растворах окисляются даже кислородом воздуха.
Например , хлорид хрома (II) окисляется кислородом в растворе в присутствии щелочи до соединений хрома (III):
Концентрированные кислоты-окислители (азотная и серная) также окисляют соединения хрома (II):
Соли хрома (III)
Хром с валентностью III образует два типа солей:
- Соли, в которых хром (III) является катионом. Например , хлорид хрома (III) CrCl3.
- Соли, в которых хром (III) входит в состав кислотного остатка – хромиты и гидроксокомплексы хрома (III) . Например , хромит калия, KCrO2. или гексагидроксохромат (III) калия K3[Cr(OH)6].
1. Соли хрома (III) проявляют слабые восстановительные свойства . окисляются под действием сильных окислителей в щелочной среде.
Например , бром в присутствии гидроксида калия окисляет хлорид хрома (III):
2CrCl3 + 3Br2 + 16KOH → 2K2CrO4 + 6KBr + 6KCl + 8H2O
или сульфат хрома (III):
Пероксид водорода в присутствии щелочи также окисляет соли хрома (III):
Даже перманганат калия в щелочной среде окисляет соли хрома (III):
Комплексные соли хрома (III) также окисляются сильными окислителями в присутствии щелочей.
Например , гексагидроксохроматы окисляются бромом в щелочи:
Оксид свинца (IV) также окисляет хромиты:
2. Соли хрома (III) в щелочной среде образуют гидроксид хрома (III), который сразу растворяется, образуя гидроксокомплекс.
2CrCl3 + 6KOH → 2Cr(OH)3 + 6KCl
3. Более активные металлы вытесняют хром (III) из солей.
Например , цинк реагирует с хлоридом хрома (III):
Гидролиз солей хрома (III)
Растворимые соли хрома (III) и сильных кислот гидролизуются по катиону. Гидролиз протекает ступенчато и обратимо, т.е. чуть-чуть:
I ступень: Cr 3+ + H2O = CrOH 2+ + H +
II ступень: CrOH 2+ + H2O = Cr(OH )2 + + H +
Однако сульфиды, сульфиты, карбонаты хрома (III) и их кислые соли гидролизуются необратимо, полностью, т.е. в водном растворе не существуют, а разлагаются водой в момент образования.
Например , при сливании растворов солей хрома (III) и сульфита, гидросульфита, карбоната или сульфида натрия протекает взаимный гидролиз:
Более подробно про гидролиз можно прочитать в соответствующей статье.
Хромиты
Соли, в которых хром (III) входит в состав кислотного остатка (хромиты) — образуются из оксида хрома (III) при сплавлении с щелочами и основными оксидами:
Для понимания свойств хромитов их удобно мысленно разделить на два отдельных вещества.
Например , хромит натрия мы поделим мысленно на два вещества: оксид хрома (III) и оксид натрия.
NaСrO2 разделяем на Na2O и Cr2O3
При этом очевидно, что хромиты реагируют с кислотами. При недостатке кислоты образуется гидроксид хрома (III):
NaCrO2 + HCl (недостаток) + H2O → Cr(OH)3 + NaCl
В избытке кислоты гидроксид хрома (III) не образуется:
NaCrO2 + 4HCl (избыток) → CrCl3 + NaCl + 2H2O
NaCrO2 + 4HCl → CrCl3 + NaCl + 2H2O
Под действием избытка воды хромиты гидролизуются:
Соли хрома (VI)
Оксиду хрома ( VI ) соответствуют две кислоты – хромовая Н2 CrO 4 и дихромовая Н2 Cr 2 O 7. Поэтому хром в степени окисления +6 образует два типа солей: хроматы и дихроматы.
Например , хромат калия K2CrO4 и дихромат калия K2Cr2O7.
1. Различить эти соли довольно легко: хроматы желтые, а дихроматы оранжевые. Хроматы устойчивы в щелочной среде, а дихроматы устойчивы в кислой среде.
При добавлении к хроматам кислот они переходят в дихроматы.
Например , хромат калия взаимодействует с серной кислотой и разбавленной соляной кислотой с образованием дихромата калия:
И наоборот: дихроматы реагируют с щелочами с образованием хроматов.
Например , дихромат калия взаимодействует с гидроксидом калия с образованием хромата калия:
Видеоопыт взаимных переходов хроматов и дихроматов при добавлении кислоты или щелочи можно посмотреть здесь.
2. Хроматы и дихроматы проявляют сильные окислительные свойства. При взаимодействии с восстановителями они восстанавливаются до соединений хрома (III).
В нейтральной среде хроматы и дихроматы восстанавливаются до гидроксида хрома (III).
Например , дихромат калия реагирует с сульфитом натрия в нейтральной среде:
Хромат калия окисляет сульфид аммония:
При взаимодействии с восстановителями в щелочной среде хроматы и дихроматы образуют комплексные соли.
Например , хромат калия окисляет гидросульфид аммония в щелочной среде:
Хромат натрия окисляет сернистый газ:
Хромат натрия окисляет сульфид натрия:
При взаимодействии с восстановителями в кислой среде хроматы и дихроматы образуют соли хрома (III).
Например , дихромат калия окисляет сероводород в присутствии серной кислоты:
Дихромат калия окисляет йодид калия, фосфид кальция, соединения железа (II), сернистый газ, концентрированную соляную кислоту:
Составте уравнения реакций горения следующих веществ кальция, Хрома (в образ оксиде хром 3 — х вол) , Вольфрама (в образ оксиде вольфрам 6 вол) , Цинка , Пропана C3H8 , Бутена C4H8?
Химия | 5 — 9 классы
Составте уравнения реакций горения следующих веществ кальция, Хрома (в образ оксиде хром 3 — х вол) , Вольфрама (в образ оксиде вольфрам 6 вол) , Цинка , Пропана C3H8 , Бутена C4H8.
4Cr + 3O2 = 2Cr2O3
C3H8 + 5O2 = 3CO2 + 4H2O
C4H8 + 6O2 = 4CO2 + 4H2O.
Пожалуйстаа, очень надо, кто разбирается в химии, даю 40 баллов?
Пожалуйстаа, очень надо, кто разбирается в химии, даю 40 баллов!
напишите уравнения реакций горения в кислороде кальция, хрома(в образующемся оксиде хром трехвалентен), вольфрама( в образующемся оксиде вольфрам шестивалентен), цинка, пропана С3Н8, бутена С4Н8.
Напишите уравнения реакций между соляной кислотой и : а) гидроксидом кальция ; б) оксидом алюминия ; в) цинком?
Напишите уравнения реакций между соляной кислотой и : а) гидроксидом кальция ; б) оксидом алюминия ; в) цинком.
Назовите образующиеся вещества.
Вычислите кол — во вещества оксида хрома(ІІІ) и массу воды, которые образуются при разложении гидроксида хрома(ІІІ)массой 41, 2г?
Вычислите кол — во вещества оксида хрома(ІІІ) и массу воды, которые образуются при разложении гидроксида хрома(ІІІ)массой 41, 2г.
Составьте формулы веществ по названию фосфид кальция карбид кремния (IV) хлорид кремния (IV) сульфид цинка оксид фосфора (V) оксид хрома(III) оксид натрия оксид железа (II)?
Составьте формулы веществ по названию фосфид кальция карбид кремния (IV) хлорид кремния (IV) сульфид цинка оксид фосфора (V) оксид хрома(III) оксид натрия оксид железа (II).
Помогите?
Даны вещ — ва : оксид хрома(3), кислород, цинк, соляная кислота.
Составьте уравнения реакций, в результате которых можно получить : водород, хром, оксид цинка, воду.
Вольфрам W получает восстановлением оксида вольфрама (VI) водородом ?
Вольфрам W получает восстановлением оксида вольфрама (VI) водородом .
Напишите уравнение реакции.
Напишите уравнение реакций разложения : а)гидроксида бария если при этом образуется оксид бария и вода, б)нитрата цинка, если при этом образуется оксид цинка, оксид азота(lV) и кислород, в)нитрата амм?
Напишите уравнение реакций разложения : а)гидроксида бария если при этом образуется оксид бария и вода, б)нитрата цинка, если при этом образуется оксид цинка, оксид азота(lV) и кислород, в)нитрата аммония (NH4NO3) если при этом образуется оксид азота(I) и вода, г)гидроксид хрома(III), если при этом образуется соответствующий оксид и вода, д)питьевой соды (NaHCO3) если при этом образуется карбонат натрия, оксид углерода(IV)и вода.
Помогите пожалуйста?
Формула какого вещества Cr2O3?
1)хромат кислорода 2)оксид хрома (II) 3) оксид хрома (III) 4) оксид хрома.
Составьте уравнения реакций последовательного перехода : Дихромат калия — > ; оксид хрома (VI) — > ; оксид хрома (III) — > ; метахромит калия — > ; сульфат хрома (III)?
Составьте уравнения реакций последовательного перехода : Дихромат калия — > ; оксид хрома (VI) — > ; оксид хрома (III) — > ; метахромит калия — > ; сульфат хрома (III).
Напишите уравнения реакций взаимодействия кальция со след веществами : азот, разбавленная серная кислота,оксид хрома (III), водой?
Напишите уравнения реакций взаимодействия кальция со след веществами : азот, разбавленная серная кислота,
оксид хрома (III), водой.
На этой странице находится ответ на вопрос Составте уравнения реакций горения следующих веществ кальция, Хрома (в образ оксиде хром 3 — х вол) , Вольфрама (в образ оксиде вольфрам 6 вол) , Цинка , Пропана C3H8 , Бутена C4H8?, из категории Химия, соответствующий программе для 5 — 9 классов. Чтобы посмотреть другие ответы воспользуйтесь «умным поиском»: с помощью ключевых слов подберите похожие вопросы и ответы в категории Химия. Ответ, полностью соответствующий критериям вашего поиска, можно найти с помощью простого интерфейса: нажмите кнопку вверху страницы и сформулируйте вопрос иначе. Обратите внимание на варианты ответов других пользователей, которые можно не только просмотреть, но и прокомментировать.
Cl₂ Br₂ I₂ F₂ Вроде бльше нет Всегда пишутся отдельно так, если ввещ — ве, например Ca²⁺Cl₂⁻ то здесь двойка из — за степени окисления кальция.
1. m(в — ва) = m(р — ра) * n = 450 * 20% = 90 грамм m(H2O) = m(р — ра) — m(в — ва) = 450 — 90 = 360 грамм 2. 90 + 30 = 120грамм (в — ва(2)) 360 + 120 = 480грамм (раствора(2)) n = m(в — ва(2)) / m(раствора(2)) = (120 / 480) * 100% = 25%.
Ответ 3 Fe3(PO4)2 Mr = 3Fe + 2P + 😯 = 168 + 62 + 16 * 8 = 358 w (3Fe) = m элемента / m вещества = 168 / 358 = 0. 47 = 47% w(2P) = 0. 17 = 17% w(8O) = 0. 36 = 36%.
Азотная кислота — HNO3 Серная кислота — H2SO4.
ZnCl2 + Na2S = ZnS + 2NaCl.
1. C4H8 + H2 = C4H10 Бутен + водород = бутан 2. C4H10 + Cl2 = C4H9Cl + HCl Бутан + хлор = хлорбутан + хлороводород 3. 2C4H9Cl + 2Na = C8H18 + 2NaCl Хлорбутан + натрий = октан + хлорид натрия 4. C8H18 + 12. 5O2 = 8CO2 + 9H2O Октан + кислород = угл..
Это две отдельные реакции : 3ZnSO₄ + 2Na₃PO₄ = Zn₃(PO₄)₂ + 3Na₂SO₄ 3MgCl₂ + 2Na₃PO₄ = Mg₃(PO₄)₂ + 6NaCl суммарно : 3ZnSO₄ + 3MgCl₂ + 4Na₃PO₄ = Zn₃(PO₄)₂ + 3Na₂SO₄ + Mg₃(PO₄)₂ + 6NaCl.
1 — ВОРОНКА 2 — СТАКАН 3 — ? 4 — ЗАЖИМ 5 — СТЕРЖЕНЬ 6 — ПРОБИРКА 7 — ? 8 — КОЛБА 9 — ПРОБКА 10 — КОЛЬЦО Ключевое слово — Князь Игорь.
3 — бутилфенол и пентилбутаноат).
Ответ — Г ) Ar , тк слева на право радиус уменьшается.
Химические свойства хрома
Задание 411
Хромит калия окисляется бромом в щелочной среде. Зеленая окраска раствора переходит в желтую. Составьте электронные и молекулярные уравнения реакции. Какие ионы обусловливают начальную и конечную окраску раствора?
Решение:
Уравнение реакции окисления-восстановления хромата калия бромом
2Cr 3+ + 3Br2 0 = 2Cr 6+ + 6Br —
Начальная, зелёная окраска обусловливается хромит-ионами CrO2 — , а конечная, жёлтая – хромат-ионами CrO4 2- .
Задание 412
Составьте электронные и молекулярные уравнения реакций растворения: а) молибдена в азотной кислоте; б) вольфрама в щелочи в присутствии кислорода. Учтите, что молибден и вольфрам приобретают высшую степень окисления.
Решение:
Уравнения реакций растворения металлов в кислоте и щёлочи
а) Растворение молибдена в азотной кислоте
б) Растворение вольфрама в щелочи в присутствии кислорода
2W 0 + 3O2 0 = 2W 6+ + 6O 2-
Задание 413
При сплавлении хромита железа Fe(CrO2)2 с карбонатом натрия в присутствии кислорода хром (III) и железо (II) окисляются и приобретают соответственно степени окисления +6 и +3. Составьте электронные и молекулярное уравнения реакции.
Решение:
Уравнение реакции сплавления хромита железа с карбонатом натрия
Задание 414
К подкисленному серной кислотой раствору дихромата калия прибавили порошок алюминия. Через некоторое время оранжевая окраска раствора перешла в зеленую. Составьте электронные и молекулярное уравнения реакции.
Решение:
Уравнение реакции серной кислоты с дихроматом калия
Al 0 + Cr 6+ = Al 3+ + Cr 3+
Задание 415
Хром получают методом алюминотермии из его оксида (III), а вольфрам — восстановлением оксида вольфрама (VI) водородом. Составьте электронные и молекулярные уравнения соответствующих реакций.
Решение:
Уравнениие реакции получения хрома методом алюминотермии
а) Получение хрома методом алюминотермии
Al 0 + Cr 6+ = Al 3+ + Cr 3+
б) Получение вольфрама методом алюминотермии
http://himia.my-dict.ru/q/1925345_sostavte-uravnenia-reakcij-gorenia-sleduusih-vesestv/
http://buzani.ru/zadachi/khimiya-shimanovich/993-svojstva-khroma-zadaniya-412-415