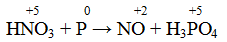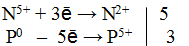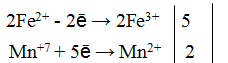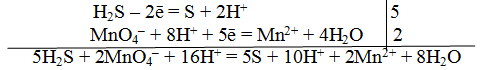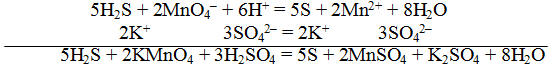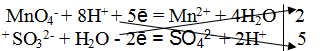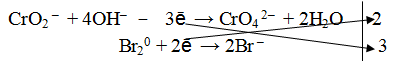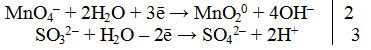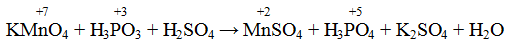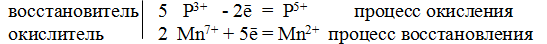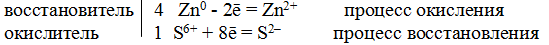Составление уравнений окислительно-восстановительных реакций
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Составление уравнений окислительно-восстановительных реакций.
Для составления уравнений окислительно-восстановительных реакций и определения коэффициентов применяют два метода: метод электронного баланса и ионно-электронный метод (метод полуреакций).
Метод электронного баланса является более простым и учитывает изменение степени окисления элементов в реакциях. Ионно-электронный метод учитывает характер химической связи в молекуле и наличие тех ионов, которые в действительности существуют в растворе, например, MnO4 – , SO4 2- , Cr2O7 2- . При реакциях окисления-восстановления электроны не берутся откуда-то со стороны, а только переходят от одних атомов или ионов к другим, поэтому число электронов, принятых окислителем, равно числу электронов, отданных восстановителем. При составлении уравнений окислительно-восстановительных реакций для того, чтобы правильно написать продукты реакции, необходимо знать свойства реагирующих веществ.
8.3.1.Метод электронного баланса.
Подбор коэффициентов в реакции методом электронного баланса осуществляется по следующей схеме:
1) Составить схему реакции
Разбавленная азотная кислота с а) неактивными металлами (Cu), б) неметаллами (P, As, S) и в) производными этих неметаллов (AsH3, PH3, As2S3) образует оксид азота (II), понижая свою степень окисления:
Атом элемента в своей высшей положительной степени окисления является окислителем, следовательно, окислитель
Атом фосфора проявляет восстановительные свойства в данной реакции, отдавая электроны с последнего энергетического уровня и повышая свою степень окисления до +5.
Следовательно, молекулярное уравнение реакции имеет следующий вид:
2) Определить величину и знак степени окисления элементов до реакции и после реакции.
3) Составить электронный баланс
4) Подставить найденные коэффициенты в уравнение реакции.
5) Подсчитать количество атомов водорода в правой и левой части равенства и уравнять их за счет добавления молекул воды в ту часть равенства, где их недостаточно.
6) Подсчитать количество атомов кислорода.
При правильно написанном и решенном уравнении количество атомов кислорода в правой и левой части равенства совпадает.
Пример 1. Написать уравнение окислительно-восстановительной реакции, подобрав коэффициенты к нему: FeSO4 + KMnO4 + H2SO4→ Fe2(SO4)3 + + MnSO4 + K2SO4 + H2O. Определяем степень окисления элементов до реакции и после реакции.
Составляем уравнения электронного баланса
Подставляем найденные коэффициенты в уравнение реакции. Подсчитываем количество групп в правой части уравнения (15+2+1=18), добавляем в левую часть равенства недостающие -группы в виде коэффициента при H2SO4. уравниваем число атомов водорода в правой и левой части равенства.
Правильность написанного уравнения проверяем по числу атомов кислорода в правой и левой части равенства.
8.3.2. Ионно-электронный метод.
При составлении электронно-ионных уравнений следует исходить не из изменения степени окисления элементов в реагирующих веществах, а нужно учитывать действительно существующие ионы в водном растворе с точки зрения теории электролитической диссоциации. Например, если реакция происходит с участием перманганата калия, то в реакции окислителем будут ионы MnO4 – , а не ионы Mn 7+ , так как перманганат калия в водном растворе диссоциирует KMnO4↔K + +MnO4 – . При этом вещества неионного характера и недиссоциирующие изображаются в электронных уравнениях в виде молекул: NH3, CO, NO2, SiO2, P.
В окислительно-восстановительных реакциях могут получаться различные продукты реакции в зависимости от характера среды – кислой, щелочной, нейтральной. Для таких реакций в молекулярной схеме необходимо указывать окислитель, восстановитель и вещество, характеризующее реакцию среды (кислоту, щелочь, воду). В этом случае в ионном уравнении необходимо руководствоваться правилами стяжения, указывать ионы, характеризующие реакцию среды: H + , OH – , H2O. Правила стяжения сводятся к следующему:
1. В кислой среде избыток ионов O +2 образует с ионами H + молекулы воды:
2. В нейтральной или щелочной среде избыток ионов O 2- образует с молекулами воды гидроксид – ионы:
3. В щелочной среде недостаток ионов O 2– компенсируется двумя ионами OH – , одновременно образуется одна молекула воды:
| Реакция среды | Избыток ионов О 2– | Недостаток ионов О 2– |
| окислитель | восстановитель | |
| Кислая | Н + Н2О | Н2O 2Н + |
| изб. O 2– + 2H + = Н2О | Н2О 2Н + + O 2– | |
| Нейтральная | H2O OH – | Н2O 2Н + |
| изб. О 2– + Н2О 2OН – | Н2О 2Н + + О 2– | |
| Щелочная | Н2O ОН – | 2OН – Н2О |
| изб. О 2– + Н2O 2OН – | 2OН – Н2О + О 2– |
Разберем на конкретных примерах.
Пример 1. Составить уравнение реакции, которая протекает при пропускании сероводорода Н2S через подкисленный раствор перманганата калия КМnO4
При протекании реакции малиновая окраска исчезает и раствор мутнеет. Опыт показывает, что помутнение раствора происходит в результате образования элементарной серы из сероводорода:
В этой схеме число атомов одинаково в левой и правой частях. Для уравнивания зарядов надо от левой части схемы отнять два электрона, после чего можно стрелку заменить на знак равенства:
Эта первая полуреакция — процесс окисления восстановителя H2S.
Обесцвечивание раствора связано с переходом иона МnО – 4 (он имеет малиновую окраску) в ион Mn 2+ (почти бесцветный и лишь при большой концентрации имеет розоватую окраску), что можно выразить схемой
Опыт показывает, что в кислом растворе кислород, входящий в состав ионов MnO – 4, вместе с ионами водорода в конечном итоге образует воду. Поэтому процесс перехода записываем так:
Чтобы стрелку заменить на знак равенства, надо уравнять и заряды. Поскольку исходные вещества имеют семь положительных зарядов (7+), а конечные – два положительных (2+), то для выполнения условия сохранения зарядов надо к левой части схемы прибавить пять электронов:
MnO – 4 + 8H + +5e – = Mn 2+ +4H2О
Это вторая полуреакция – процесс восстановления окислителя – иона MnO – 4.
Для составления общего (суммарного) уравнения реакции надо уравнение полуреакций почленно суммировать, предварительно уравнять число отданных и полученных электронов. В этом случае по правилам нахождения наименьшего кратного определяют соответствующие множители, на которые умножаются равенства полуреакций. Сокращенно запись проводится так:
Сократив на 10 Н + , окончательно получим
Проверяем правильность составленного ионного уравнения. В примере число атомов кислорода в левой части 8, в правой 8; число зарядов в левой части (2-) + (6+) == 4+, в правой 2(2+) = 4+. Уравнение составлено правильно.
Методом полуреакций составляется ионное уравнение реакции. Чтобы от ионного уравнения перейти к молекулярному, поступаем так: в левой части ионного уравнения к каждому аниону подбираем соответствующий катион, а к каждому катиону — анион. Затем такие же ионы в таком же количестве записываем и в правую часть уравнения, после чего ионы объединяем в молекулы:
Пример 2. Реакция среды кислая
1. Составить схему реакции
Из опытных данных знаем, что окислителем является КМnO4. Ион MnO4 – восстанавливается в кислой среде до Мn 2+ (фиолетово-малиновая окраска иона MnO4 – становится бесцветной, переходя в Мn 2+ – ион), следовательно, ион SO3 2 – будет являться восстановителем, переходя в ион SO4 2- .
2. Составить электронно-ионные уравнения
а) для окислителя
Из ионной схемы видно, что, ион MnO4 – – превращается в ион Мn 2+ , при этом освобождаются ионы О 2- , которые по правилу стяжения в кислой среде связываются ионами Н + , образуя молекулы Н2O.
б) для восстановителя
Из ионной схемы видно, что ион SO3 2- превращается в ион SO4 2- . Для этого превращения необходимо добавить ион О 2- , который берется из молекулы H2O (реакция протекает в водной среде), при этом освобождаются два иона Н+.
3. Подсчитать число зарядов в правой и левой части равенства, добавляя или уменьшая необходимое число электронов. Алгебраическая сумма зарядов в обеих частях равенства должна быть одинакова.
MnO4 – + 8H + + 5ē = Mn 2+ + 4H2O
4. Найти основные коэффициенты, т. е. коэффициенты при окислителе и восстановителе:
5. Написать суммарное электронно-ионное уравнение, учитывая найденные коэффициенты:
6. Сократить в левой и правой части уравнения 10 Н + и 5Н2O. Получается ионное уравнение:
7. По ионному уравнению составить молекулярное уравнение реакции:
8. Число ионов и атомов каждого элемента в правой и левой части равенства, должно быть равно.
Пример 3. Реакция среды щелочная.
1. Составить схему реакции
Окислителем в данной реакции является молекула брома, следовательно, восстановителем будет являться метахромит калия, а именно ион СrO2 – .
2. Составить электронно-ионное уравнение
а) для окислителя
б) для восстановителя
Из ионной схемы видно, что ион CrO2 – превращается в ион СгО4 2– . Каждый недостающий ион О 2– берется по правилу стяжения из двух гидроксильных ионов (среда щелочная ОН – ), при этом одновременно образуется одна молекула воды.
3. Подсчитать число зарядов в правой и левой части равенства. Найти коэффициенты при окислителе и восстановителе.
4. Написать суммарное уравнение, учитывая найденные коэффициенты:
5. По ионному уравнению составить молекулярное уравнение реакции.
6. Число атомов и ионов каждого элемента в правой и левой части уравнения должно быть равно.
Пример 4. Реакция среды нейтральная.
1. Составить схему реакции
Окислителем является КМnO4, так как ион элемента в своей высшей степени окисления не способен более отдавать электроны (Мn +7 ). Восстановителем является сульфит калия K2SO3.
2. Составить электронно-ионное уравнение
а) для окислителя
В нейтральной среде избыток ионов кислорода стягивается с молекулами воды, образуя гидроксид-ионы.
б) для восстановителя
Из ионной схемы видно, что ион SО3 2- превращается в ион SO4 2- , для этого необходимо добавить один ион О 2- , который берется из молекулы Н2O (реакция протекает в водной среде). При этом освобождаются два иона Н + .
3. Подсчитать число зарядов в правой и левой части равенства. Найти коэффициенты при окислителе и восстановителе.
4.Написать электронно-ионное уравнение, учитывая найденные коэффициенты:
Сокращаем левую и правую часть равенства на 6Н20. Получаем окончательное ионное уравнение.
5. По ионному уравнению составить молекулярное уравнение реакции.
6. Число атомов и ионов каждого элемента в правой и левей части уравнения должно быть равно.
Пример 5. Исходя из степени окисления (п) азота, серы и марганца в соединениях NН3, HNO2, HNO3, H2S, Н2SO3, Н2SО4, MnO2 и КМnO4, определите, какие из них могут быть только восстановителями, только окислителями и какие проявляют как окислительные, так и восстановительные свойства.
Решение. Степень окисления азота в указанных соединениях соответственно равна: -3 (низшая), +3 (промежуточная), +5 (высшая); n(S), соответственно, равна: -2 (низшая), +4 (промежуточная), +6 (высшая); n(Мn), соответственно, равна: + 4 (промежуточная), +7 (высшая). Отсюда: NН3, H2S — только восстановители; HNO3, H2SO4, КMnО4 — только окислители; НNО2, Н2SО3, MnO2 — окислители и восстановители.
Пример 6. Могут ли происходить окислительно-восстановительные реакции между следующими веществами: a) H2S и HI; б) H2S и Н2SО3; в) Н2SО3 и НС1O4?
а) Степень окисления в Н2S n(S) = -2; в HI n(I) = -1. Так как и сера и иод находятся в своей низшей степени окисления, то оба вещества проявляют только восстановительные свойства и взаимодействовать друг с другом не могут;
б) в H2S n(S) = -2 (низшая), в H2SO3 n(S) = +4 (промежуточная).
Следовательно, взаимодействие этих веществ возможно, причем, Н2SО3 является окислителем;
в) в Н2SO3 n(s) = +4 (промежуточная); в НС1O4 n(Сl) = +7 (высшая). Взятые вещества могут взаимодействовать, Н2SО3 в этом случае будет проявлять восстановительные свойства.
Пример 7. Составьте уравнения окислительно-восстановительной реакции, идущей по схеме:
Решение. Если в условии задачи даны как исходные вещества, так и продукты их взаимодействия, то написание уравнения реакции сводится, как правило, к нахождению и расстановке коэффициентов. Коэффициенты определяют методом электронного баланса с помощью электронных уравнений. Вычисляем, как изменяют степень окисления восстановитель и окислитель, и отражаем это в электронных уравнениях:
Общее число электронов, отданных восстановителем, должно быть равно числу электронов, которые присоединяет окислитель. Общее наименьшее кратное для отданных и принятых электронов 10. Разделив это число на 5, получаем коэффициент 2 для окислителя и продукта его восстановления, а при делении 10 на 2 получаем коэффициент 5 для восстановителя и продукта его окисления. Коэффициент перед веществами, атомы которых не меняют свою степень окисления, находят подбором. Уравнение реакции будет иметь вид:
Пример 8. Составьте уравнение реакции взаимодействия цинка с концентрированной серной кислотой, учитывая максимальное восстановление последней.
Решение. Цинк, как любой металл, проявляет только восстановительные свойства. В концентрированной серной кислоте окислительная функция принадлежит сере (+6). Максимальное восстановление серы означает, что она приобретает минимальную степень окисления. Минимальная степень окисления серы как p-элемента VIA-группы равна -2. Цинк как металл IIВ-группы имеет постоянную степень окисления +2. Отражаем сказанное в электронных уравнениях:
Составляем уравнение реакции:
Перед H2SO4 стоит коэффициент 5, а не 1, ибо четыре молекулы H2SO4 идут на связывание четырех ионов Zn 2+ .
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 6de1bb4718f30c05 • Your IP : 85.95.188.35 • Performance & security by Cloudflare
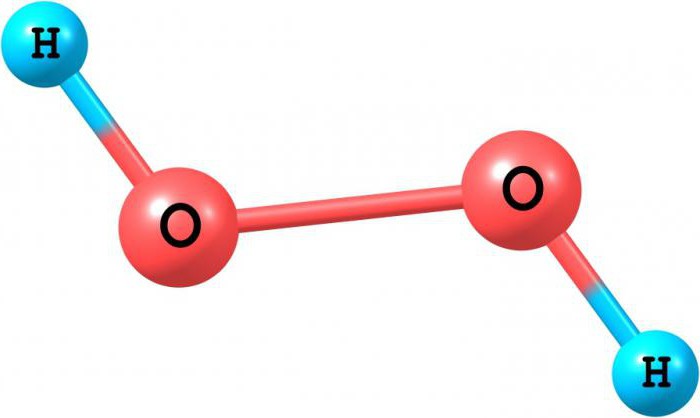
H2O2 — что это за вещество?

Общеизвестна формула основы жизни – воды. Её молекула состоит из двух атомов водорода и одного кислорода, что записывается как H2O. Если же кислорода будет в два раза больше, то получится совсем другое вещество – H2O2. Что это и чем полученное вещество будет отличаться от своей «родственницы» воды?
H2O2 – что это за вещество?
Остановимся на нем подробнее. H2O2 – формула перекиси водорода, Да, той самой, которой обрабатывают царапины, белой. Пероксид водорода H2O2 — название вещества научное.
Для дезинфекции используют трехпроцентный раствор перекиси. В чистом или концентрированном виде она вызывает химические ожоги кожи. Тридцатипроцентный раствор перекиси иначе называют пергидроль; раньше его применяли в парикмахерских для обесцвечивания волос. Обожженная им кожа также становится белой.
Химические свойства Н2О2
Перекись водорода представляет собой жидкость без цвета и с «металлическим» привкусом. Является хорошим растворителем и сама легко растворяется в воде, эфире, спиртах.
Трёх- и шестипроцентные растворы перекиси обычно готовят, разбавляя тридцатипроцентный раствор. При хранении концентрированного Н2О2 происходит разложение вещества с выделением кислорода, поэтому в плотно закупоренных емкостях его хранить не следует во избежание взрыва. С уменьшением концентрации пероксида, повышается его устойчивость. Также для замедления разложения Н2О2 можно добавлять в него различные вещества, например, фосфорную или салициловую кислоту. Для хранения растворов сильной концентрации (более 90 процентов) в перекись добавляют пирофосфат натрия, который стабилизирует состояние вещества, а также используют сосуды из алюминия.
Н2О2 в химических реакциях может быть как окислителем, так и восстановителем. Однако чаще пероксид проявляет окислительные свойства. Перекись принято считать кислотой, но очень слабой; соли перекиси водорода называют пероксидами.
Реакция разложения как метод получения кислорода
Реакция разложения Н2О2 происходит при воздействии на вещество высокой температуры (более 150 градусов Цельсия). В результате образуются вода и кислород.
Формула реакции – 2 Н2О2 + t -> 2 Н2О + О2
Можно посчитать электронный баланс H2O2 в уравнении:
Степень окисления Н в Н2О2 и Н2О = +1.
Степень окисления О: в Н2О2 = -1, в Н2О = -2, в О2 = 0
2 О -1 — 2е -> О2 0
О -1 + е -> О -2
2 Н2О2 = 2 Н2О + О2
Разложение перекиси водорода может произойти и при комнатной температуре, если использовать катализатор (химическое вещество, ускоряющее реакцию).
В лабораториях одним из методов получения кислорода, наряду с разложением бертолетовой соли или марганцовки, является реакция разложения перекиси. В таком случае в качестве катализатора используют оксид марганца (IV). Другие вещества, ускоряющие разложение H2O2, – медь, платина, гидроксид натрия.
История открытия перекиси
Первые шаги к открытию перекиси были сделаны в 1790 году немцем Александром Гумбольдтом, когда он обнаружил превращения оксида бария в пероксид при нагревании. Тот процесс сопровождался поглощением кислорода из воздуха. Через двенадцать лет учеными Тенаром и Гей-Люссаком был проведен опыт по сжиганию щелочных металлов с избытком кислорода, в результате чего был получен пероксид натрия. Но пероксид водорода был получен позже, лишь в 1818 году, когда Луи Тенар изучал воздействие кислот на металлы; для их устойчивого взаимодействия было необходимо низкое количество кислорода. Проводя подтверждающий опыт с перекисью бария и серной кислотой, ученый добавил к ним воду, хлористый водород и лёд. Через непродолжительное время, Тенар обнаружил на стенках емкости с пероксидом бария небольшие застывшие капли. Стало ясно, что это H2O2. Тогда дали полученному H2O2 название «окисленная вода». Это и была перекись водорода — бесцветная, ничем не пахнущая, трудноиспаримая жидкость, хорошо растворяющая другие вещества. Результат взаимодействия H2O2 и H2O2 — реакция диссоциации, перекись растворима в воде.
Интересный факт – быстро обнаружились свойства нового вещества, позволяющие использовать его в реставрационных работах. Сам Тенар при помощи пероксида отреставрировал картину Рафаэля, потемневшую от времени.
Перекись водорода в XX веке
После тщательного изучения полученного вещества его стали производить в промышленных масштабах. В начале двадцатого века ввели электрохимическую технологию производства перекиси, основанную на процессе электролиза. Но срок годности полученного таким методом вещества был невелик, около пары недель. Чистая перекись нестабильна, и по большей части её выпускали в тридцатипроцентной концентрации для отбеливания ткани и в трёх- или шестипроцентной – для бытовых нужд.
Учёные фашистской Германии использовали пероксид для создания ракетного двигателя на жидком топливе, который использовался для оборонных нужд во Второй Мировой войне. В результате взаимодействия Н2О2 и метанола/гидразина, получалось мощное топливо, на котором самолет достигал скорости более 950 км/ч.
Где применяется Н2О2 сейчас?
- в медицине — для обработки ран;
- в целлюлозно-бумажной промышленности используются отбеливающие свойства вещества;
- в текстильной промышленности перекисью отбеливают натуральные и синтетические ткани, меха, шерсть;
- как ракетное топливо или его окислитель;
- в химии — для получения кислорода, как пенообразователь для производства пористых материалов, как катализатор или гидрирующий агент;
- для производства дезинфицирующих или чистящих средств, отбеливателей;
- для обесцвечивания волос (это устаревший метод, так как волосы сильно повреждаются пероксидом);
- некоторые используют перекись для отбеливания зубов, но при этом разрушается их эмаль;
- в аквариумистике и рыбных хозяйствах используют трёхпроцентный раствор Н2О2 для оживления задохнувшихся рыб, для уничтожения водорослей и паразитов в аквариуме, а также для борьбы с некоторыми заболеваниями рыбы;
- во всех отраслях пероксид может применяться как средство дезинфекции поверхностей, оборудования, упаковки;
- для чистки бассейнов;
- для добычи металлов и нефти в горно- и нефтедобывающей промышленности;
- для обработки металлов и сплавов в металлообработке.
Применение Н2О2 в быту
Перекись водорода можно успешно применять для решения разных бытовых задач. Но использовать в этих целях можно лишь трёхпроцентную перекись водорода. Вот некоторые способы:
- Для очистки поверхностей нужно залить перекись в сосуд пульверизатором и разбрызгивать на загрязненные места.
- Для дезинфекции предметов их нужно протереть неразбавленным раствором Н2О2. Это поможет очистить их от вредных микроорганизмов. Губки для мытья можно замочить в воде с перекисью (пропорция 1:1).
- Для отбеливания тканей при стирке белых вещей добавляют стакан пероксида. Можно также выполоскать белые ткани в воде, смешанной со стаканом Н2О2. Этот способ возвращает белизну, предохраняет ткани от пожелтения и помогает удалить трудновыводимые пятна.
- Для борьбы с плесенью и грибком следует смешать в емкости с пульверизатором перекись и воду в пропорции 1:2. Полученную смесь распылять на зараженные поверхности и через 10 минут очищать их при помощи щётки или губки.
- Обновить потемневшую затирку в кафельной плитке можно, распылив пероксид на нужные участки. Через 30 минут нужно тщательно потереть их жесткой щёткой.
- Для мытья посуды полстакана Н2О2 добавить в полный таз с водой (или раковину с закрытым сливом). Промытые в таком растворе чашки и тарелки будут сиять чистотой.
- Чтобы очистить зубную щётку, нужно опустить её в неразведенный трёхпроцентный раствор перекиси. Затем промыть под сильной струей воды. Этот способ хорошо дезинфицирует предмет гигиены.
- Чтобы продезинфицировать купленные овощи и фрукты, следует распылить на них раствор 1 части перекиси и 1 части воды, после чего тщательно промыть их водой (можно холодной).
- На дачном участке при помощи Н2О2 можно бороться с болезнями растений. Нужно опрыскивать их раствором перекиси или замочить семена незадолго до посадки в 4,5 литрах воды, смешанной с 30 мл сорокапроцентной перекиси водорода.
- Для оживления аквариумных рыбок, если они отравились аммиаком, задохнулись при отключении аэрации или по другой причине, можно попробовать поместить их в воду с перекисью водорода. Нужно смешать трёхпроцентную перекись с водой из расчёта 30 мл на 100 литров и поместить в полученную смесь бездыханных рыб на 15-20 минут. Если они не оживут за это время, значит, средство не помогло.
Перекись водорода в природе
Не стоит считать пероксид водорода искусственным соединением, получаемым только в лабораториях. В Н2О2 содержится в дожде и снеге, в горном воздухе. В горах можно встретить источники и реки с белой от мельчайших кислородных пузырьков водой, которая справедливо считается полезной. Мало кто знает, что цвет и пузырьки обусловлены наличием в воде Н2О2, образующейся из-за хорошей её аэрации. Между тем, не стоит бояться пить такую воду некипяченой, если, разумеется, поблизости нет заводов и фабрик. Перекись водорода, естественным путем образующаяся в воде, служит обеззараживающим средством против микроорганизмов и паразитов.
Даже в результате активного встряхивания бутылки с водой в ней образуется некоторое количество пероксида, так как вода при этом действии насыщается кислородом.
В свежих фруктах и овощах Н2О2 также содержится, пока они не подвергнутся термической обработке. При нагреве, варке, обжарке и других процессах с сопутствующей высокой температурой уничтожается большое количество кислорода. Именно поэтому прошедшие кулинарную обработку продукты считаются не такими полезными, хотя какое-то количество витаминов в них остается. Свежевыжатые соки или кислородные коктейли, подаваемые в санаториях, полезны по той же причине – из-за насыщения кислородом, который дает организму новые силы и очищает его.
Опасность перекиси при употреблении внутрь
После вышесказанного может показаться, что перекись можно специально принимать внутрь, и от этого будет польза организму. Но это совсем не так. В воде или соках соединение содержится в минимальных количествах и тесно связано с другими веществами. Прием же «ненатуральной» перекиси водорода внутрь (а вся перекись, купленная в магазине или произведенная в результате химических опытов самостоятельно, никак не может считаться натуральной, к тому же обладает слишком высокой концентрацией по сравнению с природной) может привести к опасным для жизни и здоровья последствиям. Чтобы понять — почему, нужно вновь обратиться к химии.
Как уже упомянуто, при некоторых условиях пероксид водорода разрушается и выделяет кислород, являющийся активным окислителем. Например, реакция разложения может произойти при столкновении Н2О2 с пероксидазой – внутриклеточным ферментом. В основе использования перекиси для дезинфекции положены именно её окислительные свойства. Так, когда рану обрабатывают Н2О2 – выделяющийся кислород уничтожает живые патогенные микроорганизмы, попавшие в нее. Такое же действие она оказывает и на другие живые клетки. Если обработать неповрежденную кожу пероксидом, а потом протереть место обработки спиртом, почувствуется жжение, что подтверждает наличие микроскопических повреждений после перекиси. Но при внешнем применении перекиси низкой концентрации какого-то заметного вреда организму не будет.
Другое дело, если её пытаться принимать внутрь. То вещество, которое способно повреждать даже сравнительно толстую кожу снаружи, попадает на слизистые оболочки пищеварительного тракта. То есть происходят химические мини-ожоги. Разумеется, выделяющийся окислитель – кислород – может заодно убить и вредные микробы. Но этот же процесс произойдет и с клетками пищевого тракта. Если ожоги в результате действия окислителя будут повторяться, то возможна атрофия слизистых оболочек, а это – первый шаг на пути к раку. Гибель клеток кишечника приводит к невозможности организма усваивать питательные вещества, этим объясняется, например, снижение веса и исчезновение запоров у некоторых людей, практикующих «лечение» перекисью.
Отдельно нужно сказать о таком методе употребления перекиси, как внутривенные инъекции. Даже если по какой-то причине их назначил врач (оправдано это может быть лишь при заражении крови, когда других подходящих лекарств в наличии нет), то под медицинским наблюдением и со строгим расчетом дозировок риски все-таки есть. Но в такой экстремальной ситуации это будет шансом на выздоровление. Самому же назначать себе уколы перекиси водорода ни в коем случае нельзя. Н2О2 представляет большую опасность для клеток крови – эритроцитов и тромбоцитов, так как при попадании в кровеносное русло разрушает их. К тому же, может произойти смертельно опасная закупорка сосудов высвободившимся кислородом – газовая эмболия.
Меры безопасности в обращении с Н2О2
- Хранить в недоступном для детей и недееспособных лиц месте. Отсутствие запаха и выраженного вкуса делает перекись особенно опасной для них, так как могут быть приняты большие дозы. При попадании внутрь раствора, последствия употребления могут быть непредсказуемыми. Необходимо незамедлительно обратиться к врачу.
- Растворы перекиси концентрацией более трёх процентов вызывают ожоги при попадании на кожу. Место ожога нужно промыть большим количеством воды.
- Не допускать попадания раствора пероксида в глаза, так как образуется их отек, покраснение, раздражение, иногда болевые ощущения. Первая помощь до обращения к врачу – обильное промывание глаз водой.
- Хранить вещество так, чтобы было понятно, что это — H2O2, то есть в емкости с наклейкой во избежание случайного применения не по назначению.
- Условия хранения, продлевающие его срок, – темное, сухое, прохладное место.
- Нельзя смешивать пероксид водорода с любыми жидкостями, кроме чистой воды, в том числе и с хлорированной водой из-под крана.
- Все вышесказанное применимо не только к Н2О2, но и ко всем содержащим его препаратам.
http://gomolog.ru/reshebniki/8-klass/gabrielyan-2013/41/3.html
http://fb.ru/article/357616/h-o—chto-eto-za-veschestvo