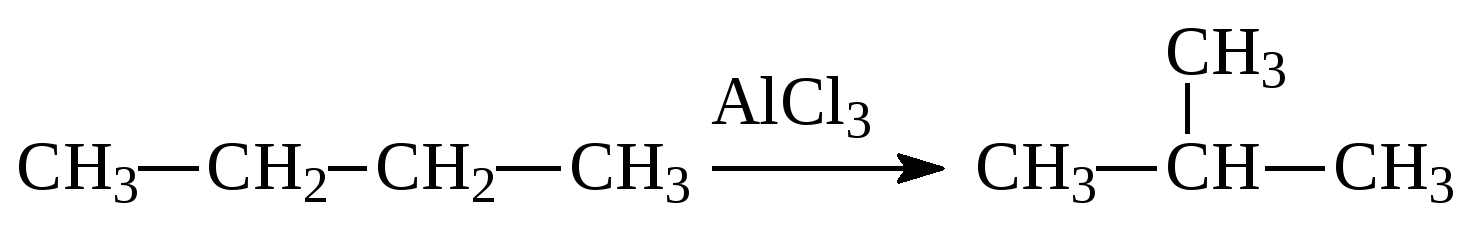Характеристика реакции, уравнение которой 4KClO3 → 2KCl + 3O2: А) Соединения, ОВР; Б) Замещения ОВР; В) Обмена не ОВР; Г) Разложения ОВР.
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,298
- гуманитарные 33,622
- юридические 17,900
- школьный раздел 607,232
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Контрольная работа — Химические реакции
учебно-методический материал по химии (11 класс) по теме
Контрольная работа — Химические реакции
Скачать:
| Вложение | Размер |
|---|---|
| kontrolnaya_rabota_-_khimicheskie_reaktsii.doc | 317 КБ |
Предварительный просмотр:
Х–11 Контрольная работа №2 «Химические реакции» Вариант №1
При выполнении заданий А1-А10 из предложенных вариантов ответов выберите тот, который вы считаете правильным. 2 балла за каждое верно выполненное задание.
А1. Характеристика реакции, уравнение которой 4Fe + 6H 2 O + 3O 2 →4Fe(OH) 3 :
1) Соединения, ОВР 2) Замещения ОВР 3) Обмена не ОВР 4) Разложения ОВР
А2. Какая масса угля вступает в реакцию, термохимическое уравнение которой С+О 2 = СО 2 + 402 кДж, если при этом выделилось 1608 кДж теплоты?
1) 4,8 г 2) 48 г 3) 120 г 4) 240 г
А3. Химическая реакция, уравнение которой:
1) Дегидрирования 2) Изомеризации 3) Полимеризации 3) Присоединения
А4. Окислитель в реакции синтеза аммиака, уравнение которой N 2 + 3H 2 = 2NH 3 + Q
1) N 0 2) H 0 3) H +1 4) N –3
А5. При повышении температуры на 30 °С (температурный коэффициент равен 3) скорость увеличится
1) в 3 раза 2) в 9 раз 3) в 27 раз 4) в 81 раз
А6. Факторы, позволяющие сместить химическое равновесие, для реакции CaO(т)+CO 2 (г)↔CaCO 3 (т)+Q, в сторону продуктов реакции:
1) Повышение температуры и понижение давления 2) Понижение температуры и давления
3) Понижение температуры и повышение давления 4) Повышение температуры и давления
А7. Щелочную среду имеет водный раствор соли, формула которой:
1) AlCl 3 2) KNO 3 3) K 2 CO 3 4) FeCl 3
А8. Наиболее сильной кислотой из перечисленных является:
1) H 2 CO 3 2) H 3 PO 4 3) H 2 SO 4 4) H 2 SO 3
А9. Осадок образуется при взаимодействии хлорида калия с:
1) AgNO 3 2) NaOH 3) H 2 SO 4 4) NaCl
А10. Гидролизу не подвергается:
1) ZnSO 4 2) Ba(NO 3 ) 2 3) Na 2 S 4) NH 4 Cl
В заданиях В1-В3 установите соответствие. Ответ запишите в виде последовательности цифр.
4 балла за верно выполненное задание.
В1. Установите соответствие между схемой ОВР и коэффициентом перед формулой восстановителя:
Химические реакции
Контрольная работа по химии для 11 класса по теме «Химические реакции»
Просмотр содержимого документа
«Химические реакции»
Контрольная работа №2 «Химические реакции»
1) Соединения, ОВР 2) Замещения ОВР 3) Обмена не ОВР 4) Разложения ОВР
А2. Какая масса угля вступает в реакцию, термохимическое уравнение которой С+О2 = СО2 + 402 кДж, если при этом выделилось 1608 кДж теплоты?
1) 4,8 г 2) 48 г 3) 120 г 4) 240 г
А3. Химическая реакция, уравнение которой:
1) Дегидрирования 2) Изомеризации 3) Полимеризации 3) Присоединения
1) N 0 2) H 0 3) H +1 4) N –3
А5. При повышении температуры на 30 °С (температурный коэффициент равен 3) скорость увеличится
1) в 3 раза 2) в 9 раз 3) в 27 раз 4) в 81 раз
А6. Факторы, позволяющие сместить химическое равновесие, для реакции CaO(т)+CO2(г)↔CaCO3(т)+Q, в сторону продуктов реакции:
1) Повышение температуры и понижение давления 2) Понижение температуры и давления
3) Понижение температуры и повышение давления 4) Повышение температуры и давления
А7. Щелочную среду имеет водный раствор соли, формула которой:
А8. Наиболее сильной кислотой из перечисленных является:
А9. Осадок образуется при взаимодействии хлорида калия с:
А10. Гидролизу не подвергается:
В1. Установите соответствие между схемой ОВР и коэффициентом перед формулой восстановителя:
http://nsportal.ru/shkola/khimiya/library/2013/09/05/kontrolnaya-rabota-khimicheskie-reaktsii
http://multiurok.ru/files/khimicheskie-reaktsii-1.html