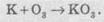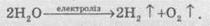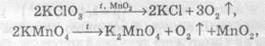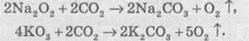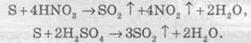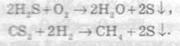Химические свойства кислорода и озона уравнения
4 объемы кислорода в 100 объемах воды
45 объемов озона в 100 объемах воды
Жидкий и твердый кислород — парамагнитные вещества, т.е. втягиваются в магнитное поле
Имеет диамагнитные свойства, то есть не взаимодействует с магнитным полем
Необходим для дыхания растений и животных (в смеси с азотом или инертным газом). Вдыхание чистого кислорода приводит к сильному отравлению
В атмосфере образует так называемый озоновый слой, который защищает биосферу от вредного воздействия ультрафиолетового излучения. Ядовитый
Химические свойства кислорода и озона
Взаимодействие кислорода с металлами
Молекулярный кислород — довольно сильный окислитель. Он окисляет практически все металлы (кроме золота и платины). Много металлов медленно окисляются на воздухе, но в атмосфере чистого кислорода сгорают очень быстро, при этом образуется оксид:
Однако некоторые металлы при горении образуют не оксиды, а пероксиды (в таких соединениях степень окисления Кислорода равна -1) или надпероксиди (степень окисления атома Кислорода — дробная). Примером таких металлов могут быть барий, натрий и калий:
Взаимодействие кислорода с неметаллами
Оксиген проявляет степень окисления -2 в соединениях, которые образованы со всеми неметаллами, кроме Фтора, Гелия, Неона и Аргона. Молекулы кислорода при нагревании непосредственно вступают во взаимодействие со всеми неметаллами, кроме галогенов и инертных газов. В атмосфере кислорода фосфор самовоспламеняется и некоторые другие неметаллы:
При взаимодействия кислорода с фтором образуется кислород фторид, а не фтор оксид, поскольку атом Фтора имеет большую электроотрицательности, чем атом Кислорода. Оксиген фторид — это газ бледно-желтого цвета. Его используют как очень сильный окислитель и фторувальний агент. В этой соединении степень окисления Кислорода равна +2.
В избытка фтора может образовываться диоксиген дифторид, в котором степень окисления Кислорода равна +1. По строению такая молекула похожа на молекулу водород пероксида.
По определенных условиях кислород вступает во взаимодействие со многими сложными веществами. При этом образуются оксиды элементов, простые вещества, образованные этими элементами:
Кислород может вступать во взаимодействие с оксидами, в которых элементы находятся не в высших степенях окисления:
Озон является более сильным окисником, чем молекулярный кислород. Почти все реакции, которые проходят под действием кислорода, проходят также с озоном, но при этом реакция протекает быстрее и выделяется большее количество энергии. Многие вещества под действием озона занимаются:
При взаимодействия калия с озоном образуется озонід (соединение ионного типа):
Озон обнаруживают в лабораторных условиях пропусканием исследуемой смеси через раствор калий йодида с небольшим количеством крахмала:
Если в пропущенной газовой смеси присутствует озон, то раствор окрашивается в интенсивно-синий цвет, за счет образования комплексного соединения йода с крахмалом. Эту реакцию называют качественной реакцией на озон.
Кислород в аналогичную реакцию не вступает.
Кислород обычно добывают в лабораториях электролизом слабого водного раствора натрий гидроксида (никелированные электроды):
Кислород можно добыть термическим разложением богатых Оксиген соединений (хлоратов, перманганатів, нитратов, пероксидов, оксидов):
В промышленности кислород получают из жидкого воздуха. Сначала воздух охлаждают до -200 °С, а затем постепенно нагревают. При -196 °С испаряется азот, и остается жидкий кислород.
Методы добывания озона
Озон образуется в атмосфере на высоте 20 — 30 километров из кислорода под действием ультрафиолетового излучения Солнца.
Озон можно добыть из кислорода под действием тлеющего электрического разряда.
Он также образуется в различных копировальных аппаратах, при сварке металлов, при работе трансформаторов и при ударе молнии.
Применение кислорода и озона. Значение озонового слоя
Кислород используют все аэробные живые существа для дыхания. В процессе фотосинтеза растения выделяют кислород и поглощают углекислый газ.
Молекулярный кислород применяют для так называемой интенсификации, то есть ускорение окислительных процессов в металлургической промышленности. А еще кислород используют для добывания пламени с высокой температурой. При горении ацетилена (С2Н2) в кислороде температура пламени достигает 3500 °С. В медицине кислород применяют для облегчения дыхания больных. Его также используют в дыхательных аппаратах для работы людей в трудной для дыхания атмосфере. Жидкий кислород применяют как окислитель ракетного топлива.
Озон используют в лабораторной практике как очень сильный окислитель. В промышленности с его помощью дезинфицируют воду, поскольку ему присуща сильная окислительная действие, которая уничтожает различные микроорганизмы.
Пероксиды, надпероксиди и озонидов щелочных металлов применяют для регенерации кислорода в космических кораблях и на подводных лодках, Такое применение основано на реакции этих веществ с углекислым газом СО2:
В природе озон содержится в высоких слоях атмосферы на высоте около 20-25 км, в так называемом озоновом слое, который защищает Землю от жесткого солнечного излучения. Уменьшение концентрации озона в стратосфере хотя бы на 1 может привести к тяжелым последствиям, таким рост числа онкологических заболеваний кожи в людей и животных, увеличение числа заболеваний, связанных с угнетением иммунной системы человека, замедление роста наземных растений, снижение скорости роста фитопланктона и т.д.
Без озонового слоя жизнь на планете было бы невозможным. Тем временем загрязнение атмосферы различными промышленными выбросами приводят к разрушению озонового слоя. Самыми опасными веществами для озона являются фреоны (их используют как хладагенты в холодильных машинах, а также как наполнители для баллончиков с дезодорантами) и отходы ракетного топлива.
Мировое сообщество очень обеспокоено в связи с образованием дыры в озоновом слое на полюсах нашей планеты, в связи с чем в 1987 г. был принят «Монреальский протокол по веществам, разрушающим озоновый слой», который ограничил использование веществ, вредных для озонового слоя.
Физические свойства веществ, образованных элементом Сульфуром
Атомы Серы, так же, как и Кислорода, могут образовывать различные аллотропные модификации ( S ∞ ; S 12 ; S 8 ; S 6 ; S 2 и другие). При комнатной температуре сера находится в виде α -серы (или ромбической серы), что представляет собой желтые хрупкие кристаллы, без запаха, не растворимые в воде. При температуре свыше +96 °С происходит медленный переход α -серы в β -серу (или моноклінну серу), что представляет собой почти белые пластинки. Если расплавленную серу перелить в воду, происходит переохлаждение жидкой серы и образования желто-коричневой резино-подобной пластической серы, которая погодя снова превращается в а-серу. Сера кипит при температуре, равной +445 °С, образуя пары темно-бурого цвета.
Все модификации серы не растворяются в воде, зато достаточно хорошо растворяются в сероуглероде ( CS 2 ) и некоторых других неполярных растворителях.
Простая вещество сера при нагревании взаимодействует практически со всеми металлами, за исключением золота, иридия и платины. При этом образуются сульфиды соответствующих металлов. В сульфідах степень окисления Серы равна -2:
Под нагревании сера реагирует со многими неметаллами. При горении на воздухе образуется сульфур(И V ) оксид:
При нагревании серы в потоке водорода образуется сероводород. В сероводороде Сульфур находится в степени окисления-2. Такой же степень окисления Сульфур проявляет и в сероуглероде, который образуется при взаимодействии серы и углерода:
Взаимодействие серы со сложными веществами
Простая вещество сера вступает в реакции с сильными окислителями, при этом чаще всего окисляется до сульфура диоксида:
При кипячении с раствором щелочи образуется сульфид и сульфат, то есть проходит реакция диспропорціонування:
В этом случае в исходном состоянии степень окисления Серы равна 0. В натрий сульфаті ( N a 2 SO 4 ) степень окисления Серы равна +6, а в натрий сульфіді ( Na 2 S ) -2, т.е. произошла реакция дислропорціонування.
В промышленных масштабах серу добывают из самородных подземных залежей методом выплавки ее перегретым водяным паром с последующей перегонкой полученного продукта.
Серу можно добывать также частичным окисненням сероводорода или неполным восстановлением сероуглерода:
Главный продукт серной промышленности — это сульфатная кислота. На ее производство приходится около 60 % серы, которую добывают. В гумотехнічній промышленности серу используют для превращения каучука в высококачественную резину, то есть для вулканизации каучука. Сера — важнейший компонент любых пиротехнических смесей. Например, в спичечных головках содержится около 5 %, а в намазці на коробке — около 20 % серы по массе. В сельском хозяйстве серу используют для борьбы с вредителями виноградников. В медицине серу применяют при изготовлении различных мазей для лечения кожных заболеваний.
Кислород: химия кислорода
Кислород
Положение в периодической системе химических элементов
Кислород расположен в главной подгруппе VI группы (или в 16 группе в современной форме ПСХЭ) и во втором периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение кислорода
Электронная конфигурация кислорода в основном состоянии :
+8O 1s 2 2s 2 2p 4 1s 

Атом кислорода содержит на внешнем энергетическом уровне 2 неспаренных электрона и 2 неподеленные электронные пары в основном энергетическом состоянии.
Физические свойства и нахождение в природе
Кислород О2 — газ без цвета, вкуса и запаха, немного тяжелее воздуха. Плохо растворим в воде. Жидкий кислород – голубоватая жидкость, кипящая при -183 о С.
Озон О3 — при нормальных условиях газ голубого цвета со специфическим запахом, молекула которого состоит из трёх атомов кислорода.
Кислород — это самый распространённый в земной коре элемент. Кислород входит в состав многих минералов — силикатов, карбонатов и др. Массовая доля элемента кислорода в земной коре — около 47 %. Массовая доля элемента кислорода в морской и пресной воде составляет 85,82 %.
В атмосфере содержание свободного кислорода составляет 20,95 % по объёму и 23,10 % по массе.
Способы получения кислорода
В промышленности кислород получают перегонкой жидкого воздуха.
Лабораторные способы получения кислорода:
- Разложение некоторых кислородосодержащих веществ:
Разложение перманганата калия:
Разложение бертолетовой соли в присутствии катализатора MnO2 :
2KClO3 → 2KCl + 3O2
Разложение пероксида водорода:
2HgO → 2Hg + O2
Соединения кислорода
Основные степени окисления кислород +2, +1, 0, -1 и -2.
| Степень окисления | Типичные соединения |
| +2 | Фторид кислорода OF2 |
| +1 | Пероксофторид кислорода O2F2 |
| -1 | Пероксид водорода H2O2 Пероксид натрия Na2O2 и др. |
| -2 | Вода H2O Оксиды металлов и неметаллов Na2O, SO2 и др. Соли кислородсодержащих кислот Кислородсодержащие органические вещества Основания и амфотерные гидроксиды |
Химические свойства
При нормальных условиях чистый кислород — очень активное вещество, сильный окислитель. В составе воздуха окислительные свойства кислорода не столь явно выражены.
1. Кислород проявляет свойства окислителя (с большинством химических элементов) и свойства восстановителя (только с более электроотрицательным фтором). В качестве окислителя кислород реагирует и с металлами , и с неметаллами . Большинство реакций сгорания простых веществ в кислороде протекает очень бурно, иногда со взрывом.
1.1. Кислород реагирует с фтором с образованием фторидов кислорода:
С хлором и бромом кислород практически не реагирует, взаимодействует только в специфических очень жестких условиях.
1.2. Кислород реагирует с серой и кремнием с образованием оксидов:
1.3. Фосфор горит в кислороде с образованием оксидов:
При недостатке кислорода возможно образование оксида фосфора (III):
Но чаще фосфор сгорает до оксида фосфора (V):
1.4. С азотом кислород реагирует при действии электрического разряда, либо при очень высокой температуре (2000 о С), образуя оксид азота (II):
N2 + O2→ 2NO
1.5. В реакциях с щелочноземельными металлами, литием и алюминием кислород также проявляет свойства окислителя. При этом образуются оксиды:
2Ca + O2 → 2CaO
Однако при горении натрия в кислороде преимущественно образуется пероксид натрия:
2Na + O2→ Na2O2
А вот калий, рубидий и цезий при сгорании образуют смесь продуктов, преимущественно надпероксид:
K + O2→ KO2
Переходные металлы окисляются кислород обычно до устойчивых степеней окисления.
Цинк окисляется до оксида цинка (II):
2Zn + O2→ 2ZnO
Железо , в зависимости от количества кислорода, образуется либо оксид железа (II), либо оксид железа (III), либо железную окалину:
2Fe + O2→ 2FeO
4Fe + 3O2→ 2Fe2O3
3Fe + 2O2→ Fe3O4
1.6. При нагревании с избытком кислорода графит горит , образуя оксид углерода (IV):
при недостатке кислорода образуется угарный газ СО:
2C + O2 → 2CO
Алмаз горит при высоких температурах:
Горение алмаза в жидком кислороде:
Графит также горит:
Графит также горит, например, в жидком кислороде:
Графитовые стержни под напряжением:
2. Кислород взаимодействует со сложными веществами:
2.1. Кислород окисляет бинарные соединения металлов и неметаллов: сульфиды, фосфиды, карбиды, гидриды . При этом образуются оксиды:
4FeS + 7O2→ 2Fe2O3 + 4SO2
Ca3P2 + 4O2→ 3CaO + P2O5
2.2. Кислород окисляет бинарные соединения неметаллов:
- летучие водородные соединения ( сероводород, аммиак, метан, силан гидриды . При этом также образуются оксиды:
2H2S + 3O2→ 2H2O + 2SO2
Аммиак горит с образованием простого вещества, азота:
4NH3 + 3O2→ 2N2 + 6H2O
Аммиак окисляется на катализаторе (например, губчатое железо) до оксида азота (II):
4NH3 + 5O2→ 4NO + 6H2O
- прочие бинарные соединения неметаллов — как правило, соединения серы, углерода, фосфора ( сероуглерод, сульфид фосфора и др.):
CS2 + 3O2→ CO2 + 2SO2
- некоторые оксиды элементов в промежуточных степенях окисления ( оксид углерода (II), оксид железа (II) и др.):
2CO + O2→ 2CO2
2.3. Кислород окисляет гидроксиды и соли металлов в промежуточных степенях окисления в водных растворах.
Например , кислород окисляет гидроксид железа (II):
Кислород окисляет азотистую кислоту :
2.4. Кислород окисляет большинство органических веществ. При этом возможно жесткое окисление (горение) до углекислого газа, угарного газа или углерода:
CH4 + 2O2→ CO2 + 2H2O
2CH4 + 3O2→ 2CO + 4H2O
CH4 + O2→ C + 2H2O
Также возможно каталитическое окисление многих органических веществ (алкенов, спиртов, альдегидов и др.)
Химические свойства кислорода и озона: взаимодействие с простыми веществами
Разделы: Химия
Класс: 8
Цели урока
- экспериментально изучить взаимодействие кислорода с простыми веществами;
- родолжить отработку навыка составления уравнений реакций, формул соединений по валентности;
- продолжить формирование умений наблюдения, умений формулировать выводы.
К уроку — колбы, наполненные кислородом, сера, красный фосфор, уголь древесный, железная игла, тигельные щипцы, спиртовка, спички, ложечки для сжигания веществ, стаканчик с водой, пинцет.
Компьютерная презентация, распечатки заданий на столах.
Ход урока
На столах – распечатки.
Ответьте на вопросы следующим образом: верно “+”, неверно “-”.
1 вариант.
- Реакция соединения- это всегда реакция получения сложного вещества.
- Кислород составляет основную часть атмосферы.
- Бинарные соединения элементов с кислородом называются оксидами.
- В процессе фотосинтеза поглощается углекислый газ и выделяется кислород.
- Кислород легче воздуха
- Озон и кислород – это разные названия одного и того же вещества.
2 вариант.
- Реакция разложения — это всегда реакция получения простого вещества.
- Бинарные соединения элементов с кислородом называются сульфидами
- Кислород составляет одну пятую часть атмосферы
- В процессе фотосинтеза выделяется углекислый газ и поглощается кислород.
- Кислород тяжелее воздуха.
- Озон и кислород – это аллотропные модификации одного и того же элемента.
У доски — решаем задачи.
1. Какой из оксидов железа содержит больше кислорода- FeO или Fe2O3?
2. Вычислите объём кислорода, содержащегося в классе у первоклашек (в 1-1) после трёх уроков, если площадь класса 500 м 3 , а в течении каждого урока первоклашки вместе с учителем расходуют 10 л кислорода. Как пополнить запас кислорода в классе?
Оцениваем работу у доски, работы в тетрадях.
Постановка проблемы.
Давайте поиграем. Я буду называть вещество или тело, а вы, если оно может гореть, хлопаете в ладоши.
Бумага, вода, лёд, дрова, уголь, стекло, спирт, железо…
— Почему не хлопнули? (Почему-то кто-то хлопнул, кто-то нет)
— Давайте проверим, горит ли железо, ведь ещё Адольф Вюрц, немецкий химик, сказал: “В химии нет ничего невозможного”
Демонстрационный опыт- горение железа в кислороде.
— Вижу, вы удивлены. Почему?
— Чего же мы ещё не знаем о кислороде?
— Почему горит железо? Какие будут гипотезы? Предположения?
(Возможный вариант диалога:
— В колбе больше кислорода, чем в воздухе!
— Ну и что, ведь это тот же кислород, вещество –то не изменилось! Или я не права? Что будем делать?)
— Помните афоризм, которому надобно следовать всегда? “Не ошибается только тот, кто ничего не делает”.
-Может быть стоит провести этот же опыт, но с другими веществами? С какими? (с простыми)
— А какие бывают простые вещества? (металлы и неметаллы)
— У меня на столе есть ещё сера, фосфор и углерод (демонстрирую). К какой группе простых веществ их можно отнести? (неметаллы).
— Кто-нибудь знает, горят они или нет? Давайте проверим.
— Как мы будем проверять? (экспериментально)
Только сегодня эксперимент будет демонстрационным, т. к. опыта обращения с кислородом и горючими веществами у вас пока маловато. Но скоро у нас урок- практикум, где я смогу увидеть и оценить сегодняшнюю вашу наблюдательность.
— Кислород- первое вещество, свойства которого нам предстоит изучить. С чего начнём?
(с планирования действий)
— Будем проводить химические реакции со всеми веществами, которые под руку попадутся или же всё-таки выстроим какую-то схему?
Тогда давайте сформулируем тему урока. (Химические свойства кислорода и озона: взаимодействие с простыми веществами)
Демонстрационный опыт: горение фосфора в кислороде и на воздухе.
— Разделите тетрадь на две половинки, пожалуйста.
Как вы думаете, почему?
(вспоминаем об озон — аллотропия, неустойчивость молекул)
| Химические свойства | |
| кислорода | озона |
— Свойства озона будут совершенно другими или всё же похожими на свойства кислорода? Вспомните о трёх “С” химии:
— Запишите уравнение горения фосфора в кислороде.
(Пошаговое комментирование у доски. Понятия – исходные вещества, продукт реакции, валентность, коэффициент, схема реакции, уравнение реакции)
Демонстрационный опыт: горении серы в кислороде и на воздухе, горение угля в кислороде и воздухе (записываем уравнения)
— Теперь пришла пора записать уравнение реакции окисления железа.
Давайте заглянем в учебник (стр. 81). Взгляните на уравнение реакции.
— Что вас удивляет? (дробная валентность железа) Мы с таким явлением сталкиваемся в первый, но поверьте мне,не в последний раз.
Дело в том,что железная окалина представляет собой смешанный оксид (смесь).
— Перенесете эту информацию дома в справочники. А как назовём этот оксид? ( за правильный ответ — орден “Мудрого совёнка)
Вывод: Простые вещества- как металлы, так и неметаллы- вступают в реакцию с кислородом, в результате получаются оксиды, а реакции называются реакциями окисления.
— А как ещё можно назвать увиденные нами реакции ( реакциями горения)
— Ни у кого не возникло вопросов по поводу нашего вывода?
- Все ли простые вещества вступают во взаимодействие с кислородом?
- При каких условиях начинается реакция? Да и почему всё-таки игла сгорела, но не на воздухе?
- И почему сера, фосфор и углерод ведут себя на воздухе совсем не так как в кислороде?
- И что будет, если увеличить содержание кислорода в воздухе до 30%? Или уменьшить до 8%?
- Всегда ли реакции окисления сопровождаются горением?
- Почему мы дышим кислородом? Мы горим !?
Это всё вопросы домашнего задания, поищите информацию в книгах, в Интернете, а на следующем уроке поговорим. Думаю, будет интересно.
— У нас осталась незаполненной половинка листа. О чём нам надо вспомнить? (об озоне)
Мы решили, что его свойства должны быть похожи на свойства кислорода, но только похожи.
Действительно, химические свойства озона отличает чрезвычайно высокая реакционная способность. Озон – один из сильнейших окислителей, за счёт атомарного кислорода, который образуется при распаде озона.
Очень важно помнить, что озон проявляет окислительные свойства уже при комнатной температуре. Так, при работе с озоном нельзя использовать резиновые шланги – они моментально прохудятся. (То есть в кислородной подушке его хранить нельзя).
Записываем уравнения реакций во второй половине тетради, помня о том. что и в реакциях простых веществ с кислородом получаются оксиды, но идут эти реакции гораздо интенсивнее, чем с кислородом.
Итог урока.
- И кислород, и озон вступают в реакции соединения с простыми веществами.
- Реакции соединения кислорода и озона с простыми веществами называются реакциями окисления, а сами кислород и озон называются окислителями.
- В результате этого взаимодействия образуются оксиды.
Закрепление. Упражнение № 8(в тексте учебника, стр. 82)
Какой вывод можно сделать из упражнения?
- В реакциях с озоном Ме проявляют более высокие валентности, чем в реакциях с кислородом
Д/з:$16, стр. 80-82; напишите с/х или сказку, нарисуйте комиксы по свойствам кислорода и озона. Для тех, кто тяготеет к исследовательской работе- проведите мини исследования по вопросам:
- Что будет, если увеличить содержание кислорода в воздухе до 30%? Или уменьшить до 8%?
- Озон-друг или враг?
Изучаем материал внимательно- готовимся к аукциону знаний.
Учебник: Кузнецова Л. М. , Химия-8, М. “Мнемозина”. 2003
http://chemege.ru/kislorod/
http://urok.1sept.ru/articles/419240