Нуклеиновые кислоты: функции и химические свойства
Рост и развитие всех организмов определяются и контролируются генетической программой. Вы уже знаете, что наследственная информация хранится в структуре молекул ДНК (дезоксирибонуклеиновой кислоты). Другие молекулы РНК (рибонуклеиновой кислоты) — участвуют в реализации этой информации, а именно в биосинтезе белка. Оба указанных типа молекул относятся к нуклеиновым кислотам.
Нуклеиновые кислоты — биополимеры, мономерами которых являются нуклеотиды. Нуклеотиды — это органические вещества, состоящие из трех химических компонентов, соединенных ковалентными связями: моносахарида (пентоза), ортофосфорной кислоты и азотсодержащего основания — вещества с циклическим строением молекулы.
Разнообразие нуклеотидов
Все нуклеотиды содержат одинаковые остатки ортофосфорной кислоты. А различаются они углеводными компонентами и азотсодержащими основами. Моносахаридами, входящими в состав нуклеотидов, могут быть рибоза или дезоксирибоза. Нуклеотиды с рибозой образуют молекулы РНК, с дезоксирибозой — ДНК. Азотсодержащие основы, которые могут входить в состав нуклеотидов, называют аденином, тимином, урацилом, цитозином и гуанином. Сокращенно их обозначают первыми буквами названий веществ: А, Т, У, Ц, Г.
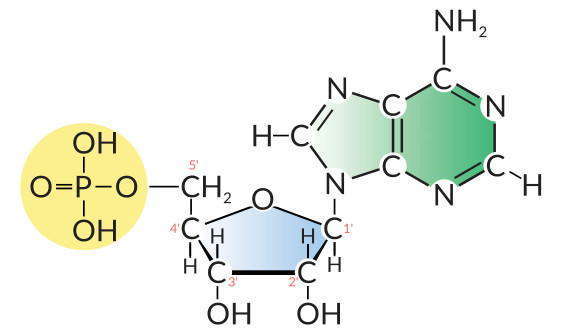
Нуклеотиды способны взаимодействовать друг с другом, формируя длинные цепи. Крепкая ковалентная связь образуется между гидроксильной группой углевода одного нуклеотида и гидроксильной группой ортофосфорной кислоты другого нуклеотида. В результате образованное соединение будет включать с одной стороны остаток ортофосфорной кислоты, а с другой — моносахарида, а потому может взаимодействовать с другим нуклеотидом. Сама молекула ДНК клеток человека содержит последовательно почти 250 млн нуклеотидов. Если эту молекулу развернуть, ее длина составит 85 мм (вспомните для сравнения размеры клетки).
Последовательность «букв» азотсодержащих оснований и является основой кода, которым записана информация в молекулах ДНК и РНК. Как он «работает», мы рассмотрим позже, а теперь рассмотрим особенности строения этих веществ.
Молекула ДНК
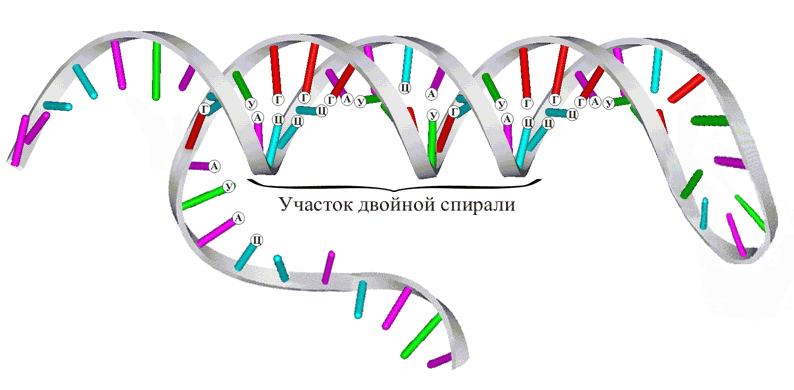
Молекулу ДНК можно представить как двойную спираль: она состоит из двух цепей, закрученные друг вокруг друга. Нуклеотиды обеих цепей расположены так, что азотсодержащие основы одной цепи содержатся напротив азотсодержащих оснований другой, образуя пары. Между основаниями возникают слабые водородные связи. Несмотря на слабость, большое их количество (сотни тысяч и миллионы) приводит к тому, что обе цепи прочно держатся вместе.
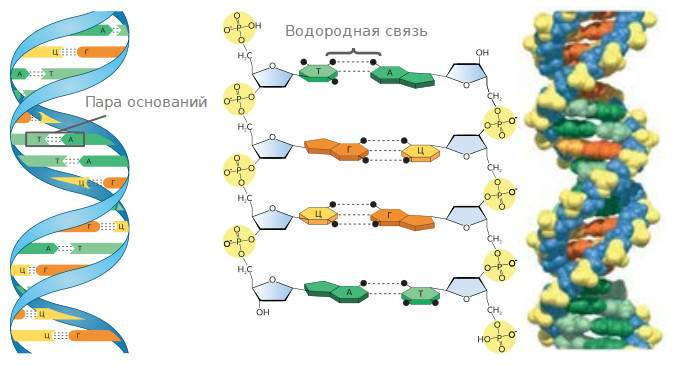
Основы взаимодействуют между собой так, что напротив основы А первой цепи всегда располагается основа Т другой, а напротив Г — всегда Ц. Такое соответствие в расположении нуклеотидов называется комплиментарностью. Эта закономерность имеет важное значение для обеспечения процессов копирования молекул ДНК и переписки с них информации на молекулы РНК. Вместе с тем такая особенность строения молекулы ДНК приводит к тому, что структура первой цепи комплементарно повторяет структуру второй, то есть из последовательности одной из спиралей может восстанавливаться последовательность другой в случае ее разрушения. Это важно для защиты молекулы ДНК от повреждений вследствие негативных химических или физических воздействий. Итак, такое строение молекулы ДНК обеспечивает выполнение своей основной функции — сохранение наследственной информации. В клетках, которые имеют ядра, молекулы ДНК связаны с белками, называемыми гистонами.
Гистоны — большой класс белков ядра клетки, выполняющих две основные функции: они участвуют в упаковке нитей ДНК в ядре клетки и в регуляции процессов в ядре клетки, таких как транскрипция, репликация и репарация. Существует пять различных типов гистонов H1/Н5, H2A, H2B, H3, H4.
Молекула РНК
Молекулы РНК клеток прокариот и эукариот состоят из одной цепи. Существуют три основных типа РНК, которые различаются местоположением в клетке, структурой и функциями в биосинтезе белка. Информационная, или матричная, РНК (иРНК, или мРНК) переносит наследственную информацию от ДНК к месту синтеза полипептидной цепи. Транспортная РНК (тРНК), которая из всех молекул РНК имеет наименьшие размеры (состоит из 70-90 нуклеотидов), транспортирует аминокислоты к месту синтеза белковых молекул. Рибосомная РНК (рРНК) входит в состав особых органических клеток — рибосом, которые обеспечивают синтез белковой молекулы. Бывают и другие типы РНК.
Ядерная ДНК сохраняется в ядре, там же синтезируются молекулы РНК. Далее РНК транспортируются из ядра клетки в цитоплазму, где синтезируются белки. Приводим сравнительную таблицу двух типов нуклеиновых кислот.
| Особенности строения и локализация в клетке | ДНК | РНК |
| Количество цепей | 2 | 1 |
| Нуклеотидный состав полимера (название нуклеотида предоставляется по названию азотсодержащих основы) | (А) Адениловый (Г) Гуаниловый (Т) тимидиловый (Ц) Цитидиловый | (А) Адениловый (Г) Гуаниловый (У) Урациловый (Ц) Цитидиловый |
| Вещества, образующие нуклеотид | Азотсодержащая основа Ортофосфорная кислота Углевод — дезоксирибоза | Азотсодержащая основа Ортофосфорная кислота Углевод — рибоза |
| Локализация в эукариотической клетке | Ядро, Хлоропласты, Митохондрии | Ядро, Цитоплазма, Рибосомы, Хлоропласты, Митохондрии |
Другие функции нуклеотидов. АТФ.
Некоторые нуклеотиды функционируют в клетках не только как мономеры нуклеиновых кислот, а имеют дополнительные, самостоятельные функции.
Самым главным из таких нуклеотидов является АТФ (аденозинтрифосфат). Этот нуклеотид состоит из аденина, рибозы и трех остатков ортофосфорной кислоты. Особенностью строения этой молекулы является то, что для присоединения последующих остатков ортофосфорной кислоты требуется гораздо больше энергии, чем на присоединение первого — так в клетках накапливается энергия. От синтезированной молекулы АТФ путем гидролиза отщепляется третий остаток ортофосфорной кислоты, накопленная энергия высвобождается и используется для осуществления различных процессов (синтез или разложение химических веществ, изменение их структуры, осуществления движений и т.д.). Уравнение такой реакции:
АТФ + Н2O -> АДФ + Н3РO4 + Е (50 кДж / моль),
где АДФ — аденозинтрифосфорная кислота, Е — энергия, выделяющаяся в результате реакции. Образованная АДФ может дальше расщепляться до аденозинмонофосфорной кислоты (АМФ), но во время этой реакции высвобождается меньше энергии (33-42 кДж / моль). Конечный результат реакций — АМФ является обычным РНК-нуклеотидом и не хранит большого количества энергии.
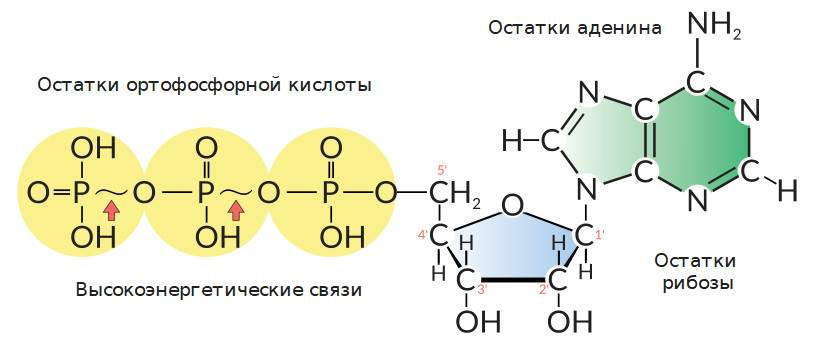
АТФ — это молекула, является универсальным внутриклеточным переносчиком энергии. Молекулы АТФ могут образовываться за счет энергии, которая выделяется в реакциях бескислородного расщепления глюкозы или окисления органических веществ в митохондриях, за счет энергии света в ходе фотосинтеза и др. Расщепление АТФ происходит всегда, когда клетке нужна энергия для осуществления определенной реакции.
Кроме АТФ в клетках «работают» и другие нуклеотиды. К ним относятся никотинамид (НАД) и никотинамид-фосфат (НАДФ). Эти нуклеотиды переносят химические вещества и являются важными для работы митохондрий и фотосинтеза.
НУКЛЕИНОВЫЕ КИСЛОТЫ
НУКЛЕИНОВЫЕ КИСЛОТЫ – биологические полимерные молекулы, хранящие всю информацию об отдельном живом организме, определяющие его рост и развитие, а также наследственные признаки, передаваемые следующему поколению. Нуклеиновые кислоты есть ядрах клеток всех растительных и животных организмов, что определило их название (лат. nucleus – ядро).
Состав полимерной цепи нуклеиновых кислот.
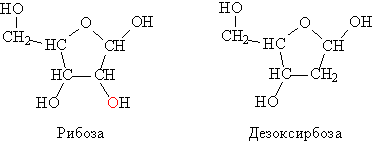
Полимерная цепь нуклеиновых кислот собрана из фрагментов фосфорной кислоты Н3РО3 и фрагментов гетероциклических молекул, представляющих собой производные фурана. Есть лишь два вида нуклеиновых кислот, каждая построена на основе одного из двух типов таких гетероциклов – рибозы или дезоксирибозы (рис. 1).
Рис. 1. СТРОЕНИЕ РИБОЗЫ И ДЕЗОКСИРИБОЗЫ.
Название рибоза (от лат. Rib – ребро, скрепка) имеет окончание – оза, что указывает на принадлежность к классу сахаров (например, глюкоза, фруктоза). У второго соединения нет группы ОН (окси-группа), которая в рибозе отмечена красным цветом. В связи с этим втрое соединение называют дезоксирибозой, т.е., рибоза, лишенная окси-группы.
Полимерная цепь, построенная из фрагментов рибозы и фосфорной кислоты, представляет собой основу одной из нуклеиновых кислот – рибонуклеиновой кислоты (РНК). Термин «кислота» в названии этого соединения употреблен потому, что одна из кислотных групп ОН фосфорной кислоты остается незамещенной, что придает всему соединению слабокислый характер. Если вместо рибозы в образовании полимерной цепи участвует дезоксирибоза, то образуется дезоксирибонуклеиновая кислота, для которой повсеместно принято широко известное сокращение ДНК.
Структура ДНК.
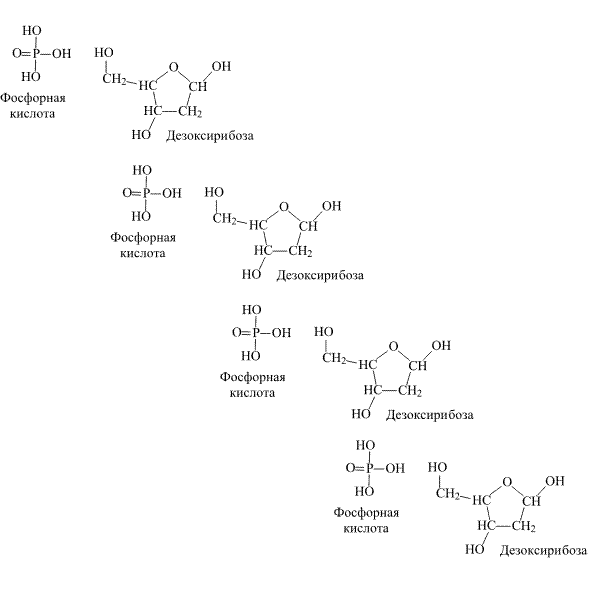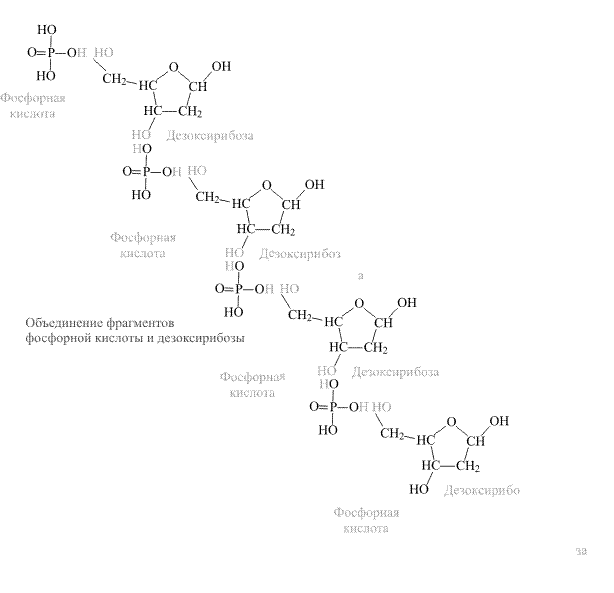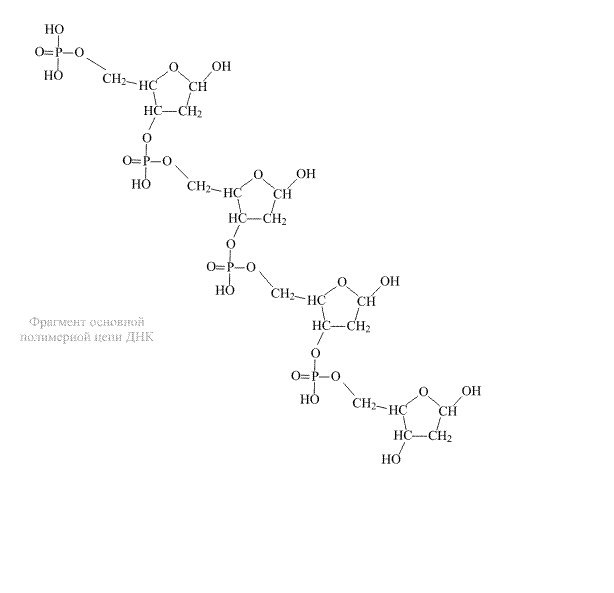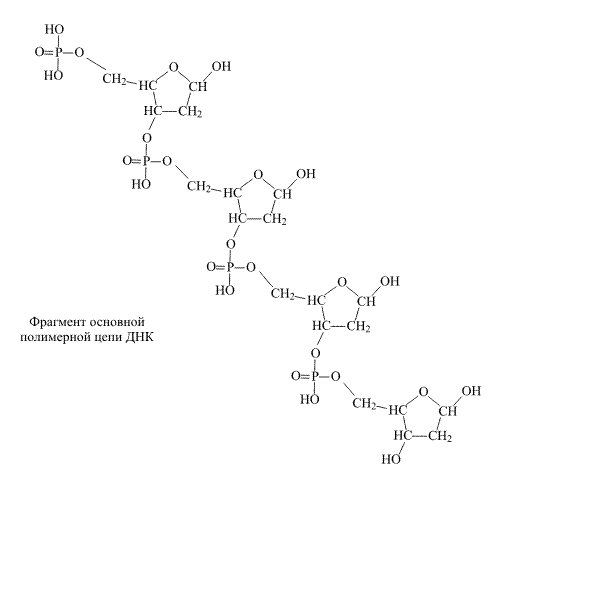
Молекула ДНК служит отправной точкой в процессе роста и развития организма. На рис. 2 показано, как объединяются в полимерную цепь два типа чередующихся исходных соединений, показан не способ синтеза, а принципиальная схема сборки молекулы ДНК.
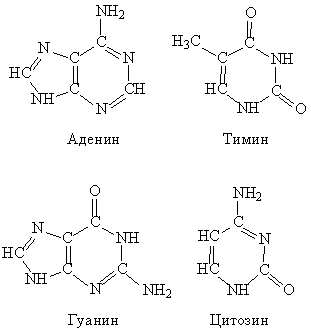
В окончательном варианте полимерная молекула ДНК содержит в боковом обрамлении азотсодержащие гетероциклы. В образовании ДНК участвуют четыре типа таких соединений, два из них представляют собой шестичленные циклы, а два – конденсированные циклы, где шестичленное кольцо спаяно с пятичленным (рис. 3).
Рис. 3. СТРОЕНИЕ АЗОТСОДЕРЖАЩИХ ГЕТЕРОЦИКЛОВ, входящих в состав ДНК
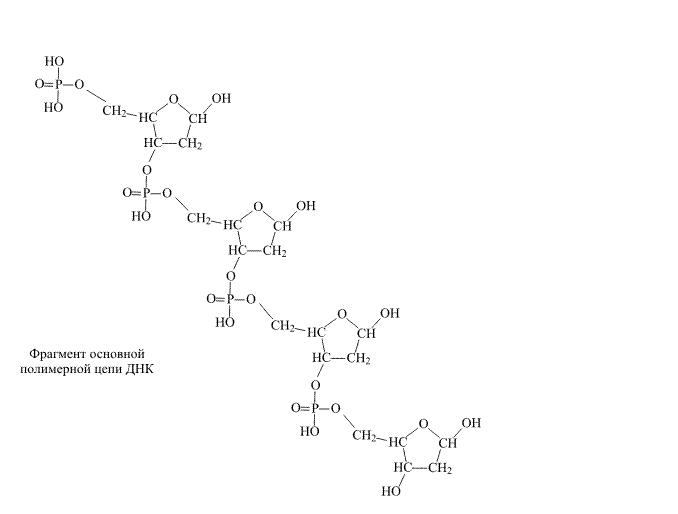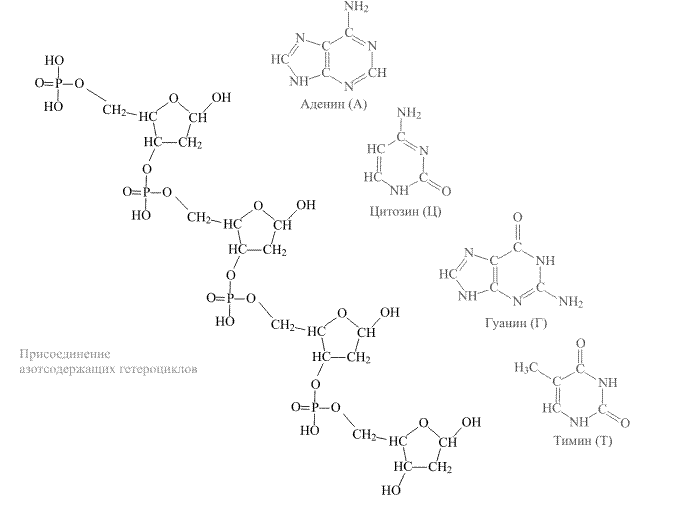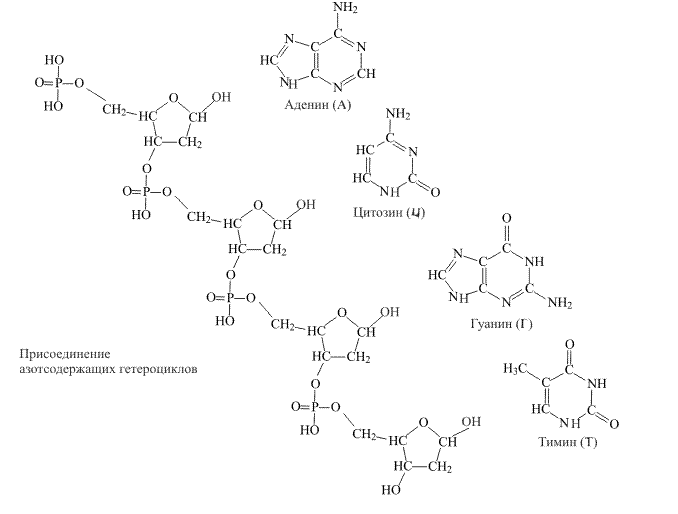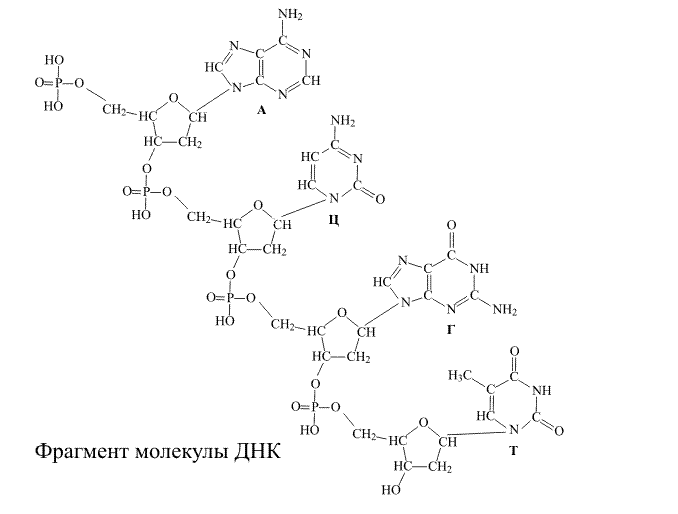
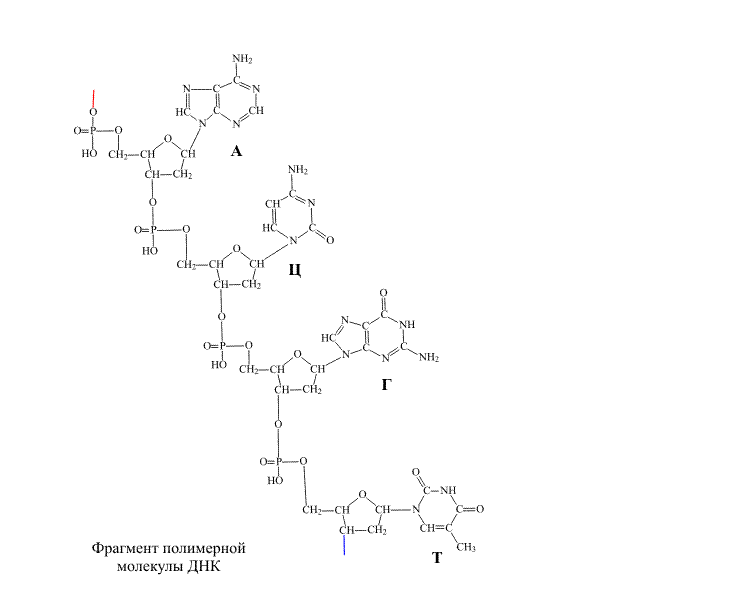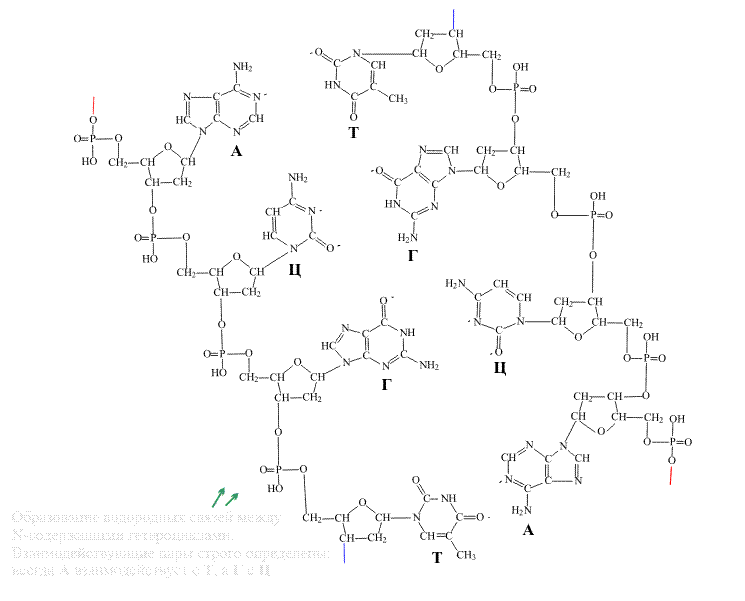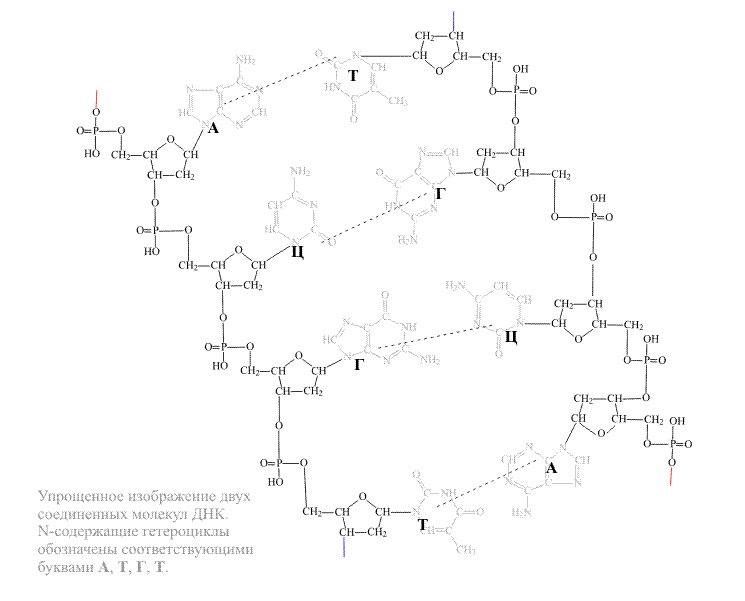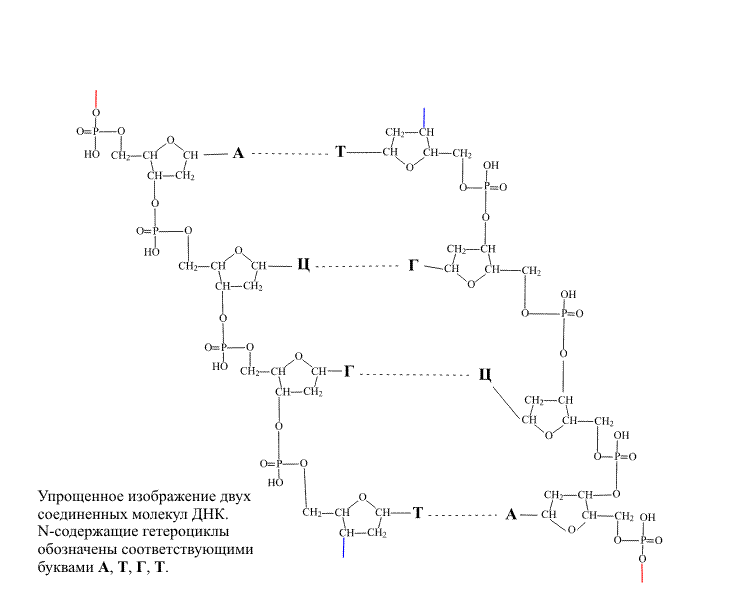
На втором этапе сборки к свободным группам ОН дезоксирибозы присоединяются показанные выше азотсодержащие гетероциклические соединения, образуя у полимерной цепи боковые подвески (рис. 4).
Присоединенные к полимерной цепи молекулы аденина, тимина, гуанина и цитозина обозначают первыми буквами названий исходных соединений, то есть, А, Т, Г и Ц.
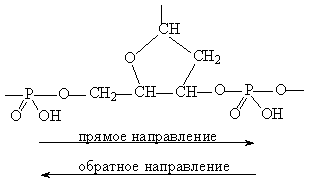
Сама полимерная цепь ДНК имеет определенную направленность – при мысленном продвижении вдоль молекулы в прямом и обратном направлении одни и те же группировки, входящие в состав цепи, встречаются на пути в разной последовательности. При движении в одном направлении от одного атома фосфора к другому вначале на пути следования идет группа СН2, а затем две группы СН (атомы кислорода можно не принимать во внимание), при движении в противоположном направлении последовательность этих групп будет обратной (рис. 5).
Рис. 5. НАПРАВЛЕННОСТЬ ПОЛИМЕРНОЙ ЦЕПИ ДНК. При описании того, в каком порядке чередуются присоединенные гетероциклы, принято использовать прямое направление, то есть от группы СН2 к группам СН.
Само понятие «направление цепи» помогает понять то, как располагаются две цепи ДНК при их объединении, а также имеет прямое отношение к синтезу белка.
На следующей стадии две молекулы ДНК объединяются, располагаясь таким образом, чтобы начало и концы цепей были направлены в противоположные стороны. В этом случае гетероциклы двух цепей обращены навстречу друг другу и оказываются расположенными неким оптимальным образом, имеется в виду, что между парами группировок С=О и NH2 , а также между є N и NH=, входящими в состав гетероциклов, возникают водородные связи (см. ВОДОРОДНАЯ СВЯЗЬ). На рис. 6 показано, как располагаются две цепи относительно друг друга и как при этом возникают водородные связи между гетероциклами. Самая важная деталь – состоит в том, что пары, связанные водородными связями, жестко определены: фрагмент А всегда взаимодействует с Т, а фрагмент Г – всегда с Ц. Строго определенная геометрия этих групп приводит к тому, что эти пары исключительно точно подходят друг другу (как ключ к замку), пара А-Т связана двумя водородными связями, а пара Г-Ц – тремя связями.
Водородные связи заметно слабее обычных валентных связей, но из-за большого их количества вдоль всей полимерной молекулы соединение двух цепей становится достаточно прочным. В молекуле ДНК содержится десятки тысяч групп А, Т, Г и Ц и порядок их чередования в пределах одной полимерной молекулы может быть различным, например, на определенном участке цепи последовательность может иметь вид: —А—А—Т—Г—Ц—Г—А—Т-. Поскольку взаимодействующие группы строго определены, то на противолежащем участке второй полимерной молекулы обязательно будет последовательность –Т—Т—А—Ц—Г—Ц—Т—А-. Таким образом, зная порядок расположения гетероциклов в одной цепи, можно указать их размещение в другой цепи. Из этого соответствия следует, что суммарно в сдвоенной молекуле ДНК количество групп А равно количеству групп Т, а количество групп Г – количеству Ц (правило Э.Чаргаффа).
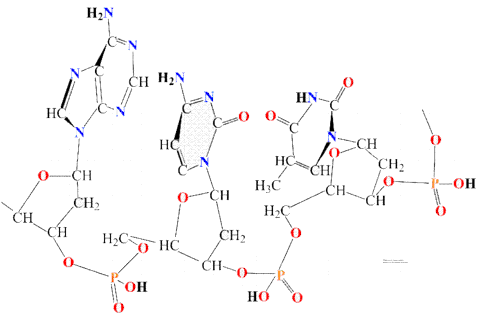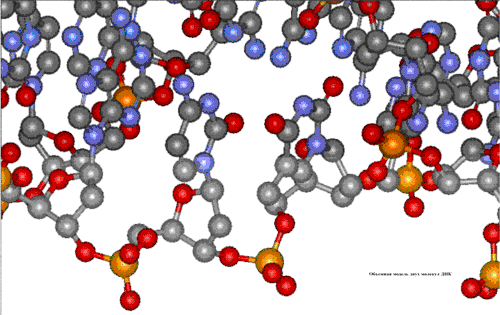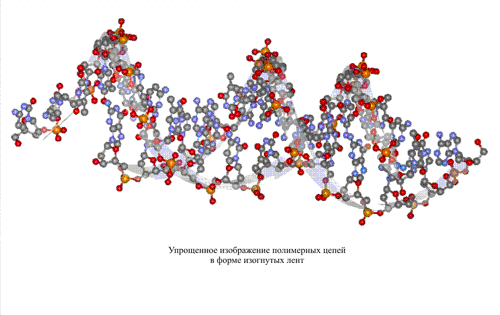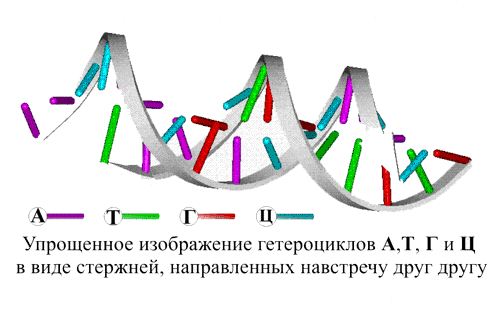
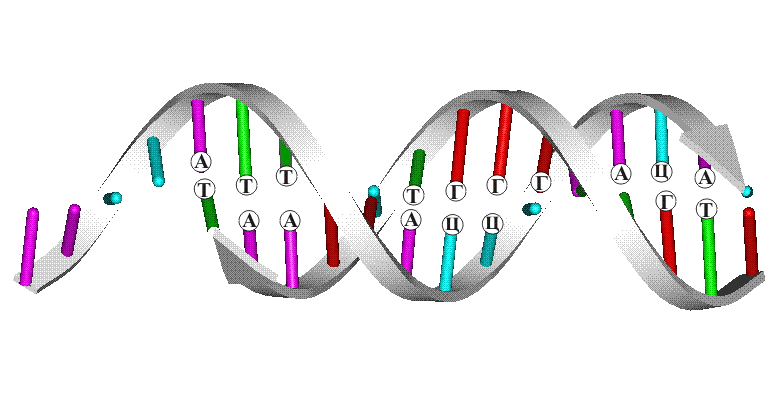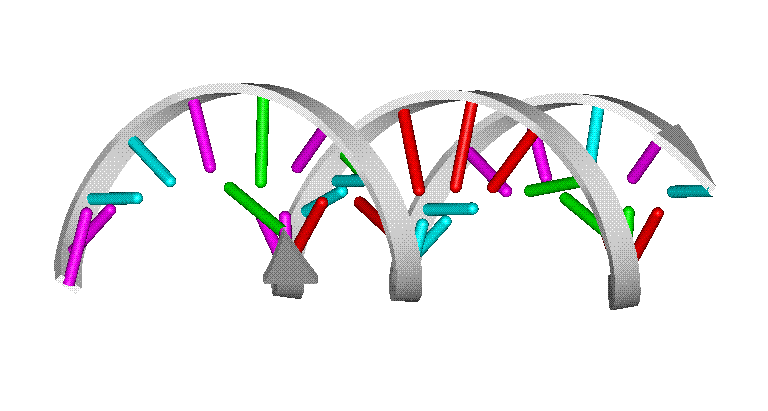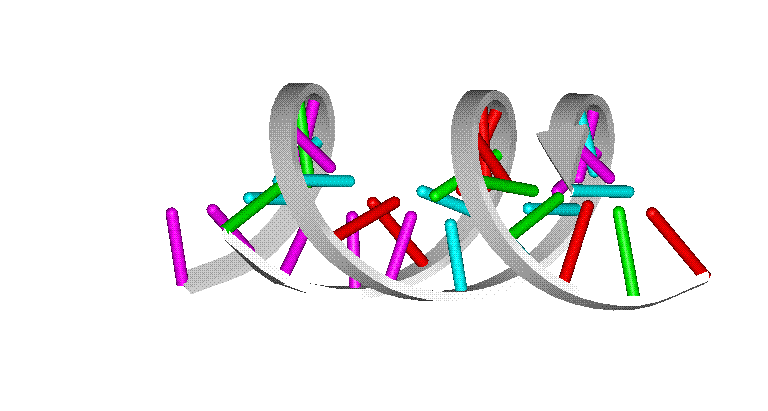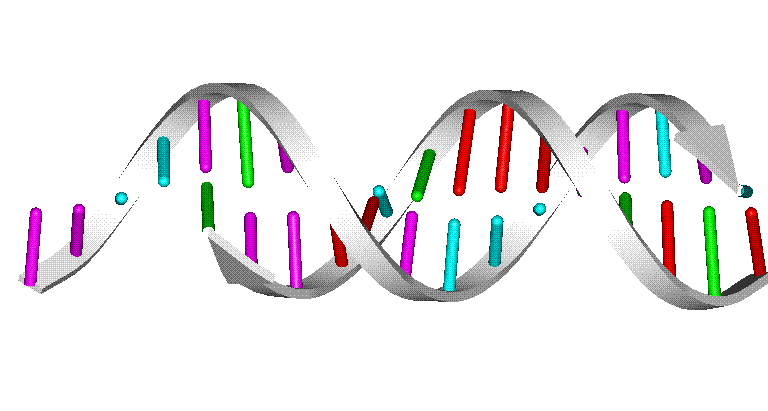
Две молекулы ДНК, связанные водородными связями, показаны на рис. 5 в виде двух плоско лежащих цепей, однако в действительности они располагаются иным образом. Истинное направление в пространстве всех связей, определяемое валентными углами и стягивающими водородными взаимодействиями, приводит к определенном изгибам полимерных цепей и повороту плоскости гетероциклов, что приблизительно показано в первом видеофрагменте рис. 7 с помощью структурной формулы. Гораздо точнее всю пространственную конструкцию можно передать только с помощью объемных моделей (рис. 7, второй видеофрагмент). При этом возникает сложная картина, поэтому принято использовать упрощенные изображения, которые особенно широко применяют при изображении структуры нуклеиновых кислот или белков. В случае нуклеиновых кислот полимерные цепи изображают в форме плоских лент, а гетероциклические группировки А, Т, Г и Ц – в виде боковых стержней или простых валентных штрихов, имеющих различные цвета, либо содержащих на конце буквенные обозначения соответствующих гетероциклов (рис. 7, третий видеофрагмент).
Во время поворота всей конструкции вокруг вертикальной оси (рис. 8) отчетливо видна спиральная форма двух полимерных молекул, которые как бы навиты на поверхность цилиндра, это широко известная двойная спираль ДНК.
При таком упрощенном изображении не исчезает основная информация – порядок чередования группировки А, Т, Г и Ц, определяющий индивидуальность каждого живого организма, вся информация записана четырехбуквенным кодом.
Строение полимерной цепи и обязательное присутствие четырех типов гетероциклов однотипно для всех представителей живого мира. У всех животных и высших растений количество пар А – Т всегда несколько больше, чем пар Г – Ц. Отличие ДНК млекопитающих от ДНК растений в том, что у млекопитающих пара А – Т на всем протяжении цепи встречается ненамного чаще (приблизительно в 1,2 раза), чем пара Г – Ц. В случае растений предпочтительность первой пары гораздо более заметна (приблизительно в 1,6 раза).
ДНК – одна из самых больших известных на сегодня полимерных молекул, у некоторых организмов ее полимерная цепь состоит из сотен миллионов звеньев. Длина такой молекулы достигает нескольких сантиметров, это очень большая величина для молекулярных объектов. Т.к. поперечное сечение молекулы всего 2 нм (1нм = 10 –9 м), то ее пропорции можно сопоставить с железнодорожным рельсом длиной в десятки километров.
Химические свойства ДНК.
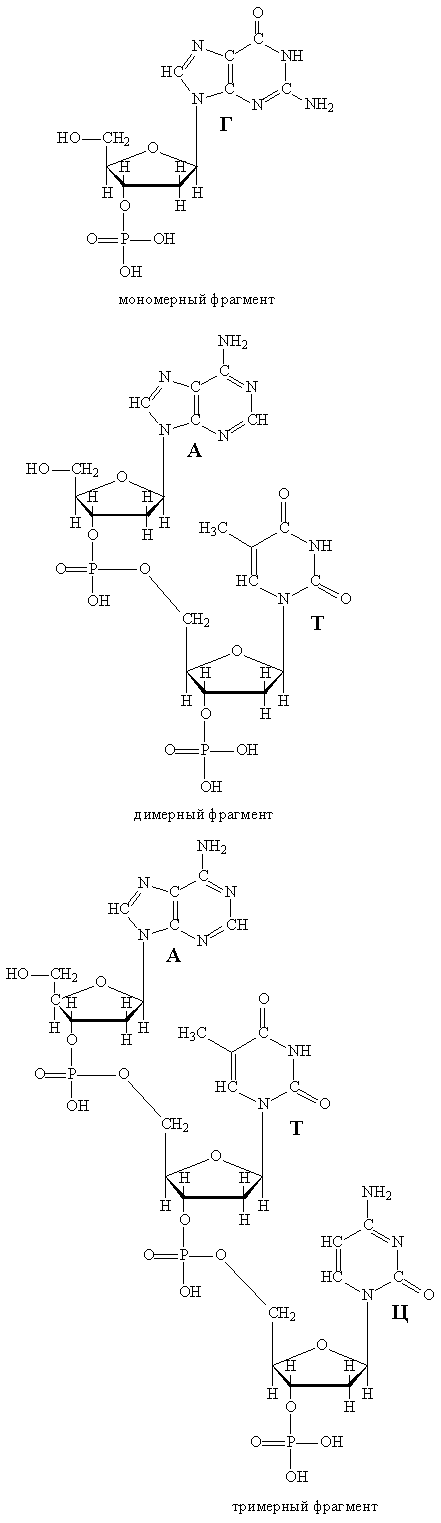
В воде ДНК образует вязкие растворы, при нагревании таких растворов до 60° С или при действии щелочей двойная спираль распадается на две составляющие цепи, которые вновь могут объединиться, если вернуться к исходным условиям. В слабокислых условиях происходит гидролиз, в результате частично расщепляются фрагменты –Р-О-СН2— с образованием фрагментов –Р-ОН и НО-СН2 , соответственно результате образуются мономерные, димерные (сдвоенные) или тримерные (утроенные) кислоты, представляющие собой звенья, из которых была собрана цепь ДНК (рис. 9).
Рис. 9. ФРАГМЕНТЫ, ПОЛУЧАЕМЫЕ ПРИ РАСЩЕПЛЕНИИ ДНК.
Более глубокий гидролиз позволяет отделить участки дезоксирибозы от фосфорной кислоты, а также группировку Г от дезоксирибозы, т.е., более детально разобрать молекулу ДНК на составляющие компоненты. При действии сильных кислот (помимо распада фрагментов –Р(О)-О-СН2-) отщепляются и группировки А и Г. Действие иных реагентов (например, гидразина) позволяет отделить группировки Т и Ц. Более деликатное расщепление ДНК на компоненты проводят с помощью биологического препарата – дезоксирибонуклеазы, выделяемой из поджелудочной железы (окончание —аза всегда указывает на то, что данное вещество представляет собой катализатор биологического происхождения – фермент). Начальная часть названия – дезоксирибонуклеаза – указывает, какое именно соединение расщепляет этот фермент. Все указанные способы расщепления ДНК ориентированы, в первую очередь, на детальный анализ ее состава.
Самая важная информация, содержащаяся в молекуле ДНК, – порядок чередования групп А, Т, Г и Ц , ее получают с помощью специально разработанных методик. Для этого создан широкий набор ферментов, которые находят в молекуле ДНК строго определенную последовательность, например, Ц—T—Г—Ц—A—Г (а также соответствующую ей последовательность на противоположной цепи Г—А—Ц—Г—Т—Ц) и вычленяют ее из состава цепи. Таким свойством обладает фермент Pst I (торговое наименование, оно образуется из названия того микроорганизма Providencia stuartii, из которого получают этот фермент). При использовании другого фермента Pal I удается найти последовательность Г—Г—Ц—Ц. Далее сопоставляются результаты, полученные при действии широкого набора различных ферментов по заранее разработанной схеме, в результате удается определить последовательность таких групп на определенном участке ДНК. Сейчас подобные методики доведены до стадии широкого применения, они используются в самых разнообразных областях, далеких от научных биохимических исследований, например, при идентификации останков живых организмов или установлении степени родства.
Структура РНК
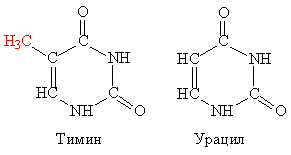
во многом напоминает ДНК, отличие в том, что в основной цепи фрагменты фосфорной кислоты чередуются с рибозой, а не с дезоксирибозой (рис.). Второе отличие – к боковому обрамлению присоединяется гетероцикл урацил (У) вместо тимина (Т), остальные гетероциклы А, Г и Ц те же, что у ДНК. Урацил отличается от тимина отсутствием метильной группы, присоединенной к циклу, на рис. 10 эта метильная группа выделена красным цветом.
Рис. 10. ОТЛИЧИЕ ТИМИНА ОТ УРАЦИЛА – отсутствие у второго соединения метильной группы, выделенной в тимине красным цветом.
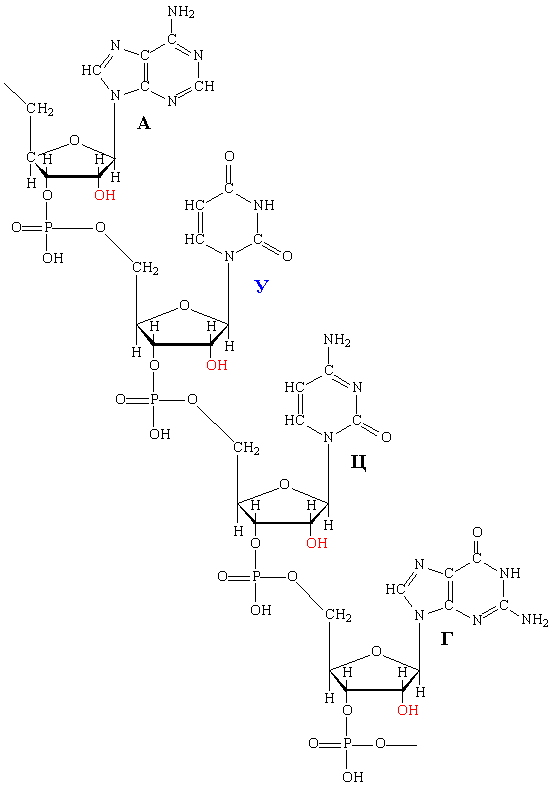
Фрагмент молекулы РНК показан на рис. 11, порядок следования группировок А, У, Г и Ц, а также их количественное соотношение может быть различным.
Рис.11. ФРАГМЕНТ МОЛЕКУЛЫ РНК. Основное отличие от ДНК – наличие группировок ОН в рибозе (красный цвет) и фрагмента урацила (синий цвет).
Полимерная цепь РНК приблизительно в десять раз короче, чем у ДНК. Дополнительное отличие в том, что молекулы РНК не объединяются в двойные спирали, состоящие из двух молекул, а обычно существуют в виде одиночной молекулы, которая на некоторых участках может образовывать сама с собой двухцепные спиральные фрагменты, чередующиеся с линейными участками. На спиральных участках взаимодействие пар соблюдается также строго, как в ДНК. Пары, связанные водородными связями и формирующие спираль (А—У и Г—Ц), возникают на тех участках, где расположение групп оказывается благоприятным для такого взаимодействия (рис. 12).
Для подавляющего большинства живых организмов количественное содержание пар А—У больше чем Г—Ц, у млекопитающих в 1,5–1,6 раза, у растений – в 1,2 раза. Существует несколько типов РНК, роли, которых в живом организме различны.
Химические свойства РНК
напоминают свойства ДНК, однако наличие дополнительных групп ОН в рибозе и меньшее (в сравнении с ДНК) содержание стабилизированных спиральных участков делает молекулы РНК химически более уязвимыми. При действии кислот или щелочей основные фрагменты полимерной цепи Р(О)-О-СН2 легко гидролизуются, группировки А, У, Г и Ц отщепляются легче. Если нужно получить мономерные фрагменты (подобные тем, что на рис. 9), сохранив при этом химически связанные гетероциклы, используют деликатно действующие ферменты, называемые рибонкулеазами.
Участие ДНК и РНК в синтезе белков
– одна из основных функций нуклеиновых кислот. Белки – важнейшие компоненты каждого живого организма. Мышцы, внутренние органы, костная ткань, кожный и волосяной покров млекопитающих состоят из белков. Это полимерные соединения, которые собираются в живом организме из различных аминокислот. В такой сборке управляющую роль играют нуклеиновые кислоты, процесс проходит в две стадии, причем на каждой из них определяющий фактор – взаимоориентация азотсодержащих гетероциклов ДНК и РНК.
Основная задача ДНК – хранить записанную информацию и предоставлять в тот момент, когда начинается синтез белков. В связи с этим понятна повышенная химическая устойчивость ДНК в сравнении с РНК. Природа позаботилась о том, чтобы сохранить по возможности основную информацию неприкосновенной.
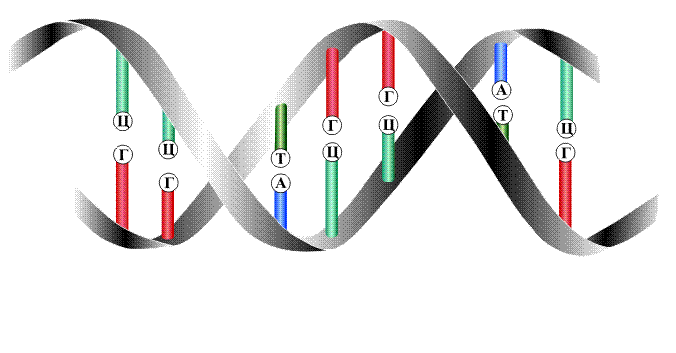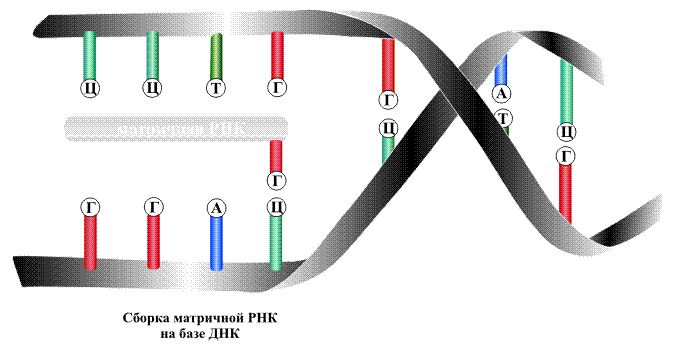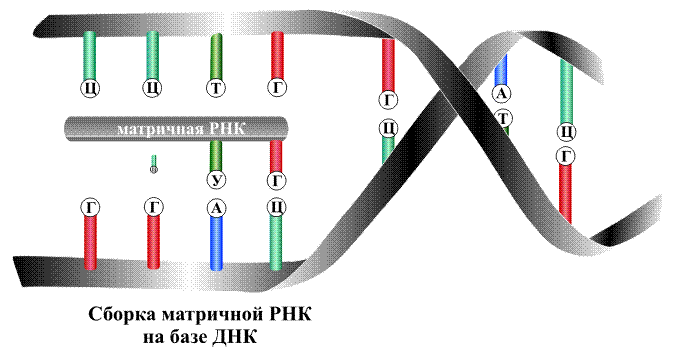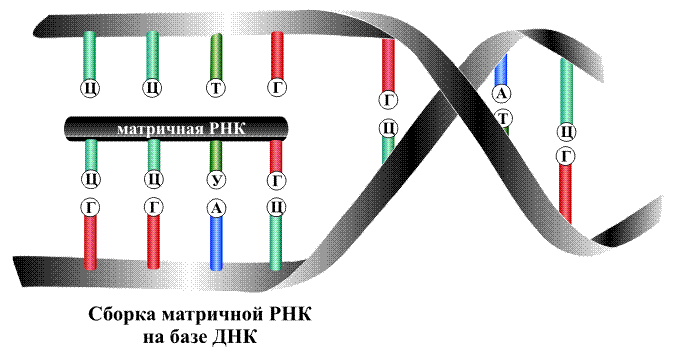
На первой стадии часть двойной спирали раскрывается, освободившиеся ветви расходятся, и на группах А, Т, Г и Ц, оказавшихся доступными, начинается синтез РНК, называемой матричной РНК, поскольку она как копия с матрицы точно воспроизводит информацию, записанную на раскрывшемся участке ДНК. Напротив группы А, принадлежащей молекуле ДНК, располагается фрагмент будущей матричной РНК, содержащий группу У, все остальные группы располагаются друг напротив друга в точном соответствии с тем, как это происходит при образовании двойной спирали ДНК (рис. 13).
По указанной схеме образуются полимерная молекула матричной РНК, содержащая несколько тысяч мономерных звеньев.
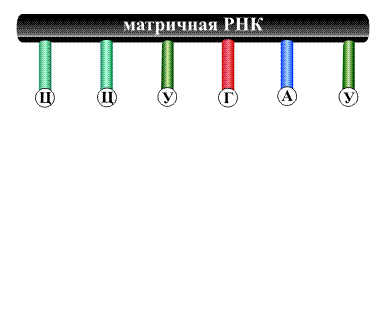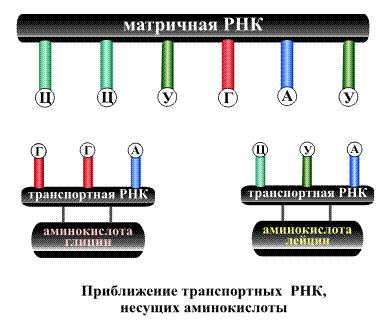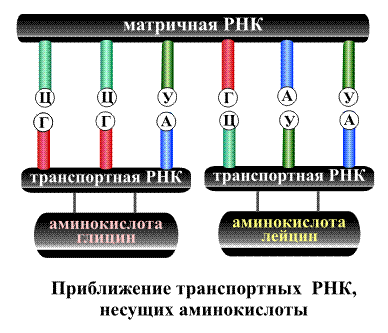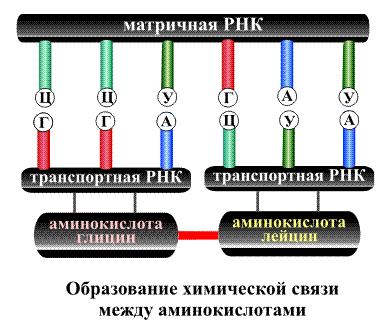
На втором этапе матричная ДНК перемещается из ядра клетки в околоядерное пространство – цитоплазму. К полученной матричной РНК подходят так называемые транспортные РНК, которые несут с собой (транспортируют) различные аминокислоты. Каждая транспортная РНК, нагруженная определенной аминокислотой, приближается к строго обусловленному участку матричной РНК, нужное место обнаруживается с помощью все того же принципа взаимосоответствия групп А—У, и Г—Ц. В конечном итоге две аминокислоты, оказавшиеся рядом, взаимодействуют между собой, так начинается сборка будущей белковой молекулы (рис. 14).
Важная деталь состоит в том, что временное взаимодействие матричной и транспортной РНК проходит всего по трем группам, например, к триаде Ц—Ц—У матричной кислоты может подойти только соответствующая ей тройка Г—Г—А транспортной РНК, которая непременно несет с собой аминокислоту глицин (рис. 14). Точно также к триаде Г—А—У может приблизиться лишь набор Ц—У—А, транспортирующий только аминокислоту лейцин. Таким образом, последовательность групп в матричной РНК указывает, в каком порядке должны соединяться аминокислоты. Кроме того, система содержит в закодированном виде дополнительные регулирующие правила, некоторые последовательности из трех групп матричной РНК указывает на то, что в этом месте синтез белка должен остановиться, т.е. молекула достигла необходимой длины.
Показанный на рис. 14 синтез белка проходит с участием еще одного – третьего вида РНКислот, они входят в состав рибосом и потому их называют рибосомными. Рибосома, представляющая собой ансамбль определенных белков рибосомных РНК, обеспечивает взаимодействие матричной и транспортной РНК, играя роль конвейерной ленты, которая передвигает матричную РНК на один шаг после того, как произошло соединение двух аминокислот.
Основной смысл двухстадийной схемы, показанной на рис. 13 и 14, состоит в том, что полимерная цепь белковой молекулы собирается из различных аминокислот в намеченном порядке и строго по тому плану, который был записан в закодированном виде на определенном участке ДНК. Таким образом, ДНК представляет собой отправную точку всего этого запрограммированного процесса.
В процессе жизнедеятельности белки постоянно расходуются, и потому они регулярно воспроизводятся по описанной схеме, весь синтез белковой молекулы, состоящей из сотен аминокислот, проходит в живом организме приблизительно в течение одной минуты.
Первые исследования нуклеиновых кислот были проведены во второй половине 19 в., понимание того, что в ДНК зашифрована вся информация о живом организме, пришло в середине 20 в., структуру двойной спирали ДНК установили в 1953 Дж.Уотсон и Ф.Крик на основании данных рентгеноструктурного анализа, что признано крупнейшим научным достижением 20 столетия. В середине 70-х годов 20 в. появились методики расшифровки детальной структуры нуклеиновых кислот, а вслед за тем были разработаны способы их направленного синтеза. Сегодня ясны далеко не все процессы, происходящие в живых организмах с участием нуклеиновых кислот, и сегодня это одна из самых интенсивно развивающихся областей науки.
Глава 3. ХИМИЯ НУКЛЕИНОВЫХ КИСЛОТ
В наше время трудно назвать область естествознания, которую не интересовала бы проблема структуры и функций нуклеиновых кислот. Несмотря на огромный прогресс, достигнутый в последние десятилетия при изучении химического состава и строения нуклеиновых кислот, много проблем предстоит еще решить для выяснения зависимости между структурой и биологической ролью нуклеиновых кислот. Нет сомнения, что именно на этом пути научного поиска исследования нуклеиновых кислот будут сделаны открытия, имеющие огромное значение для биологии, медицины и всей науки о живом. Эпохальное открытие принципа комп-лементарности нуклеиновых кислот позволило проникнуть в тайны не только тонкой структуры этих биополимеров, но и механизмов синтеза и воспроизведения биологических макромолекул. Нуклеиновые кислоты выполняют ряд важных биологических функций, не свойственных другим полимерным веществам. В частности, они обеспечивают хранение и передачу наследственной информации и принимают непосредственное участие в механизмах реализации этой информации путем программирования синтеза всех клеточных белков. Структурные компоненты нуклеиновых кислот выполняют, кроме того, функции кофакторов (коэнзим А, уридин-дифосфатглюкоза и др.), аллостерических эффекторов, входят в состав коферментов (никотинамидадениндинуклеотид, флавинадениндинуклеотид и др.), принимая тем самым непосредственное участие в обмене веществ, а также в аккумулировании (накоплении), переносе и трасформации энергии. Они являются предшественниками вторичных посредников (мессенд-жеров) – циклических мононуклеотидов (цАМФ и цГМФ), выполняющих важную функцию в передаче внутриклеточных сигналов. Подробно основные функции нуклеиновых кислот рассмотрены в главе 14.
Методы выделения нуклеиновых кислот. При изучении химического состава и строения нуклеиновых кислот перед исследователем всегда стоит задача выделения их из биологических объектов. В главе 2 было указано, что нуклеиновые кислоты являются составной частью сложных белков – нуклеопротеинов, содержащихся во всех клетках животных, бактерий, вирусов, растений. Нуклеиновые кислоты обладают сильно выраженными кислыми свойствами (обусловлены остатками ортофосфорной кислоты в их составе) и при физиологических значениях рН несут отрицательный заряд. Этим объясняется одно из важных свойств нуклеиновых кислот – способность к взаимодействию по типу ионной связи с основными белками (гистонами), ионами металлов (преимущественно с Mg 2+ ), а также с полиаминами (спермин, спермидин) и путресцином. Поэтому для выделения нуклеиновых кислот из комплексов с белками необходимо прежде всего разрушить эти сильные и многочисленные электростатические связи между положительно заряженными молекулами белков и отрицательно заряженными молекулами нуклеиновых кислот. Для этого измельченный путем гомогенизации биоматериал обрабатывают крепкими солевыми растворами (10% раствор хлорида натрия) с последующим осаждением нуклеиновых кислот этанолом. В настоящее время для выделения нуклеиновых кислот в нативном состоянии пользуются более «мягким» фенольным методом, основанным на обработке нейтрального забуференного раствора нуклеопротеинов фенолом. Обычно эту процедуру проводят в присутствии веществ, вызывающих денатурацию белкового компонента, например до-децилсульфата (ДСН) или салицилата натрия, затем смесь подвергают центрифугированию. При этом денатурированный белок попадает в фе-нольную фазу, а нуклеиновые кислоты остаются в водной среде, из которой их осаждают на холоде добавлением 2–3 объемов этанола. Этим методом удается получить достаточно очищенные препараты нуклеиновых кислот.
В настоящее время применяют ряд усовершенствованных методов разделения нуклеиновых кислот на фракции из суммарного препарата, полученного описанным методом. Это прежде всего хроматография на геле фосфата кальция, ионообменная хроматография (в качестве адсорбентов используют ДЭАЭ-целлюлозу, ДЭАЭ-сефадекс и др.), ультрацентрифугирование в градиенте плотности сахарозы, хроматография по сродству на белковых носителях, фильтрация через гели агарозы и сефарозы, гель-электрофорез и др.
После получения нуклеиновых кислот в чистом виде их подвергают гидролизу для изучения химического состава. Для этих целей используют ферментативные методы (экзо- и эндонуклеазы), а также чисто химические методы гидролиза, в частности нагревание нуклеиновых кислот с хлорной кислотой.
http://www.krugosvet.ru/enc/nauka_i_tehnika/himiya/NUKLEINOVIE_KISLOTI.html
http://xumuk.ru/biologhim/035.html