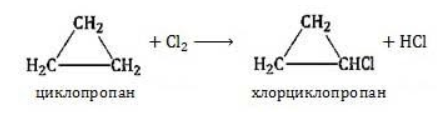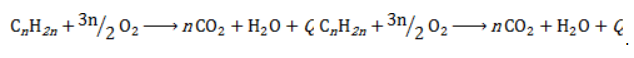Химические свойства циклопропана и его производных
Вы будете перенаправлены на Автор24
Среди циклоалканов циклопропан занимает особое место. С одной стороны его свойства крайне схожи со свойствами линейных алканов: циклопропан устойчив к действию окислителей и прочих реакционно способных веществ.
Но с другой стороны, в связи с увеличением $\pi$-характера $C-C$-связей в циклопропане, в некоторых случаях он может реагировать как алкен. Например, он подвергается гидрогалогенированию с минеральными кислотами с получением линейных алкилгалогенидов. Замещенные циклопропана также реагируют, следуя правилу Марковникова.
Особые свойства циклопропанового кольца
Циклопропановое кольцо настолько стабильно к действию окислителей, что алкилциклопропаны реагируют только по $\alpha$-положению без раскрытия цикла. Наиболее наглядным примером такого рода реакции является озонолиз тетраспироциклопропана, приводящий к моно- и диспирокетонам.
Аналогично окислительный озонолиз транс-1,2-дифенилциклопропана дает транс-циклопропан-1,2-дикарбоновую кислоту:
Готовые работы на аналогичную тему
Циклопропан является наиболее сильной $C-H$ кислотой из всех циклоалканов. Арилциклопропаны отщепляют протон уже при действии раствора трет-бутилата калия в ДМСО.
Свойства циклопропана, характерные и прочим циклоалканам
Гидрирование циклопропана (каталитический гидрогенолиз).
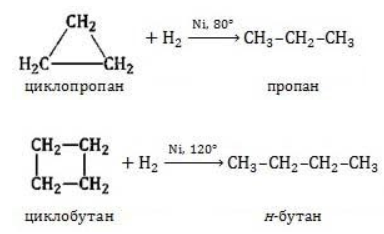
Напряжение цикла циклопропана проявляется во многих его реакциях. В частности он подвергается каталитическому гидрогенолизу с образованием пропана, однако при жестких условиях по сравнению с гидрогенолизом этилена и пропилена.
Реакции присоединения. К реакциям присоединения среди циклоалканов в первую очередь склоннен именно циклопропан (в меньшей мере также и циклобутан, который вступает в них в более жестких условиях):
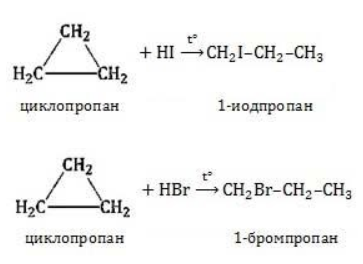
При действии галогеноводородов на производные циклопропана реакция проходит по правилу Марковникова:
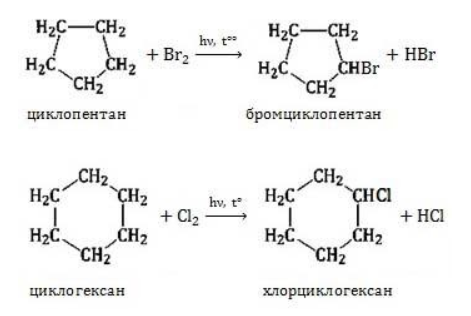
Реакции замещения в циклопропане. Несмотря на то, что реакции замещения более характерны для пяти-, шестичленных и высших циклов, циклопропан и и его производные также вступают в этот тип реакций. Например, при хлорировании на свету они образуют смесь моно- и дихлоропроизводных:
Кроме того, в зависимости от условий при реакции с хлором протекать реакция с раскрытием цикла
При аналогичной реакции с бромом образуется только 1,3-дибромпропан.
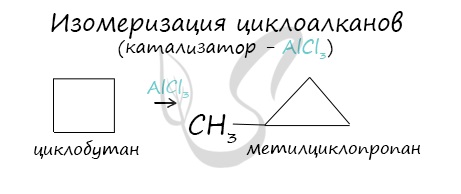
Изомеризация циклопропана. Для циклоалканов характерна изомеризация цикла с его расширением или сужением. Только циклопропан изомеризуется при нагревании в присутствии некоторых металлов с расщеплением до пропилена:
Изомеризация циклопропана происходит также при реакциях замещения, причем цикл сужается или расширяется, как правило, на один атом углерода (М. Кижнер, В. Марковников):
Реакции с солями ртути
Производные циклопропана реагируют с солями ртути. Эти реакции, были открыты Р. Я. Левиной, и напоминают оксимеркурирование алкенов. Направление раскрытия цикла также как и в случае прочих реакций присоединения соответствует правилу Марковникова.
Метиленциклопропан
Метиленциклопропан представляет собой органическое соединение с формулой $(CH_2)_2CCH_2$.
Это бесцветный легко сжижаемый газ, который используется в качестве реагента в органическом синтезе.
Будучи напряженной и ненасыщенной молекула метиленциклопропана претерпевает множество реакций, особенно в присутствии металлических катализаторов. Например, метиленциклопропаны могут быть преобразованы в циклобутеноны в присутствии платинового катализатора. Этот процесс можно рассматривать аналогично расширению цикла самого циклопропана и прочих его производных:
Получи деньги за свои студенческие работы
Курсовые, рефераты или другие работы
Автор этой статьи Дата последнего обновления статьи: 04 04 2021
Химические свойства циклоалканов
Количество углеродных атомов в цикле, образующем молекулу, влияет на свойства циклоалканов, проявляемые в различных видах химических взаимодействий. Соединения с малыми циклами, в которых существенную роль играет угловое напряжение, отличаются неустойчивостью и близки по свойствам к непредельным углеводородам. Чем больше звеньев в цикле, тем сильнее проявляются свойства, присущие алканам.
Реакции присоединения
Участие в процессах этого типа, связанных с разрывом замкнутого участка молекулы, свойственно циклопропану 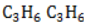
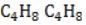
Гидрирование
Условиями реакции являются нагревание и присутствие катализатора. Цикл размыкается с образованием алкана:
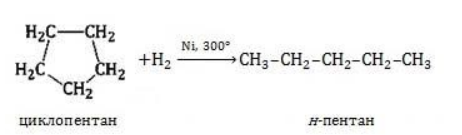
Для вступления в реакцию циклопентана требуются более жесткие условия:
Это единственная реакция присоединения, в которую способен вступать циклопентан. Сходство химических свойств циклоалканов с более высоким углеродным числом обусловливает их неучастие в реакциях присоединения.
Галогенирование
Продуктом этой реакции становится дигалогеналкан:
Гидрогалогенирование
Циклопропан реагирует в водном растворе с галогенводородами:
Присоединять галогенводород способны и гомологи циклопропана с углеводородным радикалом и трехчленным циклом. В процессах гидрогалогенирования циклоалканов соблюдается правило Марковникова, согласно которому водород присоединяется к максимально гидрогенизированному атому углерода:
Реакции замещения
Для циклоалканов со слабо напряженным или ненапряженным циклом (
Галогенирование
В результате реакции образуется галогенциклоалкан:
Хлорирование малого цикла также может происходить без его разрыва, если температура реакции не превысит 100° C:
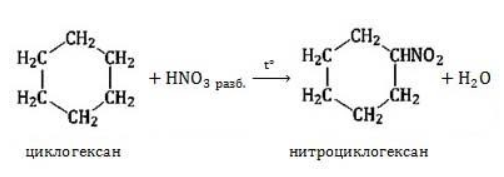
Нитрование
Азотная кислота должна быть разбавленной. Продукт взаимодействия – нитроциклоалкан:
Окисление циклоалканов
Реакции окисления одинаково свойственны всем циклоалканам. Аналогично предельным незамкнутым углеводородам, они не реагируют с водным раствором 
Мягкое окисление
При мягком окислении воздухом на хлориде кобальта получают алициклические кислородсодержащие соединения (кетон и спирт):
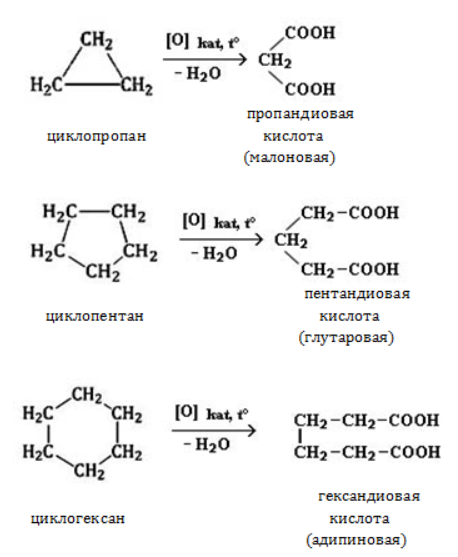
Жесткое окисление
С использованием катализатора воздействие сильного окислителя (например, разбавленной азотной кислоты) на циклоалкан приводит к образованию двухосновных кислот. Реакция протекает в жестких условиях:
Полное окисление (горение)
В общем виде уравнение горения циклоалканов записывается:
Инициирует реакцию контакт с открытым пламенем.
Реакция отщепления
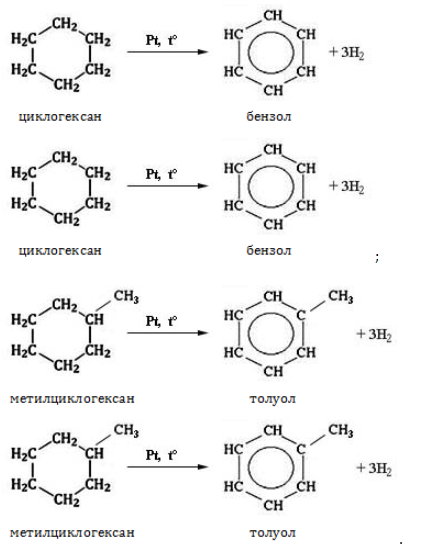
Нагревание в присутствии металлического катализатора приводит к дегидрированию циклоалканов – отщеплению водорода и образованию ароматического соединения бензольного ряда:
Изомеризация
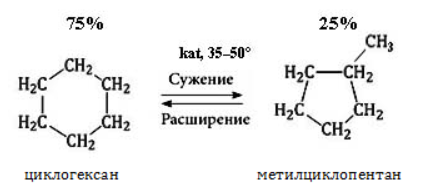
Циклоалканы способны изомеризоваться с перегруппировкой атомов в углеродном скелете. Процесс протекает на платине, хлориде или бромиде алюминия и сопровождается сужением либо расширением цикла. Образование средних циклов происходит легче, и они отличаются большей устойчивостью:
Реакция идет в обоих направлениях до установления равновесия.
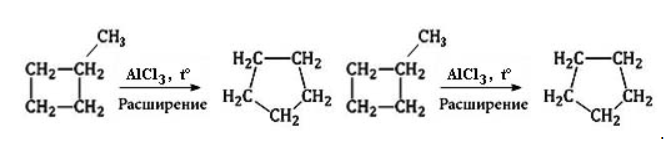
Для низших циклоалканов предпочтительной оказывается изомеризация с расширением цикла, так как она ведет к ослаблению углового напряжения в молекуле. Так, метилциклобутан переходит в циклопентан необратимо:
Заключение
Циклоалканы, находящиеся в начале гомологического ряда, сочетают в своих химических взаимодействиях свойства предельных и непредельных углеводородов линейного строения. Комбинация свойств вызвана, с одной стороны, особыми условиями образования непрочных изогнутых связей в простейших циклах, и, с другой стороны, насыщенностью соединений.
Высшие циклоалканы практически не отличаются по химическим свойствам от алканов, так как их макроциклы не оказывают деформирующего влияния на строение химических связей.
Циклоалканы
Циклоалканы (циклопарафины, нафтены) — циклические насыщенные углеводороды, по химическому строению близкие к алканам. Содержат только простые одинарные сигма связи (σ-связи), не содержат ароматических связей.
Циклоалканы имеют большую плотность и более высокие температуры плавления, кипения, чем соответствующие алканы. Общая формула их гомологического ряда — CnH2n.
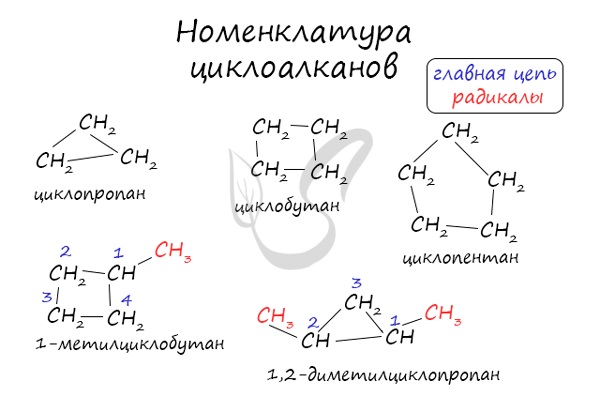
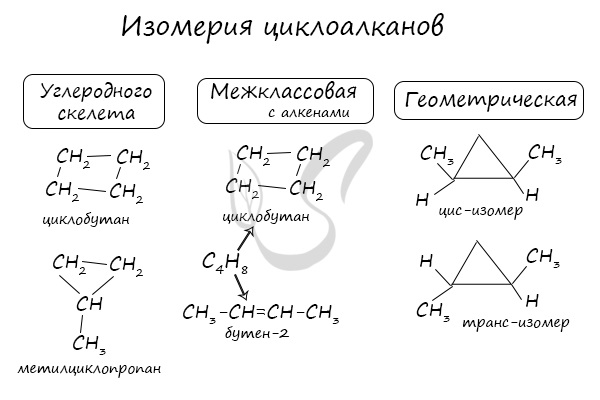
Номенклатура и изомерия циклоалканов
Названия циклоалканов формируются путем добавления приставки «цикло-» к названию алкана с соответствующим числом: циклопропан, циклобутан и т.д.
Как и у алканов, атомы углерода циклоалканов находятся в sp 3 гибридизации.
Помимо изомерии углеродного скелета, для циклоалканов характерна межклассовая изомерия с алкенами и пространственная геометрическая изомерия в виде существования цис- и транс-изомеров.
Получение циклоалканов
В промышленности циклоалканы получают несколькими способами:
- Из ароматических углеводородов
Циклоалканы можно получить гидрированием (присоединением водорода) бензола и его гомологов.
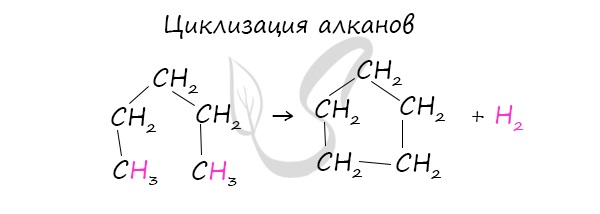
При наличии катализатора и повышенной температуры алканы способны образовывать цикл, отщепляя при этом водород.
В лабораторных условиях циклоалканы можно получить реакцией дегалогенирования дигалогеналканов.
- Дегалогенирование дигалогеналканов (внутримолекулярная реакция Вюрца)
Химические свойства циклоалканов
Важно заметить, что циклопропан и циклобутан вступают в реакции присоединения, проявляя свойства ненасыщенных соединений. Для циклопентана и циклогексана реакции присоединения не характерны, они преимущественно вступают в реакции замещения.
Наиболее легко в реакции гидрирования вступают циклопропан и циклобутан. Циклопентан и циклогексан не вступают в реакции гидрирования (в рамках вопросов ЕГЭ — не вступают, но на самом деле эти реакции идут, просто крайне затруднены).
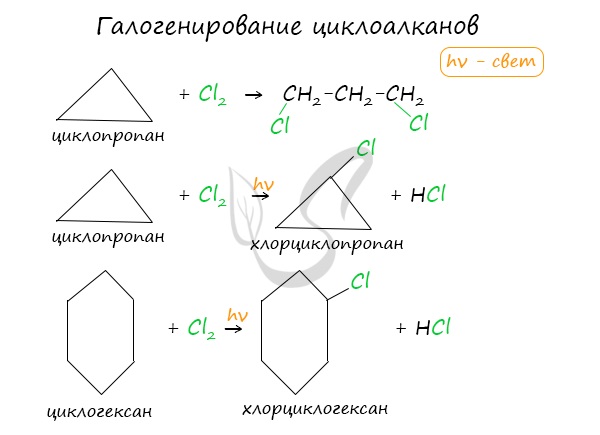
Без освещения реакция циклопропана и циклобутана с хлором идет по типу присоединения. При освещении хлор образует свободные радикалы, реакция идет, как и у алканов, по механизму замещения.
У циклопентана и циклогексана реакция идет только путем замещения.
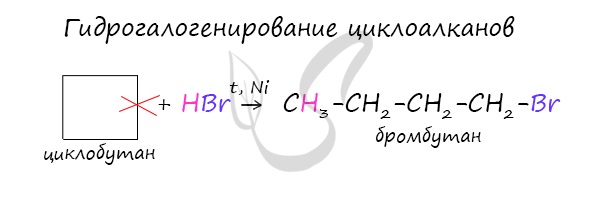
В реакции гидрогалогенирования, протекающие по типу присоединения, вступают циклопропан и циклобутан.
При отщеплении водорода от циклогексана образуется бензол, при наличии радикалов — гомологи бензола.
В ходе нагревания с катализатором — AlCl3 циклоалканы образуют изомеры.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
http://allinchemistry.ru/organicheskaya-himiya/himicheskie-svojstva-tsikloalkanov
http://studarium.ru/article/182