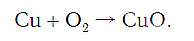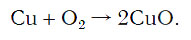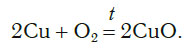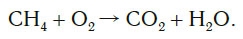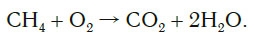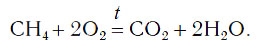Урок 12. Составление уравнений химических реакций
В уроке 12 «Составление уравнений химических реакций» из курса «Химия для чайников» мы научимся составлять уравнения химических реакций и правильно расставлять в них коэффициенты.
Составлять химические уравнения и производить расчеты по ним нужно, опираясь на закон сохранения массы веществ при химических реакциях. Рассмотрим, как можно составить химическое уравнение, на примере реакции меди с кислородом.
Слева запишем названия исходных веществ, справа — продуктов реакции. Если веществ два и более, соединяем их знаком «+». Между левой и правой частями пока поставим стрелку:
медь + кислород → соединение меди с кислородом.
Подобное выражение называют схемой химической реакции. Запишем эту схему при помощи химических формул:
Число атомов кислорода в левой части схемы равно двум, а в правой — одному. Так как при химических реакциях атомы не исчезают, а происходит только их перегруппировка, то число атомов каждого элемента до реакции и после реакции должно быть одинаковым. Чтобы уравнять число атомов кислорода в левой и правой частях схемы, перед формулой CuO ставим коэффициент 2:
Теперь число атомов меди после реакции (в правой части схемы) равно двум, а до реакции (в левой части схемы) — только одному, поэтому перед формулой меди Cu так же поставим коэффициент 2. В результате произведенных действий число атомов каждого вида в левой и правой частях схемы одинаково, что дает нам основание заменить стрелку на знак «=» (равно). Схема превратилась в уравнение химической реакции:
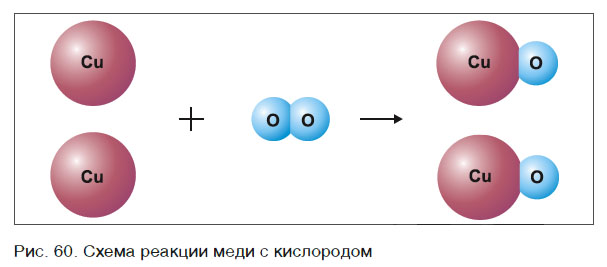
Это уравнение читается так: два купрум плюс о-два равно два купрум-о (рис. 60).
Рассмотрим еще один пример химической реакции между веществами СН4 (метан) и кислородом. Составим схему реакции, в которой слева запишем формулы метана и кислорода, а справа — формулы продуктов реакции — воды и соединения углерода с кислородом (углекислый газ):
Обратите внимание, что в левой части схемы число атомов углерода равно их числу в правой части. Поэтому уравнивать нужно числа атомов водорода и кислорода. Чтобы уравнять число атомов водорода, поставим перед формулой воды коэффициент 2:
Теперь число атомов водорода справа стало 2×2=4 и слева — также четыре. Далее посчитаем число атомов кислорода в правой части схемы: два атома кислорода в молекуле углекислого газа (1×2=2) и два атома кислорода в двух молекулах воды (2×1=2), суммарно 2+2=4. В левой части схемы кислорода только два атома в молекуле кислорода. Для того чтобы уравнять число атомов кислорода, поставим коэффициент 2 перед формулой кислорода:
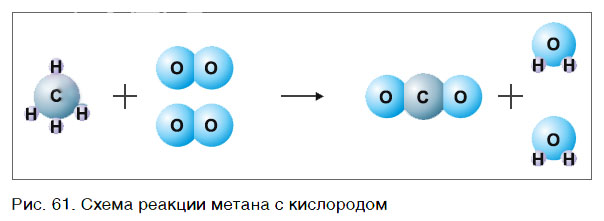
В результате проведенных действий число атомов всех химических элементов до реакции равно их числу после реакции. Уравнение составлено. Читается оно так: це-аш-четыре плюс два о-два равно це-о-два плюс два аш-два-о (рис. 61).
Данный способ расстановки коэффициентов называют методом подбора.
В химии существуют и другие методы уравнивания чисел атомов элементов в левой и правой частях уравнений реакций, с которыми мы познакомимся позднее.
Краткие выводы урока:
Для составления уравнений химических реакций необходимо соблюдать следующий порядок действий.
- Установить состав исходных веществ и продуктов реакции.
- Записать формулы исходных веществ слева, продуктов реакции — справа.
- Между левой и правой частями уравнения сначала поставить стрелку.
- Расставить коэффициенты, т. е. уравнять числа атомов каждого химического элемента до и после реакции.
- Связать левую и правую части уравнения знаком «=» (равно).
Надеюсь урок 12 «Составление уравнений химических реакций» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Если вопросов нет, то переходите к следующему уроку.
Химические уравнения исходные вещества и продукты реакции
Ключевые слова конспекта: задачи на количества исходных веществ, задачи на количества продуктов реакции,
По химическим уравнениям можно рассчитать количество вещества, массу и объем реагирующих веществ и продуктов реакции. Для этого прежде всего необходимо составить уравнение химической реакции и верно расставить коэффициенты.
Расчеты по химическим уравнениям удобнее всего вести с использованием количеств веществ реагирующих и образующихся веществ. Количества вещества соединений, вступающих в химическую реакцию и образующихся в ее результате, пропорциональны друг другу и относятся друг к другу как коэффициенты перед формулами этих веществ в количественном уравнении. Например, реакции, которая описывается уравнением 2Fe + 3Сl2 = 2FeCl3, соответствует следующее соотношение между количествами веществ железа, хлора и хлорида железа (III):
v(Fe) : v(Cl2): v(FeCl3) = 2 : 3 : 2.
Таким образом, зная количество вещества одного из реагирующих веществ или продуктов реакции, можно найти количества вещества других участников данной реакции, а по количеству вещества нетрудно рассчитать их массу или объем.
Следует отметить, что объемы вступивших в реакцию газообразных веществ и объемы газообразных продуктов реакции, измеренные при одинаковых условиях, также относятся друг к другу, как коэффициенты перед соответствующими формулами в уравнении химической реакции. Например, в реакции, уравнение которой 3Н2 + N2 = 2NH3, объемы реагирующих азота и водорода и объем образовавшегося аммиака связаны следующим соотношением:
V(Н2): F(N2): F(NH3) = 3:2:1.
Однако эти соотношения выполняются только между веществами, участвующими в одной и той же химической реакции. Если реагент участвует в двух параллельных реакциях, то его количества веществ в этих реакциях никак не связаны друг с другом и могут находиться в любых соотношениях.
Цитаты из пособия «Задачи по химии 8-9 кл.» (авт. О.С. Габриелян и др.) использованы в учебных целях. Ссылка на покупку книги указана в конце конспекта.
ПРИМЕРЫ РЕШЕНИЯ ЗАДАЧ
Задача № 1. Какой объем кислорода (н. у.) потребуется для сжигания 22,4 г серы?
Ответ. V(O2) = 15,68 л.
Задача № 2. Какую массу оксида фосфора (V) требуется растворить в воде для получения 117,6 г фосфорной кислоты?
Ответ. m(Р2O5) = 85,2 г.
Задача № 3. Вычислите массу осадка, образующегося при добавлении 100 мл 10%-ного раствора хлорида меди (II) (р = 1,08 г/мл) к избытку раствора гидроксида калия.
Ответ. m(Cu(OH)2) = 7,84 г.
Задача № 4. Какой объем соляной кислоты с массовой долей НС1 20% (р = 1,1 г/мл) потребуется для растворения 42,5 г оксида алюминия, содержащего 4% примесей?
Ответ. Vp-pa(HCl) = 398,2 мл.
Задача № 5. Какой объем хлора (н. у.) прореагирует с 112 г смеси железа и меди, массовая доля железа в которой 65% ?
Ответ. V(C12) = 57,34 л.
Задача № 6. 80 г смеси оксидов железа (II) и (III) восстановили водородом. Вычислите массу образовавшегося металла, если массовая доля оксида железа (III) в исходной смеси равна 70%.
О т в е т. m(Fe) = 57,68 г.
Задача № 7. Газ, образовавшийся при сгорании 18,6 г угля в избытке кислорода, пропустили через избыток раствора гидроксида кальция. Какова масса образовавшегося при этом осадка?
Ответ. m(CaCO3) = 155 г.
Задача № 8. Смесь оксида и сульфида цинка массой 114,9 г обработали избытком соляной кислоты. При этом выделилось 13,44 л (н. у.) газа. Определите массовую долю оксида цинка в смеси (в %).
Ответ. ω(ZnO) = 49,3%.
Задача № 9. На растворение смеси оксида и карбоната магния было затрачено 520,65 мл 15%-ного раствора хлороводорода (р = 1,075 г/мл). При этом выделилось 8,96 л (н. у.) газа. Какова масса исходной смеси?
Ответ. m(смеси) = 63,6 г.
Задача № 10. При взаимодействии 200 г раствора, содержащего карбонаты натрия и аммония, с избытком раствора гидроксида калия выделяется 6,72 л газа (н. у.), а при взаимодействии такой же массы раствора солей с избытком соляной кислоты — 8,96 л газа (н. у.). Вычислите массовые доли каждой из солей в растворе.
Ответ. ω((NH4)2CO3) = 7,2%, ω(Na2CO3) = 13,25%.
Задачи на количества исходных веществ и продуктов реакции (ответы и решения). Выберите дальнейшие действия:
Химические уравнения исходные вещества и продукты реакции
ХИМИЯ – это область чудес, в ней скрыто счастье человечества,
величайшие завоевания разума будут сделаны
именно в этой области.(М. ГОРЬКИЙ)
Таблица
Менделеева
Универсальная таблица растворимости
Коллекция таблиц к урокам по химии
Составление уравнений химических реакций
Урок посвящен изучению алгоритма составления уравнения химической реакции. В ходе урока вы научитесь составлять схему и уравнение химической реакции, зная формулы исходных веществ и продуктов реакции.
I. Схема химической реакции
Сущность химической реакции с позиции атомно-молекулярной теории заключается в том, что продукты реакции образуются из тех же атомов, которые входили в состав исходных веществ.
Пример 1. При разложении воды образуются простые вещества – водород и кислород (Рис.1.).
Рис. 1. Разложение воды под действие электрического тока
Запишем формулу исходного вещества воды слева, а формулы продуктов реакции — водорода и кислорода – справа. Между ними поставим стрелку:
Эта запись является схемой реакции.
Схема реакции показывает только состав исходных веществ и продуктов реакции, но не может полностью отражать сущность реакции. В состав молекулы воды входит один атом кислорода, а в состав простого вещества кислорода входят два атома. Это значит, что не выполняется закон сохранения массы веществ.
II. Химические уравнения реакций
Химическое уравнение – это условная запись химической реакции посредством химических формул и коэффициентов.
В результате химического взаимодействия серы и железа получено вещество – сульфид железа (II) – оно отличается от исходной смеси. Ни железо, ни сера не могут быть визуально обнаружены в нем. Невозможно их разделить и с помощью магнита. Произошло химическое превращение.
Запишем протекающую реакцию в виде уравнения химической реакции:
Рассмотрим еще один пример: 2Н2О = 2Н2 + О2
Чтобы не было противоречий с законом сохранения массы веществ, нужно уравнять число атомов каждого химического элемента слева и справа от стрелки.
Чтобы образовалась одна молекула кислорода, в реакцию должны вступить две молекулы воды. Поставив коэффициент «2» перед формулой воды. Теперь уравняем количество атомов водорода, поставив коэффициент «2» перед формулой Н2, вместо стрелки поставим знак равенства:
Эта запись является уравнением химической реакции. В отличие от схемы реакции, уравнение учитывает, что число атомов каждого химического элемента в реакции не меняется.
Цифры, стоящие перед формулой вещества, называются коэффициентами. Коэффициент показывает количество молекул вещества.
Прочитать записанное уравнение можно так: «Из двух молекул воды образуется две молекулы водорода и 1 молекула кислорода».
Составим уравнение химической реакции взаимодействия фосфора и кислорода
1. В левой части уравнения записываем химические формулы реагентов (веществ, вступающих в реакцию). Помните! Молекулы большинства простых газообразных веществ двухатомны – H2; N2; O2; F2; Cl2; Br2; I2. Между реагентами ставим знак «+», а затем стрелку:
2. В правой части (после стрелки) пишем химическую формулу продукта (вещества, образующегося при взаимодействии). Помните! Химические формулы необходимо составлять, используя валентности атомов химических элементов:
3. Согласно закону сохранения массы веществ число атомов до и после реакции должно быть одинаковым. Это достигается путём расстановки коэффициентов перед химическими формулами реагентов и продуктов химической реакции.
- Вначале уравнивают число атомов, которых в реагирующих веществах (продуктах) содержится больше.
- В данном случае это атомы кислорода.
- Находим наименьшее общее кратное чисел атомов кислорода в левой и правой частях уравнения. Наименьшее кратное для атомов натрия –10:
http://uchitel.pro/%D0%B7%D0%B0%D0%B4%D0%B0%D1%87%D0%B8-%D0%BD%D0%B0-%D0%BA%D0%BE%D0%BB%D0%B8%D1%87%D0%B5%D1%81%D1%82%D0%B2%D0%B0-%D0%B8%D1%81%D1%85%D0%BE%D0%B4%D0%BD%D1%8B%D1%85-%D0%B2%D0%B5%D1%89%D0%B5%D1%81%D1%82/
http://kardaeva.ru/88-dlya-uchenika/8-klass/124-sostavlenie-uravnenij-khimicheskikh-reaktsij