Урок 14. Расчеты по уравнениям химических реакций
В уроке 14 «Расчеты по уравнениям химических реакций» из курса «Химия для чайников» мы научимся решать задачи, используя уравнения химических реакций.
Вещества вступают в химические реакции в определенных массовых и количественных соотношениях. Следовательно, при проведении реакций в лабораториях и на химических заводах расходуются определенные массы исходных веществ для получения заданной массы продуктов реакции.
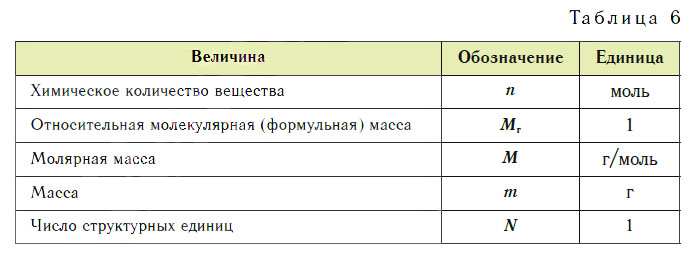
Эти расчеты проводят по уравнениям реакций. Единицы величин, которыми пользуются в химии, представлены в таблице 6.
При проведении любого вычисления по уравнению реакции нужно внимательно прочитать условие задачи. Особое в нимание обратите на расстановку коэффициентов, так как соотношение числа структурных единиц реагирующих веществ и получающихся продуктов реакции выражается в уравнениях коэффициентами так же, как и мольные отношения.
Для решения расчетной задачи необходим определенный порядок действий. Рассмотрим его на нескольких примерах.
Пример 1. Железо масс о й 224 г полностью прореагировало с хлором. Рассчитайте массу образовавшегося вещества FeCl3.
Расчеты по химическим уравнением
Разделы: Химия
Чему бы ты ни учился, ты
учишься для себя.
Петроний
Цели урока:
- познакомить учащихся с основными способами решения задач по химическим уравнениям:
- находить количество, массу и объём продуктов реакции по количеству, массе или объёму исходных веществ,
- продолжить формирование навыков работы с текстом задачи, умение аргументировано выбирать способ решения учебной задачи, умения составлять уравнения химических реакций.
- развивать умения анализировать, сравнивать, выделять главное, составлять план действия, делать выводы.
- воспитывать терпимость к другим, самостоятельность в принятии решений, умение объективно оценить результаты своего труда.
Формы работы: фронтальная, индивидуальная, парная, групповая.
Тип урока: комбинированный с применением ИКТ
Ход и содержание урока
I Организационный момент.
Здравствуйте ребята. Сегодня, мы с вами научимся решать задачи по уравнениям химических реакций. Слайд 1 (cм. презентацию).
Цели урока Слайд 2.
II.Актуализация знаний, умений, навыков.
Химия очень интересная и в то же время сложная наука. Для того чтобы знать и понимать химию, надо не только усваивать материал, но и уметь применять полученные знания. Вы узнали какие признаки указывают на протекание химических реакций, научились составлять уравнения химических реакций. Я надеюсь, что вы хорошо усвоили эти темы и без труда ответите на мои вопросы
Какое явление не является признаком химических превращений:
а) появление осадка; в) изменение объема;
а) уравнения реакций соединения
б) уравнения реакций замещения
в) уравнения реакций разложения Слайд 4
- Новая тема.
Для того, чтобы научиться решать задачи, необходимо составить алгоритм действий, т.е. определить последовательность действий.
Алгоритм для расчета по химическим уравнениям (у каждого учащегося на столе)
Для того, чтобы решить расчетную задачу по химии, можно воспользоваться следующим алгоритмом – сделать пять шагов:
1. Составить уравнение химической реакции.
2. Над формулами веществ записать известные и неизвестные величины с соответствующими единицами измерения (только для чистых веществ, без примесей). Если по условию задачи в реакцию вступают вещества, содержащие примеси, то сначала нужно определить содержание чистого вещества.
3. Под формулами веществ с известными и неизвестными записать соответствующие значения этих величин, найденные по уравнению реакций.
4. Составить и решить пропорцию.
5. Записать ответ.
Приступаем к решению задач, применяя алгоритм
Вычисление массы вещества по известной массе другого вещества, участвующего в реакции
Вычислите массу кислорода, выделившегося в результате разложения
порции воды массой 9 г.
Найдем молярную массу воды и кислорода:
Запишем уравнение химической реакции:
Над формулой в уравнении реакции запишем найденное
значение количества вещества, а под формулами веществ —
стехиометрические соотношения, отображаемые
Вычислим количество вещества, массу которого требуется найти.
Для этого составляем пропорцию
откуда х = 0,25 моль Слайд 7
Следовательно, n(O2)=0,25 моль
Найдем массу вещества, которую требуется вычислить
m(O2) = 0,25 моль • 32 г/моль = 8 г
Ответ: m(О2) = 8 г Слайд 8
Вычисление объема вещества по известной массе другого вещества, участвующего в реакции
Вычислите объем кислорода (н. у.), выделившегося в результате разложения порции воды массой 9 г.
Vm=22,4л/моль Слайд 9
Запишем уравнение реакции. Расставим коэффициенты
Над формулой в уравнении реакции запишем найденное значение количества вещества, а под формулами веществ — стехиометрические соотношения, отображаемые химическим уравнением
Вычислим количество вещества, массу которого требуется найти. Для этого составим пропорцию
откуда х = 0,25 моль
Найдем объем вещества, который требуется вычислить
Ответ: 5,6 л Слайд 11
III.Закрепление изученного материала.
Задачи для самостоятельного решения:
1.При восстановлении углем оксидов Fe2O3 и SnO2 получили по 20 г Fe и Sn. Сколько граммов каждого оксида было взято?
2.В каком случае образуется больше воды:
а) при восстановлении водородом 10 г оксида меди (I) (Cu2O) или
б) при восстановлении водородом 10 г оксида меди(II) (CuO)? Слайд 12
Проверим решение задачи 1
M(Fe)=56г/моль,
m(Fe2O3)=
Проверим решение задачи 2
4.
х моль = 0,07моль,
m (H2O) = 
n(CuO) = 10г/ 80г/моль = 0,125 моль
х моль = 0,125моль, n(H2O)=0,125 моль
Ответ: 2,25г Слайд 15
Домашнее задание: изучить материал учебника с. 45-47, решить задачу
Какую массу оксида кальция и какой объм углекислого газа (н.у.)
можно получить при разложении карбоната кальция массой 250г?
CaCO3 = CaO + CO Cлайд 16.
1. Габриелян О.С. Программа курса химии для 8-11 классов общеобразовательных учреждений. М. Дрофа 2006г.
2. Габриелян О.С. Химия. 8 класс. Учебник для общеобразовательных учреждений. Дрофа. М. 2005г.
3. Горбунцова С.В. Тесты по основным разделам школьного курса хииии. 8 — 9 классы.ВАКО, Москва,2006г.
4. Горковенко М.Ю.Поурочные разработки по химии. К учебникам О.С.Габриеляна, Л.С.Гузея, В.В.Сорокина, Р.П.Суровцевой и Г.Е.Рудзитиса, Ф.Г.Фельдмана. 8 класс.ВАКО, Москва, 2004г.
5. Габриелян О.С. Химия. 8 класс: Контрольные и проверочные работы. – М.: Дрофа, 2003.
6.Радецкий А.М., Горшкова В.П. Дидактический материал по химии для 8-9 классов: Пособие для учителя. – М.: Просвещение, 2000
Расчеты по химическим уравнениям
Для того, чтобы решить расчетную задачу по химии, можно воспользоваться следующим алгоритмом – сделать пять шагов:
1. Составить уравнение химической реакции.
2. Над формулами веществ записать известные и неизвестные величины с соответствующими единицами измерения (только для чистых веществ, без примесей). Если по условию задачи в реакцию вступают вещества, содержащие примеси, то сначала нужно определить содержание чистого вещества.
3. Под формулами веществ с известными и неизвестными записать соответствующие значения этих величин, найденные по уравнению реакций.
4. Составить и решить пропорцию.
5. Записать ответ.
Соотношение некоторых физико-химических величин и их единиц
Масса (m) : г ; кг ; мг
Кол-во в-ва (n) : моль ; кмоль ; ммоль
Молярная масса (M): г/моль ; кг/кмоль ; мг/ммоль
Объём (V) : л ; м 3 /кмоль; мл
Молярный объём(Vm) : л/моль ; м 3 /кмоль; мл/ммоль
Число частиц (N): 6•1023 (число Авагадро – NA); 6•1026 ; 6•1020
Урок по химии для 8 класса «Расчеты по химическим уравнениям»
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Развернутый план-конспект урока «Расчеты по химическим уравнениям».
Учебник: О.С. Габриелян.
Тема урока: Расчеты по химическим уравнениям.
Тип урока: комбинированный.
Образовательные задачи: познакомить с расчетами по химическим уравнениям; сформировать у учащихся знание о расчетах по химическим уравнениям; начать формировать умения по составлению химических уравнений и расчетам по уравнениям.
Воспитательные задачи: продолжить формирование естественнонаучного мировоззрения, представления о единичном и целом.
Развивающие задачи: продолжить формирования умения наблюдать, анализировать, объяснять, делать выводы.
Методы обучения: словесные (объяснение и рассказ учителя ), словесно – наглядные( объяснение с использованием записей на классной доске).
Оборудование: классная доска, таблица Д. И. Менделеева.
1.Организационный момент (2-5мин.)
Здравствуйте ребята присаживайтесь. Сегодня на уроке мы с вами должны будем научиться проводить расчеты по химическим уравнениям.
2. Контроль знаний и умений (10 – 15 мин.)
На предыдущих занятиях мы с вами проходили уравнения химических реакций, давайте вспомним, что такое химическое уравнение? (Химическим уравнением называют условную запись химической реакции с помощью химических формул и математических знаков).
На основе какого закона пишут химические реакции? (Закон сохранения массы веществ).
Как он звучит? (Масса веществ, вступивших в химическую реакцию, равна массе веществ, получившихся в результате ее).
3. Объяснение нового материала (20 – 30 мин.)
По химическому уравнению можно определить, какие вещества вступили в реакцию, и какие образовались, а также по химическому уравнению можно рассчитать массу, объем и количество реагирующих веществ.
Для расчетов очень важно выбрать соответствующие друг другу единицы измерения массы, объема и количества вещества. Давайте откроем учебники на странице 146 и найдем таблицу №7. Рассмотрим по этой таблице соотношение некоторых единиц физико – химических величин.
Для того чтобы решать расчетные задачи по химии, можно пользоваться алгоритмом. Алгоритм решения задач дан в учебнике на странице 147.
Пользуясь алгоритмом решения задач, давайте решим следующие задачу:
Задача: Рассчитайте объем водорода (н.у.), который потребуется для взаимодействия с 230 кг оксида железа (ІІІ). Вычислите количество вещества воды, которое при этом образуется.
m ( Fe 2 O 3)=230кг 1. Запишем уравнение химической реакции:
n ( H 2 O ) — ? 2. Запишем известные и неизвестные числовые значения над формулами веществ в уравнении.
Так как масса дана в килограммах, то объем находим в кубических метрах, а количество вещества – в киломолях. И тогда:
230кг х м 3 y кмоль
где х – объем водорода V ( H 2), y – количество вещества воды n ( H 2 O ).
3. а)Найдем заданную химическим уравнением массу 1кмоль Fe 2 O 3 и запишем полученное значение под его формулой:
М r(Fe 2 O 3 ) = 56 * 2 + 16 * 3 = 160,
М (Fe 2 O 3 ) = 160 кг / кмоль .
б) Найдем заданный уравнением объем 3 кмоль водорода V = Vm * n , запишем под формулой водорода найденное значение: V (3 H 2) = 22,4 м 3 /кмоль * 3 кмоль = 67,2 м 3 .
в) Под формулой воды укажем ее количество, заданное уравнением, — 3 кмоль.
Уравнение принимает вид
230кг х м 3 y кмоль
160 кг 67,2 м 3 3 кмоль
4. Составим и решим пропорции:
а) 230 = х , х = 230*67,2 = 201,6 (м 3 ) – объем водорода V ( H 2)
б) 230 = y , y = 230*3 = 9 (кмоль) – количество вещества воды n ( H 2 O ).
4.Первичное закрепление знаний (10 – 12 мин.)
Решите задачи (если можно, то несколькими способами):
Задача 1. В реакцию с кислородом вступает 0,1 моль цинка. Какое количество вещества кислорода потребуется? Какое количество вещества оксида цинка образуется?
Задача 2. Цинк количеством вещества 0,1 моль взаимодействует с кислородом. Определите массу кислорода, вступающего в реакцию, а также массу образующегося оксида цинка.
Задача 3. Алюминий массой 6,3 г вступает в реакцию с кислородом. Определите массы кислорода и образующегося оксида железа, если алюминий содержит 20% примесей.
Задача 4. Какой объем водорода (н.у.) выделится при взаимодействии 2,7 г 25% — й соляной кислоты с необходимым по реакции количеством вещества алюминия? Каково это количество вещества?
Задача 5. Какой объем углекислого газа выделится при сгорании 60 кг угля?
Задача 6. Сколько молей оксида кальция образуется при сжигании в кислороде 8 г кальция, содержащего 30% примесей?
5. Итог урока (1 -3 мин.)
Сегодня на уроке мы с вами еще раз вспомнили написание химических уравнений и научились проводить расчеты с помощью химических уравнений.
http://urok.1sept.ru/articles/612236
http://infourok.ru/urok-po-himii-dlya-klassa-rascheti-po-himicheskim-uravneniyam-477221.html