Химические уравнения встречающиеся в природе
Горение тоже происходит при участии кислорода. В результате древесина (и другое твердое топливо) превращается в золу, а это вещество с совершенно другим составом и свойствами. Кроме того, в процессе горения выделяется большое количество теплоты и света, а также газа.
С химической точки зрения горение – это окислительная реакция, которая протекает с очень большой скоростью. А при очень-очень высокой скорости реакции может произойти взрыв.
Схематически реакцию можно записать так: вещество + О 2 → оксиды + энергия.(2)

По сути, это тот же процесс, что и горение, только протекает он гораздо медленней. Гниение представляет собой взаимодействие сложных азотосодержащих веществ с кислородом при участии микроорганизмов. Наличие влаги является одним из факторов, способствующих возникновению гниения.
В результате химических реакций из белка образуется аммиак, жирные летучие кислоты, углекислота, оксикислоты, спирты, амины, скатол, индол, сероводород, меркаптаны. Часть из образованных в результате гниения азотосодержащих соединений ядовито.(3)
В природе озон в большинстве своем образуется благодаря облучению воздуха ультрафиолетовыми лучами Солнца 3О 2 + УФ свет → 2О 3
А также при электрических разрядах молний во время грозы.
В грозу под воздействием молний часть молекул кислорода распадается на атомы, молекулярный и атомарный кислород соединяются, и образуется О 3 .
Вот почему мы ощущаем особую свежесть после грозы, нам легче дышится, воздух кажется более прозрачным. Дело в том, что озон гораздо более сильный окислитель, чем кислород. И в небольшой концентрации (как после грозы) безопасен. И даже полезен, поскольку разлагает вредные вещества в воздухе. По сути, дезинфицирует его.
Однако в больших дозах озон очень опасен для людей, животных и даже растений, для них он ядовит.(4)
30 химических реакций повседневной жизни
химические реакции Мы можем найти их в повседневной жизни в целом. Это ответ, который химик мог бы дать вам без ошибок, чтобы преувеличивать.
И это то, что кто-то стремится в этом вопросе будет пытаться увидеть вещи с молекулярной или атомной точки зрения, будет пытаться увидеть реакции повсюду, и молекулы постоянно превращаются.
Люди, разбирающиеся в химии, не могут не видеть вещи с этой точки зрения, точно так же, как физик мог видеть вещи с ядерной точки зрения или биолог с клеточной точки зрения..
Для обоснования комментария ниже я привожу 30 примеров химии, присутствующей в повседневной жизни..
Химические реакции, которые остаются незамеченными дома, на кухне, в саду, на улице или даже внутри нашего тела. Я надеюсь, что это поможет осветить обычную и рутинную химию в повседневной жизни..
30 химических реакций, которые вы видите каждый день в своей жизни
Химия на кухне
1- сольватационные реакции: когда соль растворяется в воде, ионные связи разрушаются, что приводит к сольватации катионов и анионов.
Технически готовят раствор хлорида натрия в воде..
2- Фазовые изменения: При кипячении воды во время приготовления или приготовления кофе или чая происходит фазовое изменение между жидкой водой и газированной водой.
3- реакции горения: Газовые плиты используют пропан для производства пламени.
4- ХлорХлор, используемый в качестве моющего средства, на самом деле представляет собой хлорит натрия, который является восстановителем. Пятна от одежды называются хромофорами и имеют ненасыщенность. Хлор атакует эту ненасыщенность, удаляя цвет пятен. Технически это не удаляет пятно, но делает его невидимым.
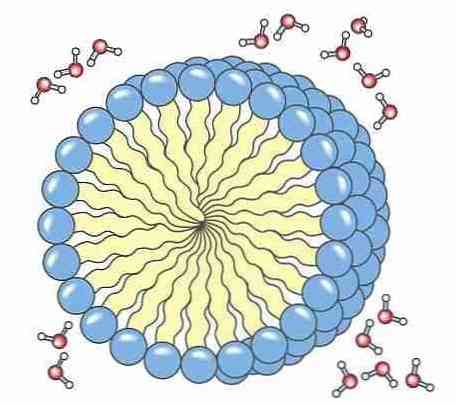
5- мылоМыла и моющие средства имеют полярную часть, обычно карбоновую кислоту, присоединенную к неполярной алифатической цепи, которая дает ей способность образовывать мицеллы. Эти мицеллы обладают способностью окружать грязь, поэтому ее можно удалить с одежды, посуды и нашего тела..
6- Пищевая сода: это слабое основание, которое при взаимодействии с кислотой, такой как уксус или вода (которая является слегка кислой), выделяет углекислый газ.
Это соединение является активным ингредиентом многих антацидов (C., 2015).
7- Среднесрочный: кухня — это химическое изменение, которое меняет пищу, делая ее вкуснее, убивает опасные микроорганизмы и делает их более усвояемыми.
Жар кулинарии может денатурировать белки, стимулировать химические реакции между ингредиентами, карамелизовать сахар и т. Д. (Helmenstine A.M., 10 примеров химических реакций в повседневной жизни, 2017).
8- Искусственный вкус и цвет: многие обработанные пищевые продукты содержат химические вещества, которые придают особый вкус или цвет и способствуют их сохранению.
9- Плачь о луке: лук содержит аминокислотные молекулы сульфоксидов. При разрезании луковых клеточных стенок происходит разрушение, выделяя эти сульфоксиды вместе с ферментами, которые разлагают его до сульфеновых кислот, сероорганического соединения формулы R-SOH, которое раздражает глаза (Reactions, 2016).
Химия в доме
10- АккумуляторыОни используют электродохимические или окислительно-восстановительные реакции для преобразования химической энергии в электрическую. Спонтанные окислительно-восстановительные реакции происходят в гальванических элементах, тогда как не спонтанные химические реакции происходят в электролитических ячейках (Helmenstine, 2017).
11- ЖК-экраны: ЖК-телевизоры содержат спиральные кристаллические молекулы, которые имеют свойство ориентироваться в соответствии с электрическим сигналом и путем изменения тона или цвета, обеспечиваемого светодиодной лампой. Каждая кристаллическая молекула представляет собой пиксель на телевизоре, и чем больше молекул, тем выше разрешение.
12- Старые книги, которые хорошо пахнут: разложение целлюлозы из бумаги книг, придает листьям желтоватый цвет и запах ванили. Если у вас есть старые книги, которые хорошо пахнут в вашей библиотеке, это происходит из-за молекул лигнина или ванилина в нем.
13- Наркотики и наркотикиНекоторые лекарственные средства представляют собой молекулы, которые частично блокируют гормональную активность, вызываемую определенным раздражителем (например, лекарственные средства для снятия напряжения или противоэпилектические средства), в то время как другие являются ферментативными ингибиторами, такими как, например, анальгетики..
14- ШампуньКак шампуни и мыло, шампуни удаляют жир с кожи головы, образуя мицеллы. Ингредиентом, который заботится об этом, обычно являются сульфаты, такие как додецилсульфат или лауриловый эфир сульфата натрия или аммония.
15- Дезодоранты и антиперспиранты: плохой запах подмышек, ног и дыхания вырабатывается бактериями, которые питаются белками и жирами в поте, который выделяет апокринные железы.
У дезодорантов есть химическое соединение, названное триклозаном, который является сильным антибактериальным и фунгицидным средством. С другой стороны, антиперспиранты содержат соли алюминия, которые проникают в поры и предотвращают потоотделение..
16- Косметика и макияжЭто химические вещества и пигменты, которые прилипают к коже. Обычно это неполярные соединения, такие как воски и масла..
Химия в саду
17- Фотосинтез: это процесс, при котором зеленые растения производят свою еду. Это происходит в присутствии солнечного света и другого сырья, а именно углекислого газа и воды. Пигмент хлорофилла собирает световую энергию солнечного света, которая превращается в глюкозу (Crystal, 2017).
18- реакции окисления: на неокрашенных железных поверхностях часто наблюдается оксидное покрытие, которое постепенно приводит к разрушению железа. Это химическое явление, называемое окислением.
В этом случае железо соединяется с кислородом в присутствии воды, что приводит к образованию оксидов железа (химические реакции в повседневной жизни, 2016 г.).
19- Органическое разложениеРазложение органических продуктов питания или даже живых существ — это реакции окисления, вызываемые бактериями, которые разлагают биохимические макромолекулы в простых молекулах, таких как нитриты, нитраты, СО2 и вода (Helmenstine, Примеры химических изменений, 2017).
20- Удобрения: калий, нитраты, фосфаты и сульфаты используются в почвах для обеспечения растений питательными веществами и могут расти.
21- ПестицидыЭто химические вещества, используемые для окуривания сельскохозяйственных культур или садов. Обычно это нейротоксины, которые поражают бактерии или насекомых, которые потребляют зерновые культуры..
Химия на улице
22- Сжигание бензина: автомобили используют бензин в качестве топлива за счет контролируемых взрывов, которые приводят в движение поршни двигателей.
23- Дым машин: вырабатывает свободные радикалы, которые являются очень реактивными соединениями и атакуют кожу или волосы, делая их сухими и ломкими, не говоря уже о том, что они канцерогенные.
24- кислотный дождь: избыток серы и оксидов азота в атмосфере, производимых заводами и автомобилями, растворяется в воде облаков с образованием серной, серной и азотной кислоты, которая выпадает в осадок в виде кислотных дождей.
25- Конструкции: цемент и другие материалы, используемые при строительстве домов, такие как картины, штукатурка и многие другие, являются продуктами химии. В частности, цемент сделан из молекул гидроксида кальция, также называемых негашеной известью.
Химия в вашем теле
26- Пищеварение: пищеварение основано на химических реакциях между пищевыми продуктами и кислотами и ферментами, которые расщепляют молекулы на питательные вещества, которые организм может усваивать и использовать.
27- Аэробное дыхание: основным процессом, который производит энергию в организме, является аэробный гликолиз. Здесь дыхание помогает расщеплять глюкозу (источник энергии) в воде, углекислый газ и энергию в форме АТФ. С6H12О6 + 6O2 → 6CO2 + 6H2O + Энергия (36 АТП)
28- Анаэробное дыхание: из-за перенапряжения, иногда клетки нашего организма истощаются и дышат анаэробно. Это вызывает синтез молочной кислоты. Анаэробное дыхание наблюдается у некоторых бактерий, дрожжей и других организмов. Уравнение анаэробного дыхания:
29- Мускульное движение: напряжение или расслабление мышц происходит из-за конформационных изменений белков скелетных мышц. Эти изменения происходят благодаря фосфокреатину, который при потере фосфата высвобождает энергию для процесса.
30- Мысль: это сложный биохимический процесс, в котором разность ионного потенциала создает электрические импульсы нейронов (Али, 2013).
Химические реакции: типы, свойства, уравнения
Содержание:
Характеристика реакций
Химические реакции, их свойства, типы, условия протекания и прочая, являются одним из краеугольных столпов интересной науки под названием химия. Попробуем же разобрать что такое химическая реакция, и какова ее роль. Итак, химической реакцией в химии принято считать превращение одного либо нескольких веществ, в другие вещества. При этом ядра атомов у них не меняются (в отличие от реакций ядерных), зато происходит перераспределение электронов и ядер, и, разумеется, появляются новые химические элементы.
Реакции в природе и быту
Мы с вами окружены химическими реакциями, более того мы сами их регулярно осуществляем различными бытовыми действиями, когда например, зажигаем спичку. Особенно много химических реакций сами того не подозревая (а может и подозревая) делают повара, когда готовят еду.
Разумеется, и в природных условиях проходит множество химических реакций: извержение вулкана, фотосинтез листвы и деревьев, да что там говорить, практически любой биологический процесс можно отнести к примерам химических реакций.
Типы реакций
Все химические реакции можно условно разделить на простые и сложные. Простые химические реакции, в свою очередь, разделяются на:
- реакции соединения,
- реакции разложения,
- реакции замещения,
- реакции обмена.
Далее мы подробно остановимся на каждом из этих видов химических реакций, известных химии.
Реакция соединения
По весьма меткому определению великого химика Д. И. Менделеева реакция соединения имеет место быть когда «их двух веществ происходит одно». Примером химической реакции соединения может быть нагревание порошков железа и серы, при которой из них образуется сульфид железа – Fe+S=FeS. Другим ярким примеров этой реакции является горение простых веществ, таких как сера или фосфор на воздухе (пожалуй, подобную реакцию можно также назвать тепловой химической реакцией).
Реакция разложения
Тут все просто, реакция разложения является противоположностью реакции соединения. При ней из одного вещества получается два или более веществ. Простым примером химической реакции разложения может быть реакция разложение мела, в ходе которой из собственно мела образуется негашеная известь и углекислый газ.
Реакция замещения
Реакция замещения осуществляется при взаимодействии простого вещества со сложным. Приведем пример химической реакции замещения: если опустить стальной гвоздь в раствор с медным купоросом, то в ходе этого простого химического опыта мы получим железный купорос (железо вытеснит медь из соли). Уравнение такой химической реакции будет выглядеть так:
Реакция обмена
Реакции обмена проходят исключительно между сложными химическими веществами, в ходе которых они меняются своими частями. Очень много таких реакций имеют место быть в различных растворах. Нейтрализация кислоты желчью – вот хороший пример химической реакции обмена.
Так выглядит химическое уравнение этой реакции, при ней ион водорода из соединения HCl обменивается ионом натрия из соединения NaOH. Следствием этой химической реакции является образование раствора поваренной соли.
Признаки реакций
По признакам протекания химических реакций можно судить прошла ли химическая реакция между реагентами или нет. Приведем примеры признаков химических реакций:
- Изменение цвета (светлое железо, к примеру, во влажном воздухе покрывается бурым налетом, как результат химической реакции взаимодействия железа и кислорода).
- Выпадение осадка (если вдруг через известковый раствор пропустить углекислый газ, то получим выпадение белого нерастворимого осадка карбоната кальция).
- Выделение газа (если Вы капнете на пищевую соду лимонной кислотой, то получите выделение углекислого газа).
- Образование слабодиссоциированных веществ (все реакции, в результате которых образуется вода).
- Свечение раствора (примером тут могут служить реакции, происходящие с раствором люминола, излучающего при химических реакциях свет).
В целом, трудно выделить какие признаки химических реакций являются основными, для разных веществ и разных реакций характерны свои признаки.
Как определить признак реакции
Определить признак химической реакции можно визуально (при изменении цвета, свечении), или по результатам этой самой реакции.
Скорость реакции
Под скоростью химической реакции обычно понимают изменение количества одного из реагирующих веществ за единицу времени. Притом, скорость химической реакции всегда положительная величина. В 1865 году химиком Н. Н. Бекетовым был сформулирован закон действия масс гласящий, что «скорость химической реакции в каждый момент времени пропорциональна концентрациям реагентов, возведенным в степени, равные их стехиометрическим коэффициентам».
К факторам скорости химической реакции можно отнести:
- природу реагирующих веществ,
- наличие катализатора,
- температуру,
- давление,
- площадь поверхности реагирующих веществ.
Все они имеют самое прямое влияние на скорость протекания химической реакции.
Равновесие реакции
Химическим равновесием называют такое состояние химической системы, при котором протекает несколько химических реакций и скорости в каждой паре прямой и обратной реакции равны между собой. Таким образом, выделяется константа равновесия химической реакции – это та величина, которая определяет для данной химической реакции соотношение между термодинамическими активностями исходных веществ и продуктов в состоянии химического равновесия. Зная константу равновесия можно определить направление протекания химической реакции.
Условия возникновения реакций
Чтобы положить начало химических реакций, необходимо для этого создать соответствующие условия:
- приведение веществ в тесное соприкосновение.
- нагревание веществ до определенной температуры (температура химической реакции должна быть подходящей).
Тепловой эффект химической реакции
Так называют изменение внутренней энергии системы как результат протекания химической реакции и превращения исходных веществ (реактантов) в продукты реакции в количествах, соответствующих уравнению химической реакции при следующих условиях:
- единственно возможной работой при этом есть только лишь работа против внешнего давления.
- исходные вещества и продукты, полученные в результате химической реакции, имеют одинаковую температуру.
Видео
И в завершение интересно видео про самые удивительные химические реакции.
Автор: Павел Чайка, главный редактор журнала Познавайка
При написании статьи старался сделать ее максимально интересной, полезной и качественной. Буду благодарен за любую обратную связь и конструктивную критику в виде комментариев к статье. Также Ваше пожелание/вопрос/предложение можете написать на мою почту pavelchaika1983@gmail.com или в Фейсбук, с уважением автор.
Эта статья доступна на английском языке – Chemical Reactions.
Похожие посты:
4 комментария
Спасибо за статью, хотелось бы также больше узнать про химические реакции ферментов и необратимые химические реакции.
Пожалуй эти темы заслуживают отдельной статьи.
1. Вы пишете: “Зная константу равновесия можно определить направление протекания химической реакции.” Одного знания константы равновесия бывает недостаточно. В общем случае, необходимо знать еще концентрации веществ.
2. Про тепловой эффект реакции сразу видно, что переписан без пояснений соответствующий абзац из учебника. Может даже не школьного. Но народу будет не до конца понятно.
3. В начале статьи вы заикаетесь о биохимических реациях и далее даже говорите о том, что есть сложные реакции. И далее не слова про них. Интуитивно понятно, что сложные реакции это совокупность нескольких. Но по хорошему надо бы хотя бы обозначить определение. И пару предложений сказать про биохимические реакции
4. Вы пишете: “К факторам скорости химической реакции можно отнести:
природу реагирующих веществ,
наличие катализатора,
температуру,
давление,
площадь поверхности реагирующих веществ.
Все они имеют самое прямое влияние на скорость протекания химической реакции.” Перфекционисту, такое утверждение будет резать слух. Например, вы ничего не говорите о концентрациях, а также не разделяете гомогенные и гетерогенные реакции-для них немного разный набор влияющих факторов. Некоторые из указанных вами факторов не так сильно влияют на скорость (если влияют вообще).
4. Указывая признаки протекания химической реакции вы выделяете яркие, заметные но не всегда проявляемые факторы, а также не эти признаки являются фундаментальным признаком протекания химической реакции. Таковым является изменение количества(концентрации) реагирующих веществ. И именно эти изменения фиксируют, т.н. кинетические кривые, снимаемые по ходу реакции графики зависимости какого-либо параметра от количества вещества.
5. Если уж вас спросили в комментариях, и вы сами вкратце касаетесь понятия химического равновесия и т.н. константы равновесия можете в дальнейшем указать, что необратимые это те реакции, у которых очень большое значение константы равновесия.
И еще предложение “При этом ядра атомов у них не меняются (в отличие от реакций ядерных), зато происходит перераспределение электронов и ядер, и, разумеется, появляются новые химические элементы.” Перечитайте! Кто отличает ядерные реакции от химических (условно говоря, 90% школьников) им это предложение ни к чему. А кто захочет разобраться (те самые 10% кто не различает ядерные и химические реакции) они ничего не поймут!
http://ru.thpanorama.com/articles/qumica/30-reacciones-qumicas-de-la-vida-cotidiana.html
http://www.poznavayka.org/himiya/himicheskie-reaktsii-tipyi-svoystva-uravneniya/