Гидрид калия: способы получения и химические свойства
Гидрид калия KH — неорганическое бинарное соединение щелочного металла калия и водорода. Белое кристаллическое вещество. При нагревании разлагается, под избыточным давлением плавится без разложения.
Относительная молекулярная масса Mr = 40,11; относительная плотность для тв. и ж. состояния d = 1,43; tпл ≈ 400º C при избыточном давлении
Способ получения
Гидрид калия получают реакцией взаимодействия калия и водорода при 200–350º C:
2K + H2 = 2KH
Химические свойства
1. Гидрид калия — сильный восстановитель. Поэтому он реагирует почти со всеми неметаллами.
1.1. При взаимодействии с кислородом при температуре выше 200º C гидрид калия образует гидроксид калия:
2KH + O2 = 2KOH
1.2. При температуре 400–450º C г идрид калия взаимодействует с хлором, образуя хлорид калия и хлороводород:
KH + Cl2 = KCl + HCl
2. Гидрид калия взаимодействует со сложными веществами :
2.1. При взаимодействии с водой гидрид калия образует гидроксид калия и газ водород:
KH + H2O = KOH + H2↑
2.2. С разбавленной хлороводородной кислотой гидрид калия реагирует с образованием хлорида калия и газа водорода:
KH + HCl = KCl + H2↑
2.3. Гидрид калия реагирует с газом аммиаком при t = 300º C с образованием нитрида калия и водорода:
3. Гидрид калия разлагается при температуре 400º C и вакууме, с образованием калия и водорода:
Гидрид калия
| Гидрид калия | |
|---|---|
 K + H − K + H − | |
| Систематическое наименование | калия гидрид |
| Хим. формула | KH |
| Рац. формула | HK |
| Состояние | белое твердое вещество |
| Молярная масса | 40.1062 г/моль |
| Плотность | 1.47 г/см³ |
| Температура | |
| • плавления | 400 °C |
| Мол. теплоёмк. | 37,91 Дж/(моль·К) |
| Энтальпия | |
| • образования | -57,82 кДж/моль |
| Растворимость | |
| • в веществах | бензол: не растворим |
диэтиловый эфир: не растворим
сероуглерод: не растворим
этанол: реагирует

Гидрид калия — это неорганическое бинарное химическое соединение белого цвета. Химическая формула KH.
Содержание
- 1 Физические свойства
- 2 Химические свойства
- 3 Получение
- 4 Токсичность
Физические свойства
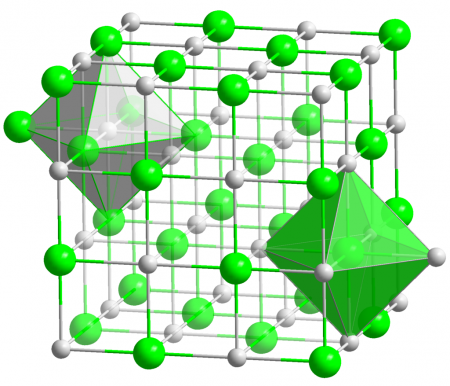
Гидрид калия образует бесцветные ионные кристаллы кубической сингонии с решеткой типа NaCl (a = 0.57 нм). Хорошо растворим в расплавленном калии, не растворяется в органических растворителях. Обладает высокой теплопроводностью.
Химические свойства
Гидрид калия является ионным соединением K + H − . Его расплав проводит электрический ток, при электролизе на аноде выделяется водород.
Вещество нестабильно и при нагревании распадается на компоненты:
2KH → 400oC,vacuum 2K + H2
Гидрид калия обладает высокой химической активностью, является сильным восстановителем. Окисляется кислородом:
2KH + O2 → 200oC 2KOH
Взаимодействует с водой:
KH + HCl → KCl + H2↑
и газообразным аммиаком:
Взаимодействует с галогенами:
KH + Cl2 → 400oC KCl + HCl↑
С углекислотой образует формиат калия:
KH + CO2 → 150oC,p K(HCOO)
Взаимодействует с оксидом кремния:
Получение
Гидрид калия получают прямой реакцией расплавленного калия с водородом под давлением:
2K + H2 → 200−350oC,p 2KH
Эта реакция была открыта Гемфри Дэви вскоре после его открытия в 1807 году калия, когда он отметил, что металл будет испаряться в токе водорода при нагревании только ниже точки кипения.
Токсичность

Свойства калия и его взаимодействие с водой
Почему его нельзя хранить на открытом воздухе
Калий — девятнадцатый элемент периодической таблицы Менделеева, относится к щелочным металлам. Это простое вещество, которое при нормальных условиях пребывает в твердом агрегатном состоянии. Закипает калий при температуре 761 °С. Температура плавления элемента — 63 °С. Калий имеет серебристо-белую окраску с металлическим блеском.
Химические свойства калия
Калий — элемент, обладающий высокой химической активностью, поэтому его нельзя хранить на открытом воздухе: щелочной металл моментально вступает в реакцию с окружающими веществами. Этот химический элемент относится к I группе и IV периоду таблицы Менделеева. Калий обладает всеми характерными для металлов свойствами.
Он взаимодействует с простыми веществами, к которым относятся галогены (бром, хлор, фтор, иод) и фосфор, сера, азот и кислород. Взаимодействие калия с кислородом называется окислением. В течение этой химической реакции кислород и калий расходуются в молярном соотношении 4:1, в результате чего образуется оксид калия в количестве двух частей. Такое взаимодействие можно выразить уравнением реакции:
Во время горения калия наблюдается пламя ярко-фиолетового цвета.
Такое взаимодействие считается качественной реакцией на определение калия. Реакции калия с галогенами называются в соответствии с названиями химических элементов: это фторирование, иодирование, бромирование, хлорирование. Такие взаимодействия являются реакциями присоединения. Пример — реакция между калием и хлором, в результате которой образуется хлорид калия. Для проведения такого взаимодействия берут два моля калия и один моль хлора. В результате образуется два моля калия:
При горении на открытом воздухе калий и азот расходуются в молярном соотношении 6:1. В результате такого взаимодействия образуется нитрид калия в количестве двух частей:
Соединение представляет собой кристаллы зелено-черного цвета. С фосфором калий реагирует по такому же принципу. Если взять 3 моля калия и 1 моль фосфора, получится 1 моль фосфида:
Калий реагирует с водородом, образуя гидрид:
Все реакции присоединения происходят при высоких температурах
Взаимодействие калия со сложными веществами
К сложным веществам, с которыми вступает в реакцию калий, относятся вода, соли, кислоты и оксиды. Так как калий — активный металл, он вытесняет атомы водорода из их соединений. Пример — реакция, происходящая между калием и соляной кислотой. Для ее проведения берется по 2 моля калия и кислоты. В результате реакции образуется 2 моля хлорида калия и 1 моль водорода:
2К + 2НСІ = 2КСІ + Н₂
Более детально стоит рассмотреть процесс взаимодействия калия с водой. Калий бурно взаимодействует с водой. Он движется по поверхности воды, его подталкивает выделяющийся водород:
2K + 2H₂O = 2KOH + H₂↑
В ходе реакции в единицу времени выделяется много тепла, что приводит к воспламенению калия и выделяющегося водорода. Это очень интересный процесс: при контакте с водой калий мгновенно воспламеняется, фиолетовое пламя потрескивает и быстро передвигается по поверхности воды. В конце реакции происходит вспышка с разбрызгиванием капель горящего калия и продуктов реакции.
Основной конечный продукт реакции калия с водой — гидроксид калия (щелочь). Уравнение реакции калия с водой:
4K + 2H₂O + O₂ = 4KOH
Внимание! Не пытайтесь повторить этот опыт самостоятельно!
При неправильном проведении эксперимента можно получить ожог щелочью. Для реакции обычно используют кристаллизатор с водой, в который помещают кусочек калия. Как только водород прекращает горение, многие хотят заглянуть в кристаллизатор. В этот момент происходит завершающая стадия реакции калия с водой, сопровождающаяся слабым взрывом и разбрызгиванием образовавшейся горячей щелочи. Поэтому в целях безопасности стоит держаться на некотором расстоянии от лабораторного стола, пока реакция не завершится полностью. Здесь вы найдете самые зрелищные опыты, которые можно проводить с детьми дома.
Строение калия
Атом калия состоит из ядра, в котором содержатся протоны и нейтроны, и электронов, вращающихся вокруг него. Количество электронов всегда равно количеству протонов, находящихся внутри ядра. При отсоединении электрона или при присоединении к атому он перестает быть нейтральным и превращается в ион. Ионы делятся на катионы и анионы. Катионы обладают положительным зарядом, анионы — отрицательным. При присоединении к атому электрона он превращается в анион; если же один из электронов покидает свою орбиту, нейтральный атом превращается в катион.
Порядковый номер калия в периодической таблице Менделеева — 19. Значит, протонов в ядре химического элемента находится тоже 19. Вывод: электронов вокруг ядра расположено 19. Количество протонов в структуре атома определяется так: от атомной массы отнять порядковый номер химического элемента. Вывод: в ядре калия находится 20 протонов. Калий принадлежит к IV периоду, имеет 4 «орбиты», на которых равномерно располагаются электроны, пребывающие в постоянном движении. На первой «орбите» расположены 2 электрона, на второй — 8; на третьей и на последней, четвертой «орбите», вращается 1 электрон. Этим объясняется высокий уровень химической активности калия: его последняя «орбита» не заполнена полностью, поэтому элемент стремится соединиться с другими атомами. В результате электроны последних орбит двух элементов станут общими.
http://chem.ru/gidrid-kalija.html
http://melscience.com/RU-ru/articles/svojstva-kaliya-i-ego-vzaimodejstvie-s-vodoj/
