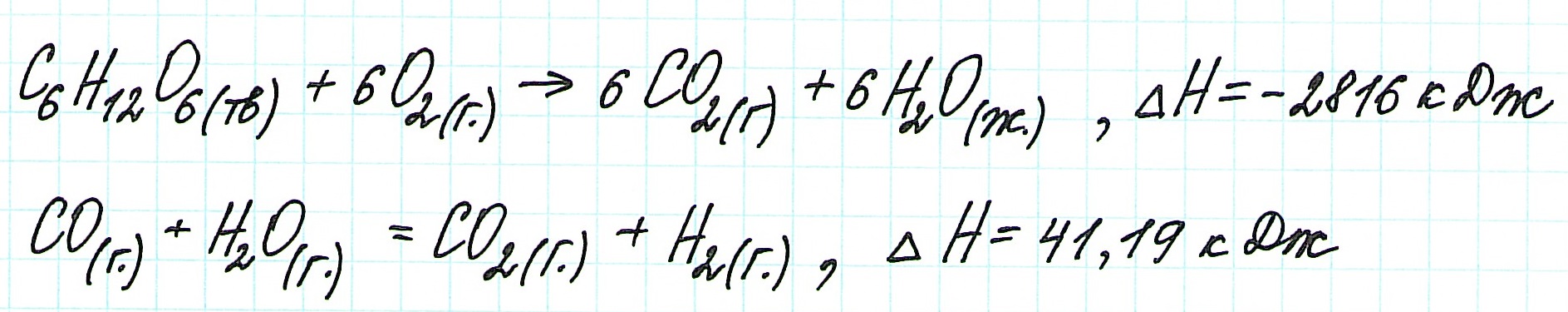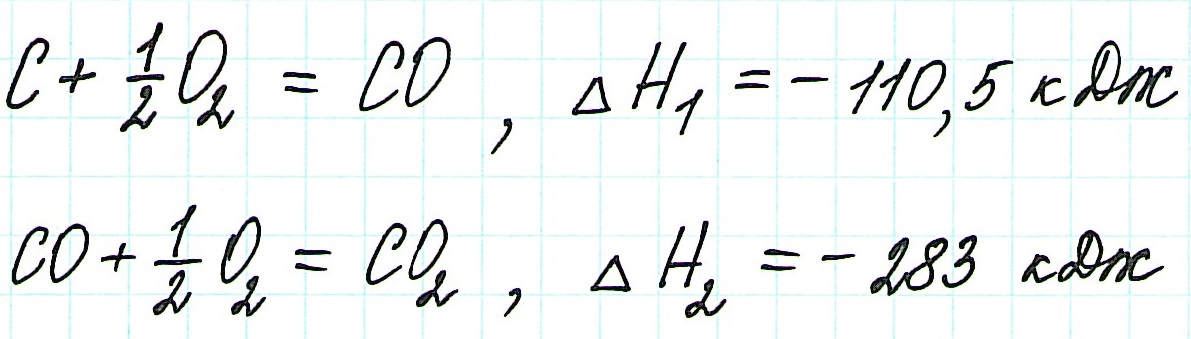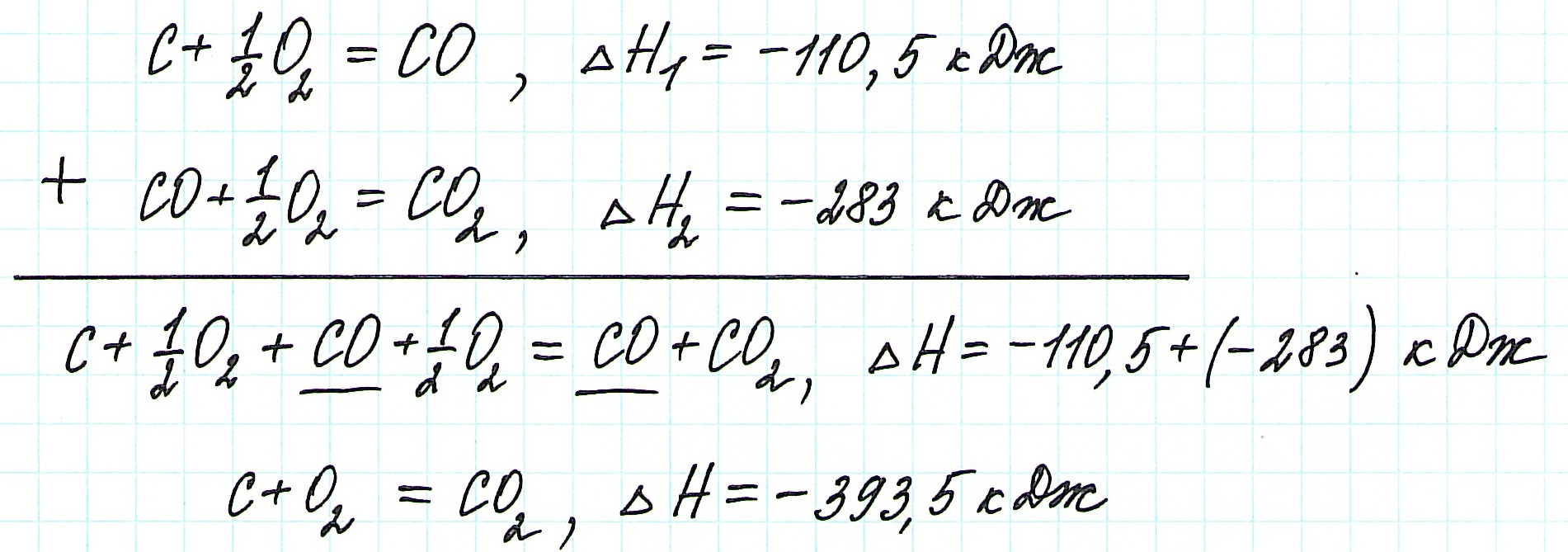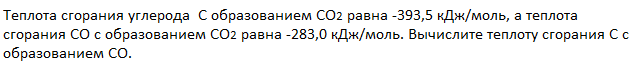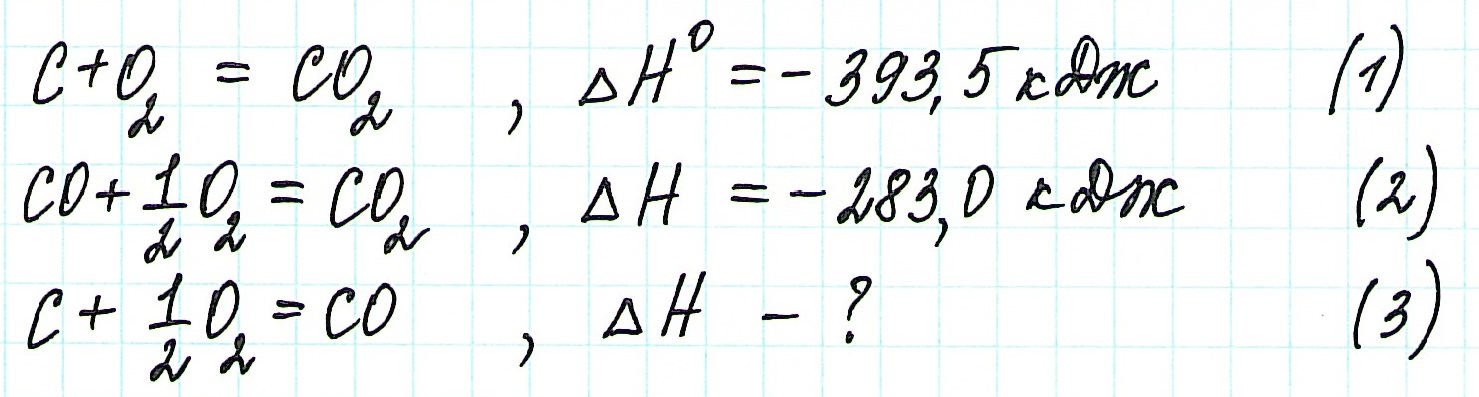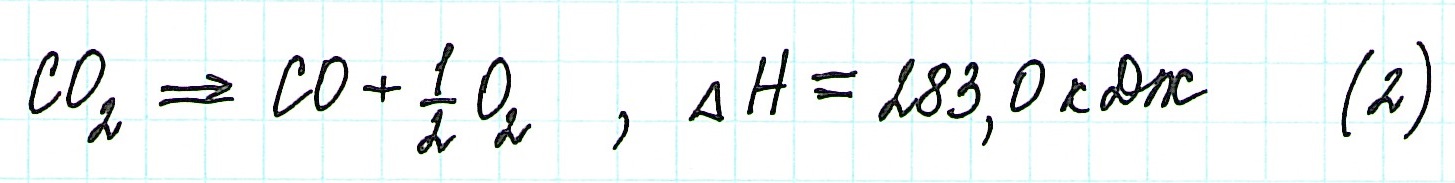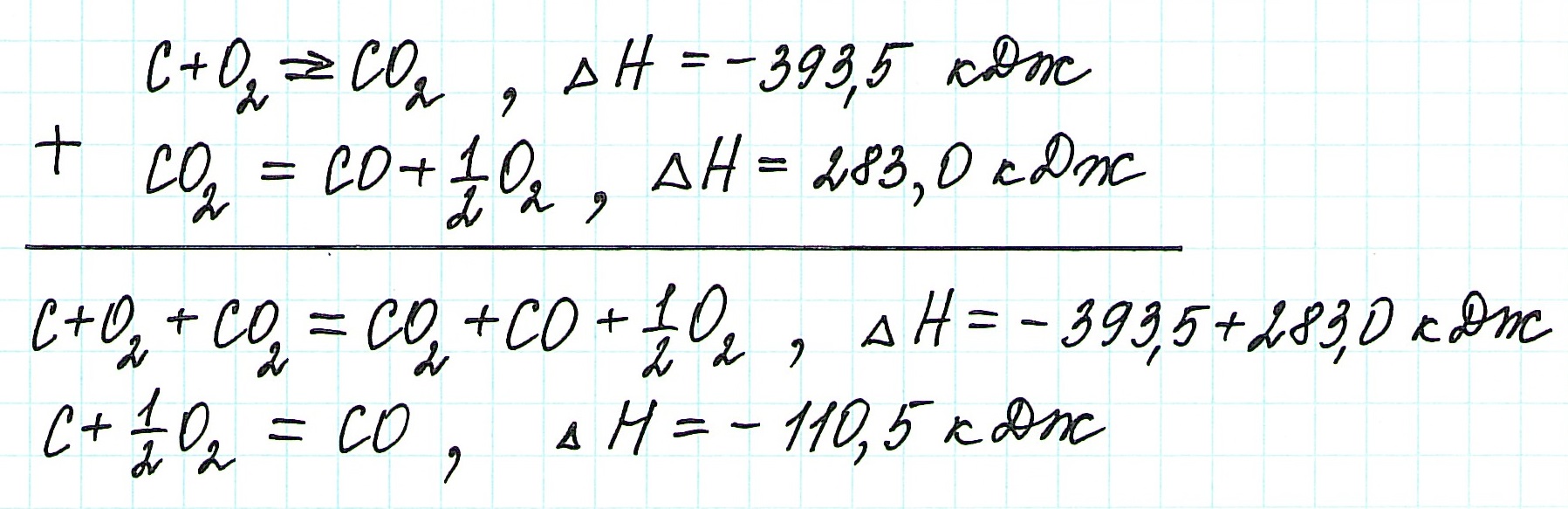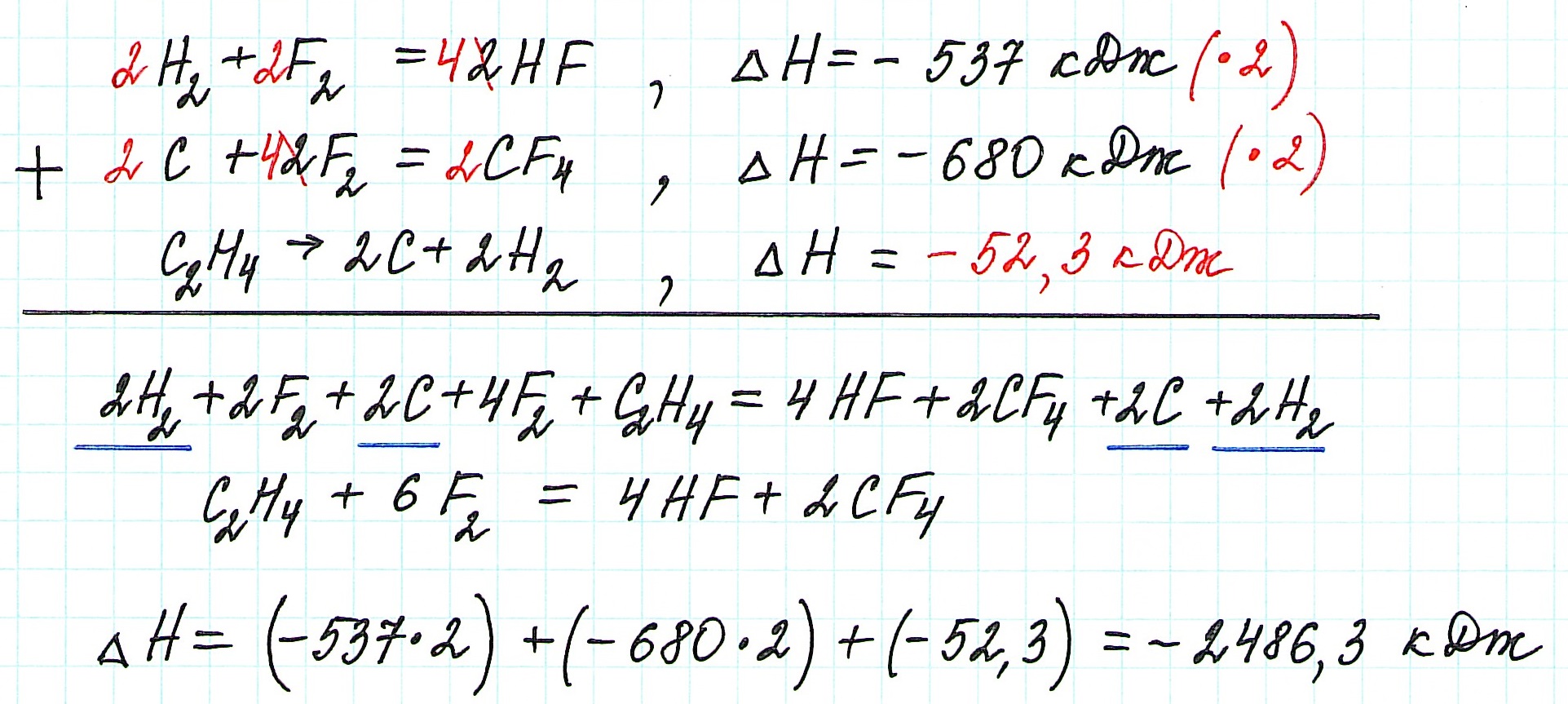ЗАКОН ГЕССА И ЕГО СЛЕДСТВИЯ: РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ
Закон Гесса (1840 г.) представляет собой частный случай закона сохранения энергии. Он позволяет определить тепловой эффект химического взаимодействия, используя данные о состояниях веществ только в начале и в конце процесса. Для этого применяется так называемая формула закона Гесса, оформленная в виде формулировки следствия из него.
Итак, что же из себя представляет закон, о котором идет речь? Как, пользуясь им, можно проводить вычисления?
Экзотермические и эндотермические реакции
Основной категорией химического процесса, с которой закон Гесса имеет дело, является тепловой эффект – главный объект термохимии.
Тепловым эффектом Q считают теплоту, либо подающуюся в систему, либо выделяющуюся из нее в ходе химического взаимодействия.
Так, если теплота подается в систему (то есть поглощается из внешней среды), то процесс является эндотермическим. Если теплота, наоборот, уходит из системы в окружающую среду, то процесс является экзотермическим.
Каждая реакция отображается с помощью уравнения. Если в уравнении указан тепловой эффект химического процесса, то такое уравнение называется термохимическим. В нем обязательно записываются либо агрегатные состояния веществ, определяющие общее состояние системы, либо их аллотропные модификации (в случае простых веществ).
Обозначения агрегатных состояний записываются нижним индексом в скобках рядом с химической формулой вещества.
Например, для экзотермического процесса:
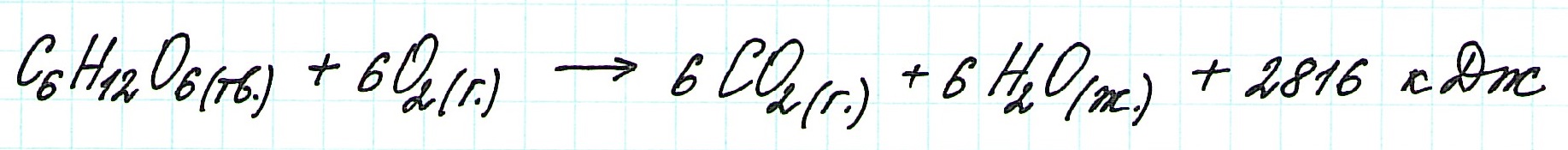

— (тв.) – твердое, или (к.) – кристаллическое;
Тепловой эффект Q реакции и изменение энтальпии ΔН имеют одинаковые численные значения, а по знаку противоположны:
В связи с этим приведенные выше уравнения можно записать так:
Закон Гесса как основной закон термохимии и примеры расчетов с его использованием
Закон Гесса констатирует:
При экзотермическом взаимодействии углерода (графита) и кислорода образуется углекислый газ. У этого процесса есть два возможных пути: напрямую или через промежуточную стадию, идущую с образованием угарного газа (оксида углерода (II)):
При прямом процессе, идущем непосредственно с образованием углекислого газа, выделяется 393,5 кДж энергии:
Если процесс взаимодействия графита с кислородом идет в две стадии, то каждая из них также сопровождается выделением энергии:
Просуммируем эти два уравнения:
Получаем то же, что и в первом случае (то есть при прямом взаимодействии графита с кислородом): выделяется 393,5 кДж энергии.
Таким образом, результат реакции совершенно не зависит как от пройденного пути, так и от количества промежуточных стадий. Важными оказываются состояния веществ: начальное и конечное.
Прежде, чем рассмотреть примеры расчетов, в которых используется формула закона Гесса, необходимо сделать некоторые уточнения:
1) результаты термохимических расчетов (и измерений) всегда относят к одному молю вещества, которое образуется в ходе реакции;
2) теплота образования – это количество теплоты, выделяющееся при реакции простых веществ с образованием 1 моля продукта;
3) теплоты образования простых веществ принимают за ноль;
4) если прямой процесс является экзотермическим, то обратный будет эндотермическим, и наоборот.
Пример 1.
Запишем термохимические уравнения реакций, о которых идет речь:
Представим уравнение (2) так, чтобы СО стал конечным продуктом реакции, а не исходным веществом. Для этого запишем уравнение в обратном виде. Теплота сгорания по знаку в таком случае станет противоположной:
Для получения ответа на вопрос задачи (по закону Гесса) просуммируем уравнения (1) и (2):
Таким образом, при сгорании углерода с образованием угарного газа выделяется 110,5 кДж энергии.
Пример 2.
В реакции, для которой требуется вычислить теплоту:
- участвуют 1 молекула этилена и 6 молекул фтора;
- образуются 2 молекулы тетрафторуглерода и 4 молекулы фтороводорода.
— в первой из данных по условию реакций все коэффициенты и теплоту реакции умножим на 2, чтобы получить 4 молекулы фтороводорода;
— во второй реакции также все коэффициенты и теплоту реакции умножим на 2, чтобы получить 2 молекулы тетрафторуглерода;
— уравнение третьей реакции запишем в обратном виде, чтобы этилен стал исходным веществом, а не продуктом реакции;
— изменим знак теплоты третьей реакции на противоположный, так как ее уравнение записываем в обратном виде.
Просуммируем все уравнения:
Таким образом, теплота реакции этилена с фтором ΔН= -2486,3 кДж.
Следствие из закона Гесса: вычисление энтальпии реакции
Чаще всего в вычислениях применяется не сам закон Гесса, а следствие из него. Оно позволяет вычислить как изменение энтальпии реакции, так и энтальпию образования любого из участников химического взаимодействия.
Следствие утверждает, что

А если учесть коэффициенты, то так:
Для вычислений обычно применяют стандартные энтальпии образования, так как именно в стандартных состояниях вещества наиболее устойчивы:
Стандартные теплоты (энтальпии) образования являются табличными величинами.
Задача 1. Используя данные таблицы стандартных термодинамических величин , вычислите изменение энтальпии для реакции:
Решение:
Задача 2.
Решение:
Задача 3. 
Тепловой эффект в термодинамическом уравнении относят к 1 молю образующегося вещества. С учетом этого запишем уравнение реакции следующим образом:
Следовательно, для данной реакции термохимическое уравнение будет выглядеть так:
В дополнение ко всему сказанному отметим, что некоторые тепловые эффекты реакций, идущих при стандартном давлении, меняются с температурой. Однако эти изменения незначительны. Поэтому при выполнении термодинамических вычислений для нестандартных условий можно использовать стандартные величины теплот образования. Появится в итоге небольшая ошибка, что вполне допускается.
Таким образом, закон Гесса, а также следствие из него позволяют проводить расчеты, в основе которых лежат тепловые явления химических процессов.
Далее будут рассмотрены случаи, в которых используется формула закона Гесса для расчета таких термодинамических величин, как энтропия и энергия Гиббса.
Энергетика химических процессов. Закон Гесса
Материалы портала onx.distant.ru
Тепловой эффект процесса
Количество выделенной (или поглощенной) теплоты Q в данном процессе называют тепловым эффектом процесса. Экзотермической является реакция, протекающая с выделением теплоты, а эндотермической – с поглощением теплоты из окружающей среды.
Для лабораторных и промышленных процессов наиболее типичен изобарный режим (Р=const). Поэтому обычно рассматривают тепловой эффект при Р,Т = const, т.е. изменение энтальпии процесса ΔН.
Следует отметить, что абсолютные значения энтальпии Н определить не представляется возможным, так как не известна абсолютная величина внутренней энергии.
Для экзотермической реакции (Q > 0) ΔН 0.
Термохимические уравнения
Химические уравнения, в которых дополнительно указывается величина изменения энтальпии реакции, а также агрегатное состояние веществ и температура, называются термохимическими уравнениями.
В термохимических уравнениях отмечают фазовое состояние и аллотропные модификации реагентов и образующихся веществ: г – газообразное, ж – жидкое, к – кристаллическое; S(ромб), S(монокл), С(графит), С(алмаз) и т.д.
Важно подчеркнуть, что с термохимическими уравнениями можно проводить алгебраические операции сложения, вычитания, деления, умножения.
Закон Гесса
Изменение энтальпии (внутренней энергии) химической реакции зависит от вида, состояния и количества исходных веществ и продуктов реакции, но не зависит от пути процесса.
Следствия из закона Гесса
- Изменение энтальпии реакции равно сумме энтальпий образования продуктов реакции за вычетом суммы энтальпий образования исходных веществ (суммирование проводится с учетом стехиометрических коэффициентов).
- Изменение энтальпии реакции равно сумме энтальпий сгорания исходных веществ за вычетом суммы энтальпий сгорания продуктов реакции (суммирование проводится с учетом стехиометрических коэффициентов).
Стандартные термодинамические величины
Стандартные термодинамические величины – это такие величины, которые относятся к процессам, все ингредиенты которых находятся в стандартных состояниях.
Стандартным состоянием вещества, находящегося в конденсированной фазе (кристаллической или жидкой), является реальное состояние вещества, находящегося при данной температуре и давлении 1 атм.
Следует подчеркнуть, что стандартное состояние может иметь место при любой температуре.
Обычно тепловой эффект (изменение энтальпии) реакции приводится для температуры 25 о С (298,15 К) и давления 101,325 кПа (1 атм), т.е. указывается стандартная энтальпия ΔН о 298.
Стандартные энтальпии образования и сгорания
Стандартная энтальпия образования ΔН о f,298 (или ΔН о обр,298) – это изменение энтальпии в процессе образования данного вещества (обычно 1 моль), находящегося в стандартном состоянии, из простых веществ, также находящихся в стандартном состоянии, причем простые вещества присутствуют в наиболее термодинамически устойчивых состояниях при данной температуре.
Например , ΔН o f,298(Н2О(ж)) = — 285,83 кДж/моль соответствует изменению энтальпии в процессе
при Т = 298,15 К и Р = 1 атм.
Стандартная энтальпия образования простых веществ равна нулю по определению (для наиболее устойчивых их модификаций при данной температуре).
Стандартной энтальпией сгорания ΔН o сгор,298 называют энтальпию сгорания вещества (обычно 1 моль), находящегося в стандартном состоянии с образованием СО2(г), Н2О(ж) и других веществ, состав которых должен быть специально указан. Все продукты сгорания также должны находиться в стандартном состоянии.
Примеры решения задач
Задача 1. Используя справочные термодинамические данные вычислить ΔН o 298 реакции:
Решение. Решим задачу, используя оба следствия из закона Гесса. Ниже для исходных веществ и продуктов реакции приведены значения энтальпий образования и сгорания в кДж/моль (энтальпия сгорания сероводорода до SO2(г) и H2O(ж)):
| Вещество | H2S(г) | O2(г) | SO2(г) | H2O(ж) |
| ΔН o f,298 | -20,60 | 0 | -296,90 | -285,83 |
| ΔН o сгор,298 | -562,10 | 0 | 0 | 0 |
Cогласно первому следствию закона Гесса энтальпия этой реакции ΔН о х.р. равна:
В соответствии со вторым следствием закона Гесса получаем:
ΔН о х.р.,298 = 2ΔН о сгор,298(H2S(г)) = 2(-562,10) = — 1124,20 кДж.
Задача 2. Вычислите ΔН о 298 реакции N2(г) + 3H2(г) = 2NH3(г), используя следующие данные:
Определите стандартную энтальпию образования NH3(г).
Решение. Поскольку с термохимическими уравнениями можно производить все алгебраические действия, то искомое уравнение получится, если:
- разделить на два тепловой эффект первого уравнения и изменить его знак на противоположный, т.е:
- умножить на 3/2 второе уравнение и соответствующую ему величину δН o , изменив ее знак на противоположный:
Таким образом, тепловой эффект реакции N2(г) + 3H2(г) = 2NH3(г) равен:
Δ Н о 298 = (- ΔН о 1/2) + (- 3/2·ΔН о 2) = 765,61 + (- 857,49) = — 91,88 кДж.
Поскольку в рассматриваемой реакции образуется 2 моль NH3(г), то
ΔН о f,298(NH3(г)) = — 91,88/2 = — 45,94 кДж/моль.
Задача 3. Определите энтальпию процесса
если при 298,15 К энтальпия растворения CuSO4(к) в n моль Н2О с образованием раствора CuSO4(р-р, nH2O) равна –40, а энтальпия растворения CuSO4·5H2O(к) с образованием раствора той же концентрации равна +10,5 кДж/моль.
Решение. Составляем цикл Гесса:
ΔН о 1 = ΔН о 2 + ΔН о х (по закону Гесса). Отсюда получаем:
ΔН о х = ΔН о 1 – ΔН о 2 = – 40,0 – 10,5 = -50,5 кДж.
Другой вариант решения.
По закону Гесса: ΔН о 1 = ΔН о х+ ΔН о 3, т.е. при сложении уравнений (2) и (3) получим уравнение (1).
Задача 4. Вычислите энтальпию образования химической связи С= С в молекуле этилена, если его стандартная энтальпия образования равна 52,3 кДж/моль, энтальпия возгонки графита составляет 716,7 кДж/моль, энтальпия атомизации водорода равна +436,0 кДж/моль, энтальпия образования связи С–Н равна –414,0 кДж/моль.
Решение. Составляем цикл Гесса:
ΔН о (С = С) = 52,3 — 2·716,7 — 2·436,0 + 4·414,0 = — 597,1 кДж/моль.
Задачи для самостоятельного решения
1. Составьте уравнение реакции, для которой ΔН о соответствует стандартной энтальпии образования ВaCl2·2H2O(к).
I. Термохимические расчеты. Закон Гесса.
УЧЕБНО-МЕТОДИЧЕСКОЕ ПОСОБИЕ
К практическим занятиям
по дисциплине «Общая и неорганическая химия»
Тема: «Термохимические расчеты. Закон Гесса.
Химическое равновесие. Правило Ле-Шателье».
«Термохимические расчеты. Закон Гесса.
Химическое равновесие. Правило Ле-Шателье».
МЕТОДИЧЕСКОЕ ПОСОБИЕ
К практическим занятиям
по дисциплине «Общая и неорганическая химия»
Ответственный редактор Гуляева Т.Г.
Рецензенты: к.т.н., доцент кафедры «Физика» Горин С.В.
к.б.н., доцент кафедры «Инженерная защита окружающей среды»
Методическое пособие предназначено для студентов 1 курса специальности 330200 «Инженерная защита окружающей среды».
Методическое пособие содержит сведения об энергетических эффектах, сопровождающих химические процессы, направления и пределы их самопроизвольного протекания. Рассмотрены основы термохимии, направленность химических реакций и химическое равновесие.
Лицензия на издательскую деятельность
Код 221. Серия ИД №01734 от 11 мая 2000г.
Термохимические расчеты. Закон Гесса. Химическое равновесие. Правило Ле-Шателье.
Методическое пособие предназначено для студентов 1 курса, специальность 330200 «Инженерная защита окружающей среды».
Методическое пособие содержит общие сведения об энергетических эффектах, сопровождающих химические процессы, направление и пределы их самопроизвольного протекания. Рассмотрены основы термохимии, направленность химических реакций и химическое равновесие.
I. Термохимические расчеты. Закон Гесса.
Наука о взаимных превращениях различных видов энергии называется термодинамикой. Раздел термодинамики, изучающий тепловые эффекты химических реакций, называется термохимией. Реакции, которые сопровождаются выделением теплоты называются экзотермическими, а те которые сопровождаются поглощением теплоты – эндотермическими.
Изменения энергии системы, при протекании в ней химической реакции при условии, что система не совершает никакой другой работы, кроме работы расширения, называется тепловым эффектом химической реакции.
где, V – объем системы , U – внутренняя энергия, называется энтальпией системы.
Энтальпия – функция состояния системы. При постоянном давлении тепловой эффект реакции равен изменению энтальпией реакции ΔH.
При экзотермической реакции ΔH 0) – энтальпия системы уменьшается.
При эндотермических реакциях ΔH>0 (Qp 0 298. Тепловой эффект зависит от температуры, поэтому в индексе указывается температура (298 К).
Уравнение процессов, в которых указаны тепловые эффекты, называются термохимическими
Чтобы энтальпию отнести к одному молю какого-либо вещества, термохимические уравнения имеют дробные коэффициенты.
В термохимических уравнениях записываются также агрегатные состояния веществ: Г-газовое, Ж-жидкое, Т-твердое, К-кристаллическое.
Энтальпия (теплота) образования – тепловой эффект образования 1 моля сложного вещества из простых веществ, устойчивых при 298 К и давлении 100 кПа. Обозначают ΔH 0 обр или ΔH 0 f.
Закон Гесса – тепловой эффект реакции зависит от природы и состояния исходных веществ и конечных продуктов, но не зависит от пути реакции, т.е. от числа и характера промежуточных стадий.
В термохимических расчетах применяют следствие из Закона Гесса:
Тепловой эффект реакции равен сумме теплот образования (ΔH 0 обр) продуктов реакции за вычетом суммы теплот образования исходных веществ с учетом коэффициентов перед формулами этих веществ в уравнениях реакции
ΔНх.р. = ∑Δ Н обр. прод . — ∑ΔН 0 обр. исх. (2)
Значения стандартных энтальпий образования ΔН 0 298 даны в таблице (приложение №1).
Пример 1. Рассчитаем стандартную энтальпию образования пропана С3Н8, если тепловой эффект реакции его сгорания
Решение: В соответствии с уравнением (2)
Подставив значение ΔН 0 х.р. и справочные данные, энтальпии простых веществ равны нулю ΔН 0 О2 = 0
ΔН 0 С3Н8 = 3(-393,51) + 4(-241,82) – 5*0 – (2043,86) = -103,85 кДж/моль
Ответ: энтальпия образования пропана относится к экзотермическим процессам.
Пример 2.Реакция горения этилового спирта выражается термохимическим уравнением:
Вычислите тепловой эффект реакции, если известно, что мольная энтальпия С2Н5ОН(ж) равна + 42,36 кДж и известны энтальпии образования С2Н5ОН (г); СО2(г); Н2О(ж) (см. табл.1).
Решение: для определения ∆Н реакции необходимо знать теплоту образования С3Н5ОН (ж). Последнюю находим из данных задачи:
ΔН С2Н5ОН (ж) = — 235,31 – 42,36 = — 277,67 кДж
Теперь вычисляем ΔН реакции, применяя следствие из закона Гесса:
ΔНх.р. = 2 (-393,51) + 3(-285,84) + 277,67 = -1366,87 кДж
Пример 3.Растворение моля безводной соды Na2CO3 в достаточно большом количестве воды сопровождается выделением 25,10 кДж теплоты, тогда как при растворении кристаллогидрата Na2CO3 * 10H2O поглощается 66,94 кДж теплоты. Вычислить теплоту гидратации Na2CO3 (энтальпию образования кристаллогидрата).
Решение: составляем термохимические уравнения соответствующих реакций:
Теперь, вычитая уравнение Б) из уравнения А), получаем ответ:
т.е. при образовании Na2CO3 * 10H2O выделяет 92,04 кДж теплоты.
Пример 4.Зная энтальпию образования воды и водяного пара (см. таб. 1), вычислить энтальпию испарения воды.
Решение: задача решается аналогично задачам в примерах 3 и 4:
Вычитая уравнение (Б) из уравнения (А) получаем ответ:
Н2О(ж) = Н2О(г); ΔН = — 241,83 + 285,84 = + 44,01 кДж,
т.е. для перевода воды в пар необходимо затратить 44,01 кДж тепла.
Пример 5.При образовании хлористого водорода по реакции
Выделяется 184,6 кДж тепла. Чему равна энтальпия образования HCl?
Решение: энтальпия образования относится к 1 моль, а по уравнению образуется 2 моль HCl.
ΔН 0 НCl = -184,6 / 2 = -92,3 кДж/моль
1/2Н2 + 1/2Cl2 = HCl; ΔН = -92,3 кДж/моль
Пример 6. Вычислить тепловой эффект горения аммиака.
Решение: на основании следствия из закона Гесса имеем
Так как энтальпии простых веществ равны 0 (ΔН 0 (N2) = 0; ΔН 0 (02) = 0)
Получаем: ΔН = 3ΔН 0 (H2О)(г) – 2ΔН 0 (NH3)
По таблице находим значение стандартных энтальпий образования
ΔН 0 (NH3) = -45,94 кДж
ΔН 0 (H2О) = -241,84 кДж
ΔН = 3 (-241,84) – 2 (-45,94) = -633,4 кДж
Пример 7.Вычислить тепловой эффект реакции горения
А) 11,2 л ацетилена
Б) 52 кг ацетилена
1. Написать термохимическое уравнение горения ацетилена
2. Написать выражение для расчета стандартного теплового эффекта реакции, пользуясь следствием из закона Гесса
Подставим в это выражение табличные значения стандартных энтальпий образования веществ:
ΔН 0 х.р. = 2(-393,5) + (-241,8) – 226,8 = -802,0 кДж
3. Из термохимического уравнения реакции видно, что количество тепла выделяется при сгорании 1 моль ацетилена (22,4 л или 26 г).
Количество тепла прямо пропорционально количеству участвующего в горении вещества. Следовательно можно составить пропорцию :
х = 52*10 3 *(-802) = — 1604 * 103 кДж
http://chemege.ru/energy-zakon-gessa/
http://poisk-ru.ru/s21134t9.html