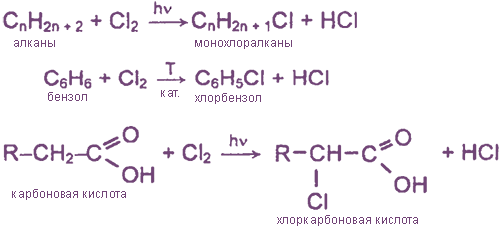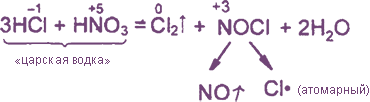Физические свойства
Cl2 при об. Т — газ желто-зеленого цвета с резким удушающим запахом, тяжелее воздуха — в 2,5 раза, малорастворим в воде (
6,5 г/л); х. р. в неполярных органических растворителях. В свободном виде встречается только в вулканических газах.
Способы получения
Основаны на процессе окисления анионов Cl —
2Cl — — 2e — = Cl2 0
Промышленный
Электролиз водных растворов хлоридов, чаще — NaCl:
Лабораторные
Окисление конц. HCI различными окислителями:
Химические свойства
Хлор — очень сильный окислитель. Окисляет металлы, неметаллы и сложные вещества, превращаясь при этом в очень устойчивые анионы Cl — :
Реакции с металлами
Активные металлы в атмосфере сухого газообразного хлора воспламеняются и сгорают; при этом образуются хлориды металлов.
Малоактивные металлы легче окисляются влажным хлором или его водными растворами:
Реакции с неметаллами
Хлор непосредственно не взаимодействует только с O2, N2, С. С остальными неметаллами реакции протекают при различных условиях.
Образуются галогениды неметаллов. Наиболее важной является реакция взаимодействия с водородом.
Вытеснение свободных неметаллов (Вr2, I2, N2, S) из их соединений
Диспропорционирование хлора в воде и водных растворах щелочей
В результате самоокисления-самовосстановления одни атомы хлора превращаются в анионы Cl — , а другие в положительной степени окисления входят в состав анионов ClO — или ClO3 — .
Cl2 + Н2O = HCl + НClO хлорноватистая к-та
Эти реакции имеют важное значение, поскольку приводят к получению кислородных соединений хлора:
КClO3 и Са(ClO)2 — гипохлориты; КClO3 — хлорат калия (бертолетова соль).
Взаимодействие хлора с органическими веществами
а) замещение атомов водорода в молекулах ОВ
б) присоединение молекул Cl2 по месту разрыва кратных углерод-углеродных связей
Хлороводород и соляная кислота
Газообразный хлороводород
Физические и химические свойства
HCl — хлорид водорода. При об. Т — бесцв. газ с резким запахом, достаточно легко сжижается (т. пл. -114°С, т. кип. -85°С). Безводный НСl и в газообразном, и в жидком состояниях неэлектропроводен, химически инертен по отношению к металлам, оксидам и гидроксидам металлов, а также ко многим другим веществам. Это означает, что в отсутствие воды хлороводород не проявляет кислотных свойств. Только при очень высокой Т газообразный HCl реагирует с металлами, причем даже такими малоактивными, как Сu и Аg.
Восстановительные свойства хпорид-аниона в HCl также проявляются в незначительной степени: он окисляется фтором при об. Т, а также при высокой Т (600°С) в присутствии катализаторов обратимо реагирует с кислородом:
Газообразный HCl широко используется в органическом синтезе (реакции гидрохлорирования).
Способы получения
1. Синтез из простых веществ:
2. Образуется как побочный продукт при хлорировании УВ:
R-H + Cl2 = R-Cl + HCl
3. В лаборатории получают действием конц. H2SO4 на хлориды:
H2SО4(конц.) + NaCl = 2HCl↑ + NaHSО4 (при слабом нагревании)
H2SО4(конц.) + 2NaCl = 2HCl↑ + Na2SО4 (при очень сильном нагревании)
Водный раствор HCl — сильная кислота (хлороводородная, или соляная)
HCl очень хорошо растворяется в воде: при об. Т в 1 л Н2O растворяется
450 л газа (растворение сопровождается выделением значительного количества тепла). Насыщенный раствор имеет массовую долю HCl, равную 36-37 %. Такой раствор имеет очень резкий, удушающий запах.
Молекулы HCl в воде практически полностью распадаются на ионы, т. е. водный раствор HCl является сильной кислотой.
Химические свойства соляной кислоты
1. Растворенный в воде HCl проявляет все общие свойства кислот, обусловленные присутствием ионов Н +
а) с металлами (до Н):
б) с основными и амфотерными оксидами:
в) с основаниями и амфотерными гидроксидами:
г) с солями более слабых кислот:
Реакции с сильными окислителями F2, MnO2, KMnO4, KClO3, K2Cr2O7. Анион Cl — окисляется до свободного галогена:
2Cl — — 2e — = Cl2 0
Уравнения реакция см. «Получение хлора». Особое значение имеет ОВР между соляной и азотной кислотами:
Реакции с органическими соединениями
а) с аминами (как органическими основаниями)
б) с аминокислотами (как амфотерными соедимнеиями)
Оксиды и оксокислоты хлора
Кислородсодержащие соединения хлора — чрезвычайно неустойчивые вещества, так как включают атомы Cl в нестабильных положительных с. о. Тем не менее некоторые из них имеют важное практическое значение.
Хлор реагирует с раствором вещества напишите уравнение реакции
Хлор взаимодействует с раствором вещества, формула которого:
А NaCl
Б NaBr
В HF
Г NaF
Информация
Посетители, находящиеся в группе Гости, не могут оставлять комментарии к данной публикации.
Хлор взаимодействует с раствором вещества, формула которого : А NaCl Б NaBr В HF Г NaF?
Химия | 5 — 9 классы
Хлор взаимодействует с раствором вещества, формула которого : А NaCl Б NaBr В HF Г NaF.
Б потому что бром не сильнее хлора.
Помогите?
Задание : Составить структурные и электронные формулы веществ : N2, NaCl, SiH4, O2, LiF, CH4, H2, HCL, NaF.
В ряду NaH — NaF — NaCl — NaBr длинна связи : 1)увеличивается 2)уменьшается 3)не изменяется 4)меняется периодически?
В ряду NaH — NaF — NaCl — NaBr длинна связи : 1)увеличивается 2)уменьшается 3)не изменяется 4)меняется периодически.
С какими веществами реагирует хлор : NaF, NaCI , NaBr, NAI ?
С какими веществами реагирует хлор : NaF, NaCI , NaBr, NAI ?
1. Выберите формулы веществ, в которых хлор имеет степень окисления – 1 :HCl, NaBr, Cl2, KCl, HBr, Br2?
1. Выберите формулы веществ, в которых хлор имеет степень окисления – 1 :
HCl, NaBr, Cl2, KCl, HBr, Br2.
Расположите в ряд по возрастанию степени ионности связи следушие соединения а)NaCl, Nal, NaBr, NaF б)K2S, K2O, KF, KCl?
Расположите в ряд по возрастанию степени ионности связи следушие соединения а)NaCl, Nal, NaBr, NaF б)K2S, K2O, KF, KCl.
СРОЧНО, ПОЖАЛУЙСТА?
В ряду NaH — NaF — NaCl — NaBr длина связи?
С РАСТВОРОМ ГИДРОКСИДА КАЛИЯ ВЗАИМОДЕЙСТВУЕТ ВЕЩЕСТВО, ФОРМУЛА КОТОРОГО FeO CaO CO2?
С РАСТВОРОМ ГИДРОКСИДА КАЛИЯ ВЗАИМОДЕЙСТВУЕТ ВЕЩЕСТВО, ФОРМУЛА КОТОРОГО FeO CaO CO2.
При взаимодействии гидроксида цинка с избытком раствора гидроксида натрия образуется вещество, формула которого ?
При взаимодействии гидроксида цинка с избытком раствора гидроксида натрия образуется вещество, формула которого .
В каком ряду приведены формулы веществ с полярной ковалентной связью 1)H2, Br2, O2 2) HCl, HBr, H2S 3) NaCl, NaF, NaBr 4) Na, H2O, CuO?
В каком ряду приведены формулы веществ с полярной ковалентной связью 1)H2, Br2, O2 2) HCl, HBr, H2S 3) NaCl, NaF, NaBr 4) Na, H2O, CuO.
Формула вещества в котором степень окисления хлора равна нулю?
Формула вещества в котором степень окисления хлора равна нулю.
Вы находитесь на странице вопроса Хлор взаимодействует с раствором вещества, формула которого : А NaCl Б NaBr В HF Г NaF? из категории Химия. Уровень сложности вопроса рассчитан на учащихся 5 — 9 классов. На странице можно узнать правильный ответ, сверить его со своим вариантом и обсудить возможные версии с другими пользователями сайта посредством обратной связи. Если ответ вызывает сомнения или покажется вам неполным, для проверки найдите ответы на аналогичные вопросы по теме в этой же категории, или создайте новый вопрос, используя ключевые слова: введите вопрос в поисковую строку, нажав кнопку в верхней части страницы.
CaCl₂ + Na₂CO₃ = CaCO₃↓ + 2NaCl CaCO₃ (t°C) = CaO + CO₂↑ CaO + 3C (t°C) = CaC₂ + CO↑ CaC₂ + 2H₂O = Ca(OH)₂ + C₂H₂↑.
Это явление называется химическим.
1)Mg — Магий, Na — натрий, Si — кремний, P — фосфор, Cu — медь, Ag — серебро, Hg — ртуть, N — азот. 2) Медь — Cu, Калий — K, Цинк — Zn, Ртуть — Hg, Золото — Au, Магний — Mg, Углерод — C, Сера — S, Хлор — Cl, Свинец — Pb.
Соль это неорганическое вещество.
1. 1) В (Водород — 1) 2) А (Сера — 32) 3) Б (Кислород — 16) 4) Г (Углерод — 12).
1. 1)водород = B. 1 2)сера = А. 32 3)кислород = Б. 16 4)углерод = Г. 12.
Na2O + H2S — > Na2S + H2O Al2O3 + 3H2S — > Al2S3 + 3H2O Mg + H2S — > MgS + H2 Na2CO3 + H2S — > Na2S + CO2 + H2O Pb(NO3)2 + Na2S — > PbS + 2NaNO3 Na2S + CuCl2 — > CuS + 2NaCl 2H2S + 3O2 — > 2H2O + 2SO2 2H2S + O2 — > 2H2O + 2S H2S + I2 — > S + 2HI.
H2O Кислород II HF Фтор I NH3 Азот III H2S Сера II CH4 Углерод IV.
А)4Al + 3O2 = 2Al2O3 — реакция соединения б)MnO2 + 2H2 = Mn + 2H2O — реакция замещения в)H2O2 = H2 + O2 — реакция разложения г)3HNO3 + Fe(OH)3 = Fe(NO3)3 + 3H2O — реакция обмена.
http://znanija.org/himiya/1352221.html
http://himia.my-dict.ru/q/612940_hlor-vzaimodejstvuet-s-rastvorom-vesestva-formula/