Хлорид аммония с кислородом уравнение
Для выполнения задания используйте следующий перечень веществ: хлорид аммония, кислород, сульфид бария, гидроксид калия, оксид бария. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна окислительно восстановительная реакция, и запишите уравнение этой реакции. Составьте электронный баланс, укажите окислитель и восстановитель.
Для выполнения задания используйте следующий перечень веществ: хлорид аммония, кислород, сульфид бария, гидроксид калия, оксид бария. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Первый вариант ответа:
Второй вариант ответа:
Запишем уравнение реакции:
Составим электронный баланс:
Сера в степени окисления −2 является восстановителем, а кислород в степени окисления 0 — окислителем.
| Критерии оценивания выполнения задания | Баллы |
|---|---|
| Ответ правильный и полный, содержит следующие элементы: — выбраны вещества, и записано уравнение окислительно-восстановительной реакции; Соли аммония: получение и химические свойстваСоли аммонияСоли аммония – это соли, состоящие из катиона аммония и аниона кислотного остатка . Способы получения солей аммония1. Соли аммония можно получить взаимодействием аммиака с кислотами . Реакции подробно описаны выше. 2. Соли аммония также получают в обменных реакциях между солями аммония и другими солями. Например , хлорид аммония реагирует с нитратом серебра: 3. Средние соли аммония можно получить из кислых солей аммония . При добавлении аммиака кислая соль переходит в среднюю. Например , гидрокарбонат аммония реагирует с аммиаком с образованием карбоната аммония: Химические свойства солей аммония1. Все соли аммония – сильные электролиты , почти полностью диссоциируют на ионы в водных растворах: NH4Cl ⇄ NH4 + + Cl – 2. Соли аммония проявляют свойства обычных растворимых солей –вступают в реакции обмена с щелочами, кислотами и растворимыми солями , если в продуктах образуется газ, осадок или образуется слабый электролит. Например , карбонат аммония реагирует с соляной кислотой. При этом выделяется углекислый газ: Соли аммония реагируют с щелочами с образованием аммиака. Например , хлорид аммония реагирует с гидроксидом калия: NH4Cl + KOH → KCl + NH3 + H2O Взаимодействие с щелочами — качественная реакция на ионы аммония. Выделяющийся аммиак можно обнаружить по характерному резкому запаху и посинению лакмусовой бумажки. 3. Соли аммония подвергаются гидролизу по катиону , т.к. гидроксид аммония — слабое основание: 4. При нагревании соли аммония разлагаются . При этом если соль не содержит анион-окислителя, то разложение проходит без изменения степени окисления атома азота. Так разлагаются хлорид, карбонат, сульфат, сульфид и фосфат аммония: Если соль содержит анион-окислитель, то разложение сопровождается изменением степени окисления атома азота иона аммония. Так протекает разложение нитрата, нитрита и дихромата аммония: При температуре 250 – 300°C: При температуре выше 300°C: Разложение бихромата аммония («вулканчик»). Оранжевые кристаллы дихромата аммония под действием горящей лучинки бурно реагируют. Дихромат аммония – особенная соль, в ее составе – окислитель и восстановитель. Поэтому «внутри» этой соли может пройти окислительно-восстановительная реакция (внутримолекулярная ОВР): Окислитель – хром (VI) превращается в хром (III), образуется зеленый оксид хрома. Восстановитель – азот, входящий в состав иона аммония, превращается в газообразный азот. Итак, дихромат аммония превращается в зеленый оксид хрома, газообразный азот и воду. Реакция начинается от горящей лучинки, но не прекращается, если лучинку убрать, а становится еще интенсивней, так как в процессе реакции выделяется теплота, и, начавшись от лучинки, процесс лавинообразно развивается. Оксид хрома (III) – очень твердое, тугоплавкое вещество зеленого цвета, его используют как абразив. Температура плавления – почти 2300 градусов. Оксид хрома – очень устойчивое вещество, не растворяется даже в кислотах. Благодаря устойчивости и интенсивной окраске окись хрома используется при изготовлении масляных красок. Видеоопыт разложения дихромата аммония можно посмотреть здесь. Вариант 4Вопросы:1. Напишите уравнения реакций: а) азота с кислородом (укажите условия протекания, обозначьте степени окисления элементов и укажите окислитель и восстановитель); б) аммиака с хлороводородом; в) раствора сульфата аммония с раствором гидроксида бария (в молекулярной и ионной формах). 2. В трех пронумерованных пробирках находятся кристаллические вещества: хлорид аммония, сульфат аммония и хлорид натрия. Как их можно распознать? Напишите уравнения соответствующих реакций. 3. Изобразите молекулярную, электронную и структурную формулы аммиака. Перечислите физические свойства аммиака. Ответы и решения:2. Данные вещества можно распознать при помощи растворов источники: http://chemege.ru/soli-ammoniya/ http://5terka.com/node/11421 |
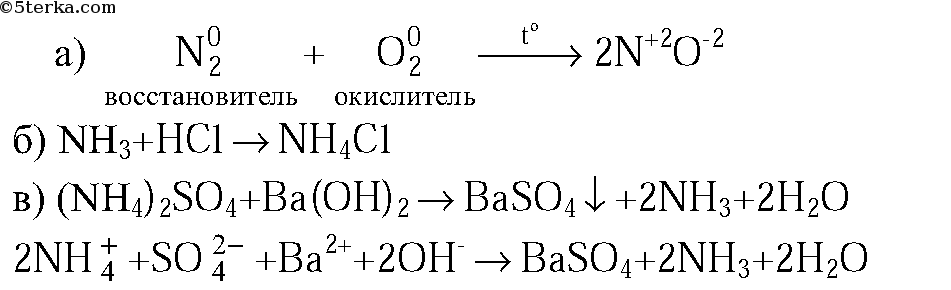
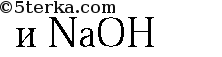
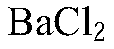


 Решебник по химии за 9 класс (А.М.Радецкий, 2011 год),
Решебник по химии за 9 класс (А.М.Радецкий, 2011 год),