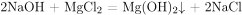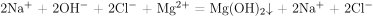Хлорид магния: способы получения и химические свойства
Хлорид магния MgCl — соль щелочного металла магния и хлороводородной кислоты. Белый, плавится без разложения. Хорошо растворяется в воде (слабый гидролиз по катиону).
Относительная молекулярная масса Mr = 95,21; относительная плотность для тв. и ж. состояния d = 2,32; tпл = 714º C; tкип = 1370º C;
Способ получения
1. Хлорид магния можно получить путем взаимодействия магния и разбавленной хлороводородной кислоты, образуются хлорид магния и газ водород:
Mg + 2HCl = MgCl2 + H2↑
2. При комнатной температуре, в результате взаимодействия магния и влажного хлора, образуется хлорид магния:
3. Разбавленная хлороводородная кислота реагирует с гидроксидом магния . Взаимодействие хлороводородной кислоты с гидроксидом магния приводит к образованию хлорида магния и воды:
4. Карбонат лития взаимодействует с разбавленной соляной кислотой , образуя хлорид магния, углекислый газ и воду:
5. Оксид магния взаимодействует с разбавленной соляной кислотой , образуя хлорид магния и воду:
MgO + 2HCl = MgCl2 + H2O
6. В результате взаимодействия оксида магния , углерода и хлора при 800 — 1000º С образуется хлорид магния и угарный газ:
MgO + C + Cl2 = MgCl2 + CO
Качественная реакция
Качественная реакция на хлорид магния — взаимодействие его с нитратом серебра, в результате реакции происходит образование белого творожного осадка:
1. При взаимодействии с нитратом серебра , хлорид магния образует нитрат магния и осадок хлорид серебра:
Химические свойства
1. Хлорид магния вступает в реакцию со многими сложными веществами :
1.1. Хлорид магния вступает в реакции с основаниями :
Хлорид магния взаимодействует с разбавленным раствором гидроксида натрия . При этом образуются гидроксид магния и хлорид натрия:
MgCl2 + 2NaOH = Mg(OH)2↓ + 2NaCl
1.2. Насыщенный хлорид магния реагирует с концентрированным и горячим гидратом аммиака, образуя гидроксид магния и хлорид аммония :
Школе NET
Register
Do you already have an account? Login
Login
Don’t you have an account yet? Register
Newsletter
Submit to our newsletter to receive exclusive stories delivered to you inbox!
- Главная
- Вопросы & Ответы
- Вопрос 9393288
Зачетный Опарыш
Составьте молекулярные, полные и сокращённые ионные уравнения реакций между растворами следующих веществ
1. сульфат натрия и хлорид бария
2. нитрат магния и гидроксид натрия
3. хлорид меди ( II ) и нитрат серебра
4. силикат калия и соляная кислота
5. фосфат натрия и хлорид магния
6. сульфат алюминия и гидроксид калия
Лучший ответ:
Энджелл
Na2SO4 BaCl2 = 2NaCl BaSO4
2Na⁺ SO4²⁻ Ba²⁺ 2Cl⁻ = 2Na⁺ 2Cl⁻ BaSO4
SO4²⁻ Ba²⁺ = BaSO4
Mg(NO3)2 2NaOH = Mg(OH)2 2NaNO3
Mg²⁺ 2NO3⁻ 2Na⁺ 2OH⁻ = Mg(OH)2 2Na⁺ 2NO3⁻
Mg²⁺ 2OH⁻ = Mg(OH)2
CuCl2 2AgNO3 = 2AgCl Cu(NO3)2
Cu²⁺ 2Cl⁻ 2Ag⁺ 2NO3⁻ = 2AgCl Cu²⁺ 2NO3⁻
2Cl⁻ 2Ag⁺ = 2AgCl
Cl⁻ Ag⁺ = AgCl
K2SiO3 2HCl = 2KCl H2SiO3
2K⁺ SiO3²⁻ 2H⁺ 2Cl⁻ = 2K⁺ 2Cl⁻ H2SiO3
SiO3²⁻ 2H⁺ = H2SiO3
2Na3PO4 3MgCl2 = Mg3(PO4)2 6NaCl
6Na⁺ 2PO4³⁻ 3Mg²⁺ 6Cl⁻ = Mg3(PO4)2 6Na⁺ 6Cl⁻
2PO4³⁻ 3Mg²⁺ = Mg3(PO4)2
Al2(SO4)3 6KOH = 2Al(OH)3 3K2SO4
2Al³⁺ 3SO4²⁻ 6K⁺ 6OH⁻ = 2Al(OH)3 6K⁺ 3SO4²⁻
2Al³⁺ 6OH⁻ = 2Al(OH)3
Al³⁺ 3OH⁻ = Al(OH)3
Vuz-24.ru
Материалы в помощь студентам и научным работникам
Задание с ответами: химия. ЕГЭ — 2018
Для выполнения задания используйте следующий перечень веществ: бромат натрия, фтор, гидроксид натрия, хлорид магния, нитрат калия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции.
Сведения для решения
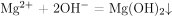
http://shkolenet.ru/QA/9393288/
http://vuz-24.ru/task/task-6032.php