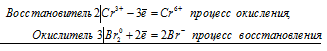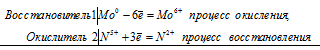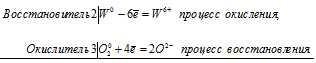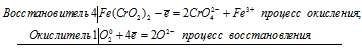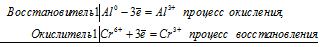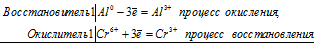Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Соли хрома: химические свойства и получениеСоли хромаСоли хрома (II)Все соли хрома (II) – сильные восстановители. В растворах окисляются даже кислородом воздуха. Например , хлорид хрома (II) окисляется кислородом в растворе в присутствии щелочи до соединений хрома (III): Концентрированные кислоты-окислители (азотная и серная) также окисляют соединения хрома (II): Соли хрома (III)Хром с валентностью III образует два типа солей:
1. Соли хрома (III) проявляют слабые восстановительные свойства . окисляются под действием сильных окислителей в щелочной среде. Например , бром в присутствии гидроксида калия окисляет хлорид хрома (III): 2CrCl3 + 3Br2 + 16KOH → 2K2CrO4 + 6KBr + 6KCl + 8H2O или сульфат хрома (III): Пероксид водорода в присутствии щелочи также окисляет соли хрома (III): Даже перманганат калия в щелочной среде окисляет соли хрома (III): Комплексные соли хрома (III) также окисляются сильными окислителями в присутствии щелочей. Например , гексагидроксохроматы окисляются бромом в щелочи: Оксид свинца (IV) также окисляет хромиты: 2. Соли хрома (III) в щелочной среде образуют гидроксид хрома (III), который сразу растворяется, образуя гидроксокомплекс. 2CrCl3 + 6KOH → 2Cr(OH)3 + 6KCl 3. Более активные металлы вытесняют хром (III) из солей. Например , цинк реагирует с хлоридом хрома (III): Гидролиз солей хрома (III)Растворимые соли хрома (III) и сильных кислот гидролизуются по катиону. Гидролиз протекает ступенчато и обратимо, т.е. чуть-чуть: I ступень: Cr 3+ + H2O = CrOH 2+ + H + II ступень: CrOH 2+ + H2O = Cr(OH )2 + + H + Однако сульфиды, сульфиты, карбонаты хрома (III) и их кислые соли гидролизуются необратимо, полностью, т.е. в водном растворе не существуют, а разлагаются водой в момент образования. Например , при сливании растворов солей хрома (III) и сульфита, гидросульфита, карбоната или сульфида натрия протекает взаимный гидролиз: Более подробно про гидролиз можно прочитать в соответствующей статье. ХромитыСоли, в которых хром (III) входит в состав кислотного остатка (хромиты) — образуются из оксида хрома (III) при сплавлении с щелочами и основными оксидами: Для понимания свойств хромитов их удобно мысленно разделить на два отдельных вещества. Например , хромит натрия мы поделим мысленно на два вещества: оксид хрома (III) и оксид натрия. NaСrO2 разделяем на Na2O и Cr2O3 При этом очевидно, что хромиты реагируют с кислотами. При недостатке кислоты образуется гидроксид хрома (III): NaCrO2 + HCl (недостаток) + H2O → Cr(OH)3 + NaCl В избытке кислоты гидроксид хрома (III) не образуется: NaCrO2 + 4HCl (избыток) → CrCl3 + NaCl + 2H2O NaCrO2 + 4HCl → CrCl3 + NaCl + 2H2O Под действием избытка воды хромиты гидролизуются: Соли хрома (VI)Оксиду хрома ( VI ) соответствуют две кислоты – хромовая Н2 CrO 4 и дихромовая Н2 Cr 2 O 7. Поэтому хром в степени окисления +6 образует два типа солей: хроматы и дихроматы. Например , хромат калия K2CrO4 и дихромат калия K2Cr2O7. 1. Различить эти соли довольно легко: хроматы желтые, а дихроматы оранжевые. Хроматы устойчивы в щелочной среде, а дихроматы устойчивы в кислой среде. При добавлении к хроматам кислот они переходят в дихроматы. Например , хромат калия взаимодействует с серной кислотой и разбавленной соляной кислотой с образованием дихромата калия: И наоборот: дихроматы реагируют с щелочами с образованием хроматов. Например , дихромат калия взаимодействует с гидроксидом калия с образованием хромата калия: Видеоопыт взаимных переходов хроматов и дихроматов при добавлении кислоты или щелочи можно посмотреть здесь. 2. Хроматы и дихроматы проявляют сильные окислительные свойства. При взаимодействии с восстановителями они восстанавливаются до соединений хрома (III). В нейтральной среде хроматы и дихроматы восстанавливаются до гидроксида хрома (III). Например , дихромат калия реагирует с сульфитом натрия в нейтральной среде: Хромат калия окисляет сульфид аммония: При взаимодействии с восстановителями в щелочной среде хроматы и дихроматы образуют комплексные соли. Например , хромат калия окисляет гидросульфид аммония в щелочной среде: Хромат натрия окисляет сернистый газ: Хромат натрия окисляет сульфид натрия: При взаимодействии с восстановителями в кислой среде хроматы и дихроматы образуют соли хрома (III). Например , дихромат калия окисляет сероводород в присутствии серной кислоты: Дихромат калия окисляет йодид калия, фосфид кальция, соединения железа (II), сернистый газ, концентрированную соляную кислоту: Химические свойства хромаЗадание 411 Уравнение реакции окисления-восстановления хромата калия бромом2Cr 3+ + 3Br2 0 = 2Cr 6+ + 6Br — Начальная, зелёная окраска обусловливается хромит-ионами CrO2 — , а конечная, жёлтая – хромат-ионами CrO4 2- . Задание 412 Уравнения реакций растворения металлов в кислоте и щёлочиа) Растворение молибдена в азотной кислоте б) Растворение вольфрама в щелочи в присутствии кислорода 2W 0 + 3O2 0 = 2W 6+ + 6O 2- Задание 413 Уравнение реакции сплавления хромита железа с карбонатом натрия Задание 414 Уравнение реакции серной кислоты с дихроматом калия Al 0 + Cr 6+ = Al 3+ + Cr 3+ Задание 415 Уравнениие реакции получения хрома методом алюминотермииа) Получение хрома методом алюминотермии Al 0 + Cr 6+ = Al 3+ + Cr 3+ б) Получение вольфрама методом алюминотермии источники: http://chemege.ru/soli-chroma/ http://buzani.ru/zadachi/khimiya-shimanovich/993-svojstva-khroma-zadaniya-412-415 |