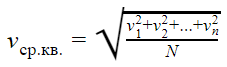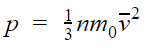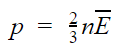Идеальный газ основное уравнение мкт газов 10 класс
Идеальный газ — это просто!
Идеальный газ
Идеальный газ — это физическая модель газа, взаимодействие между молекулами которого пренебрежительно мало.
Понятие «идеальный газ» вводится для математического описания поведения газов.
Реальные разреженные газы ведут себя как идеальный газ!
Свойства идеального газа:
— взаимодействие между молекулами пренебрежительно мало
— расстояние между молекулами много больше размеров молекул
— молекулы — это упругие шары
— отталкивание молекул возможно только при соударении
— движение молекул — по законам Ньютона
— давление газа на стенки сосуда — за счет ударов молекул газа
Скорость молекул газа
В теории газов скорость молекул принято определять через среднее значение квадрата скорости молекул.
Хотя скорости различных молекул сильно отличаются друг от друга, но среднее значение квадрата скорости молекул есть величина постоянная.
Формула для расчета среднего значения квадрата скорости молекул газа:
где
n — число молекул в газе
v — модули скоростей отдельных молекул в газе
В теории газов часто используется понятие кинетической энергии молекул.
Используя среднее значение квадрата скорости молекул, получаем формулу для определения средней кинетической энергии молекул:
Основное уравнение МКТ газа
Основное уравнение МКТ связывает микропараметры частиц (массу молекулы, среднюю кинетическую энергию молекул, средний квадрат скорости молекул) с макропараметрами газа (р — давление, V — объем, Т — температура).
Давление газа на стенки сосуда пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы.
Ниже приведены различные выражения для основного уравнения МКТ:
где
р — давление газа на стенки сосуда(Па)
n — концентрация молекул, т.е. число молекул в единице объема ( 1/м 3 )


ρ — плотность газа (кг/м 3 )

Давление идеального газа на стенки сосуда зависит от концентрации молекул и пропорционально средней кинетической энергии молекул.
Дополнительные расчетные формулы по теме
Формула для расчета концентрации молекул:
где
N — число молекул газа
V — объем газа (м 3 )
Формула для расчета плотности газа:
где
mo — масса молекулы (кг)
n — концентрация молекул (1/м 3 )
Молекулярная физика. Термодинамика — Класс!ная физика
Урок физики в 10 классе «ОСНОВНОЕ УРАВНЕНИЕ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ »
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
ТЕМА «ОСНОВНОЕ УРАВНЕНИЕ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ » 10 КЛАСС
Обучающие: познакомить с понятием идеального газа, вывести основное уравнение молекулярно-кинетической теории газов.
· развивать способности анализировать увиденное, логическое мышление и творческое воображение учащихся;
· учить устанавливать причинно-следственные связи в изучаемых явлениях, формулировать эмпирические закономерности.
Воспитывающие : воспитывать ответственное отношение к учебе, положительное отношение к предмету физики.
· воздушный насос, вакуумная тарелка, стеклянный колокол, воздушный шарик
· карточки с тестом
I . Повторение пройденного. Беседа с учащимися с использованием презентации (Приложение 1)
- Каковы основные положения молекулярно-кинетической теории строения вещества? (слайд 2)
- Докажите, что все вещества состоят из молекул, между которыми есть промежутки? (слайд 3)
- В чем суть броуновского движения? Доказательством каких положений является броуновское движение? (слайд 4)
- Что такое диффузия? Доказательством каких положений является броуновское движение? (слайд 5)
- Зависит ли скорость диффузии от температуры? (слайд 6)
- О чем говорят опыты, показанные на слайде № 7
- Каковы размеры молекул? (слайд 8)
- Опишите словами модель взаимодействия между молекулами или атомами твердого тела. (слайд 9)
- В каком агрегатном состоянии находится вещество, показанное на слайдах № 10,11,12? Укажите особенности расположения и движения молекул в различных агрегатных состояниях.
II . Изучение нового материала
Итак, мы знаем, что частицы в газах, в отличие от жидкостей и твердых тел, располагаются друг относительно друга на расстояниях, существенно превышающих их собственные размеры. В этом случае взаимодействие между молекулами пренебрежимо мало и кинетическая энергия молекул много больше энергии межмолекулярного взаимодействия. Для выяснения наиболее общих свойств, присущих всем газам, используют упрощенную модель газа — идеальный газ.
Идеальный газ – это газ, у которого взаимодействие между молекулами пренебрежимо мало (слайд13) (записываем в тетрадь)
Основные отличия идеального газа от реального газа:
1. Частицы идеального газа — сферические тела очень малых размеров, практически материальные точки.
2. Между частицами отсутствуют силы межмолекулярного взаимодействия.
3. Соударения частиц являются абсолютно упругими.
Реальные разреженные газы действительно ведут себя подобно идеальному газу. Воспользуемся моделью идеального газа для объяснения происхождения давления газа.
Вспомним опыт из 7 класса (слайд14)
Почему при откачивании воздуха из-под колокола воздушный шарик раздувается?
(Это значит, что газ внутри шарика оказывает давление, и когда внешнее давление при откачивании уменьшается, шар благодаря внутреннему давлению воздуха начинает раздуваться?
Что же такое давление газа? (слайд15)
(Давление газа — это результат ударов молекул газа о стенки сосуда)
Сегодня мы с вами попытаемся ответить, от чего зависит давление газа? (Слайд 16)
Даю возможность учащимся сделать предположения, от чего может зависеть давление газа.
Выведем основное уравнение молекулярно-кинетической теории газов (слайд 17)
Пусть в некотором объеме есть молекулы, масса каждой mo , их число равно N , и движутся они со скоростью v (очевидно, что скорости у всех молекул различны, однако среднее значение модуля скорости v вполне определенное)
Учитель делает рисунок на доске, учащиеся в тетрадях
При каждом ударе молекулы действуют на стенку сосуда с некоторой силой. Складываясь друг с другом, силы ударов отдельных частиц образуют некоторую силу давления, постоянно действующую на стенку, а значит и давление.
От чего же зависит давление газа?
Во-первых , от массы: чем больше масса молекулы, тем сильнее удар, значит здесь прямая пропорциональная зависимость давления от массы
1) р 
Во-вторых , от скорости: чем быстрее движутся молекулы, тем сильнее будут удары, а значит и давление.
2) р 
В-третьих, есть еще одна зависимость от скорости: чем быстрее движутся молекулы, тем чаще удары, а значит и давление.
3) р 
В-четвертых , давление газа зависит от числа молекул в данном сосуде, а точнее от концентрации n .
Концентрация – физическая величина, равная числу молекул, содержащихся в единице объема ( n = N / V )
( определение концентрации и единицы измерения записываем в тетрадь )
4) р 
В результате получаем: давление газа прямо пропорционально концентрации частиц, массе частицы и квадрату скорости частицы
Это и есть основное уравнение молекулярно-кинетической теории идеального газа. В этом уравнении коэффициент 1/3 означает, что в трехмерном пространстве только треть молекул участвует в движении в определенном направлении (по оси х, например).
Мы получили основное уравнение МКТ идеального газа из общих соображений, но его можно строго вывести, опираясь на законы классической механики ( § 63 , Мякишев Г.Я.)
Это уравнение можно записать по-другому, если умножить и разделить правую часть уравнения на 2.
Давление идеального газа пропорционально произведению концентрации молекул и средней кинетической энергии поступательного движения молекул
III . Закрепление изученного материала. Выполнение тестов учащимися.
Цель заданий: определить степень усвоения нового материала
1. Давление газа на стенку сосуда обусловлено
А. притяжением молекул друг к другу
Б. столкновениями молекул со стенками сосудов
В. столкновением молекул газа между собой
Г. проникновением молекул сквозь стенки сосуда
2. Как изменилось давление идеального газа, если в данном объеме скорость каждой молекулы газа увеличилась в 2 раза, а концентрация молекул осталась без изменения?
А. увеличилось в 2 раза
Б. увеличилось в 4 раза
В. уменьшилось в 2 раза
Г. уменьшилось в 4 раза
3. При повышении температуры идеального газа в запаянном сосуде его давление увеличивается. Это объясняется тем, что с ростом температуры.
А.увеличиваются размеры молекул газа
Б. увеличивается энергия движения молекул газа
В. увеличивается потенциальная энергия молекул газа
Г. увеличивается хаотичность движения молекул газа
4. Как изменится концентрация молекул газа при уменьшении объема сосуда в 2 раза?
А.увеличится в 2 раза
Б. уменьшится в 2 раза
Г. уменьшится в 4 раза
5. При уменьшении температуры средняя кинетическая энергия молекул
Г. иногда увеличится, иногда уменьшится
6. Какое утверждение неправильно?
При неизменных условиях
А. давление газа постоянно
Б. скорости всех молекул одинаковы
В. внутренняя энергия газа постоянна
Г. температура газа постоянна
7. В сосуде водород. Как изменится давление газа, если водород заменить кислородом так, что количество молекул и температура останутся неизменными?
А.увеличится в 4 раза
Б. уменьшится в 16 раз
Г. увеличится в 16 раз
IV . Проверка выполненных тестов
Правильные ответы: 1 — Б, 2 – Б, 3 – Б, 4 – А, 5 – Б, 6 – Б , 7 — Г
V . Решение задачи
В ампуле содержится водород (Н 2 ). Определите давление газа, если его концентрация равна 2 · 10 22 м -3 , а средняя квадратичная скорость движения молекул водорода 500 м/с.
VI . Задание на дом.
§ 61, § 63, Физика 10 класс Г.Я. Мякишев, Б.Б Буховцев, записи в тетради, упр. 11 (задачи 8,9)
VII . Подведение итогов урока.
1. Физика. 10 класс: учебник для общеобразовательных учреждений: базовый и профильный уровни /Г.Я Мякишев, Б.Б.Буховцев, Н.Н. Сотский; — М.: Просвещение, 2009.
2. Физика. Тесты. 10-11 классы: учебно-методическое пособие / Н.К. Гладышева, И.И. Нурминский, А.И. Нурминский и др. – М.: Дрофа, 2005.
Идеальный газ
О чем эта статья:
Газ: агрегатное состояние
У веществ есть три агрегатных состояния — твердое, жидкое и газообразное.
Их характеристики — в таблице:
Агрегатные состояния
Свойства
Расположение молекул
Расстояние между молекулами
Движение молекулы
Твердое
сохраняет форму и объем
в кристаллической решетке
соотносится с размером молекул
колеблется около положения равновесия в кристаллической решетке
Жидкое
сохраняет объем и текучесть
близко друг к другу
молекулы малоподвижны, при нагревании скорость движения увеличивается
Газообразное
занимает весь предоставленный объем
больше размеров молекул
хаотичное и непрерывное
В жизни мы встречаем вещества в газообразном состоянии, когда чувствуем запахи. Запах очень легко распространяется, потому что газ не имеет ни формы, ни объема (занимает весь предоставленный объем) и состоит из хаотично движущихся молекул, расстояние между которыми больше, чем размеры молекул.
Агрегатных состояний точно три?
На самом деле есть еще четвертое — плазма. Звучит как что-то из научной фантастики, но это просто ионизированный газ — газ, в котором, помимо нейтральных частиц, есть еще и заряженные. Ионизаторы воздуха как раз строятся на принципе перехода из газообразного вещества в плазму.
Модель идеального газа
В физике есть такое понятие, как модель. Модель — это что-то идеализированное, она нужна в случаях, когда можно пренебречь некоторыми параметрами объекта или процесса.
Идеальный газ — это модель реального газа. Молекулы идеального газа представляют собой материальные точки, которые не взаимодействуют друг с другом на расстоянии, но взаимодействуют при столкновениях друг с другом или со стенками сосуда. При работе с идеальным газом можно пренебречь потенциальной энергией молекул (но не кинетической).
В повседневной жизни идеальный газ, конечно, не встречается. Но реальный газ может вести себя почти как идеальный. Такое случается, если среднее расстояние между молекулами во много раз больше их размеров, то есть если газ очень разреженный.
Свойства идеального газа
Расстояние между молекулами значительно больше размеров молекул.
Молекулы газа очень малы и представляют собой упругие шары.
Силы притяжения между молекулами пренебрежимо малы.
Молекулы взаимодействуют только при соударениях.
Молекулы движутся хаотично.
Молекулы движутся по законам Ньютона.
Среднеквадратичная скорость
Потенциальной энергией молекул газа пренебречь можно, а вот кинетической — никак нельзя. Потому что кинетическая энергия — это энергия движения, а мы не можем пренебрегать скоростью движения молекул.
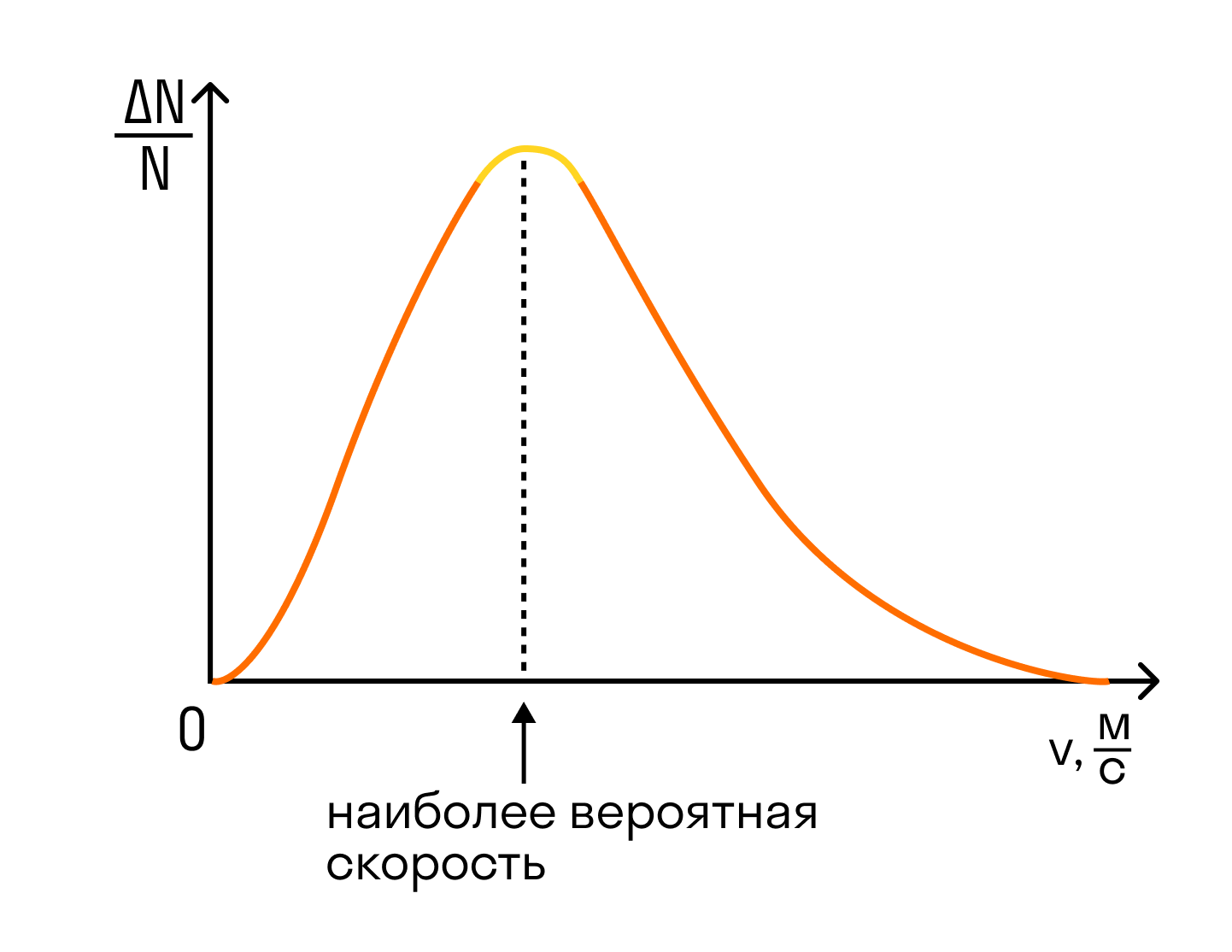
На графике показано распределение Максвелла — то, как молекулы распределяются по скоростям. Судя по графику, большинство молекул движутся со средним значением скорости. Хотя есть и быстрые, и медленные молекулы, просто их значительно меньше.
Но наш газ идеальный, а в идеальном газе случаются чудеса. Одно из таких чудес — то, что все молекулы идеального газа двигаются с одинаковой скоростью. Эта скорость называется средней квадратичной.
Средняя квадратичная скорость
vср. кв. — средняя квадратичная скорость [м/с]
v1, v2, vn — скорости разных молекул [м/с]
N — количество молекул [—]
Попробуйте курсы подготовки к ЕГЭ по физике с опытным преподавателем в онлайн-школе Skysmart!
Давление идеального газа
Молекулы газа беспорядочно движутся. Во время движения они сталкиваются друг с другом, а также со стенками сосуда, в котором этот газ находится. Поскольку молекул много, ударов тоже много.
Например, в комнате, в которой вы сейчас находитесь, за одну секунду на каждый квадратный сантиметр молекулы воздуха наносят столько ударов, что их количество выражается двадцатитрехзначным числом.
Хотя сила удара отдельной молекулы мала, действие всех молекул на стенки сосуда приводит к значительному давлению. Представьте, что комар пытается толкать машину — она не сдвинется с места. Но если за работу возьмется пара сотен миллионов комаров, то машину получится сдвинуть.
Эксперимент
Чтобы смоделировать давление газа, возьмите песок и лист бумаги, зажатый между двумя книгами. Песчинки будут выступать в роли молекул газа, а лист — в роли сосуда, в котором этот газ находится. Когда вы начинаете сыпать песок на лист бумаги, бумага отклоняется под воздействием множества песчинок. Так же и молекулы газа оказывают давление на стенки сосуда, в котором находятся.
Зависимость давления от других величин
Зависимость давления от объема
В механике есть формула давления, которая показывает, что давление прямо пропорционально силе и обратно пропорционально площади, на которую эта сила оказывается.
Давление
p = F/S
F — сила [Н]
S — площадь [м 2 ]
То есть если наши двести миллионов комаров будут толкать легковую машину, они распределятся по меньшей площади, чем если бы толкали грузовой автомобиль, — просто потому, что легковушка меньше грузовика. Из формулы давления следует, что давление на легковой автомобиль будет больше из-за его меньшей площади.
Рассмотрим аналогичный пример с двумя сосудами разной площади.
Давление в левом сосуде будет больше, чем во втором, потому что его площадь меньше. А раз меньше площадь сосуда, то меньше и его объем. Значит, давление зависит от объема следующим образом: чем больше объем, тем меньше давление, и наоборот.
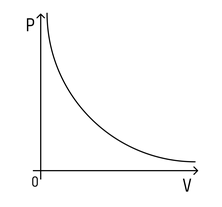
При этом зависимость будет не линейная, а примет вот такой вид (при условии, что температура постоянна):
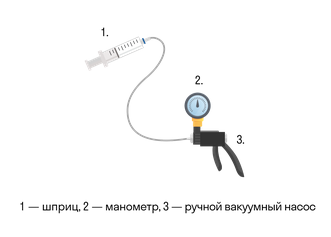
Зависимость давления от объема называется законом Бойля-Мариотта. Она экспериментально проверяется с помощью такой установки:
Объем шприца увеличивают с помощью насоса, а манометр измеряет давление. Эксперимент показывает, что при увеличении объема давление действительно уменьшается.
Зависимость давления от температуры
Рассмотрим зависимость давления газа от температуры при условии неизменного объема определенной массы газа. Исследования в этой области впервые провел французский изобретатель Жак Шарль в XVIII веке.
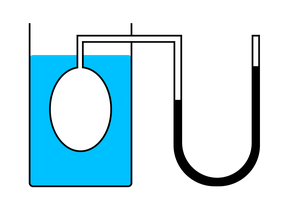
В ходе эксперимента газ нагревали в большой колбе, соединенной с ртутным манометром в виде узкой изогнутой трубки. Незначительным увеличением объема колбы при нагревании можно пренебречь, как и столь же незначительным изменением объема при смещении ртути в узкой манометрической трубке. Таким образом, объем газа можно считать неизменным.
Подогревая воду в сосуде, окружающем колбу, ученый измерял температуру газа термометром, а давление — манометром.
Эксперимент показал, что давление газа увеличивается с увеличением температуры. Это связано с тем, что при нагревании молекулы газа движутся быстрее, из-за чего чаще ударяются о стенки сосуда.
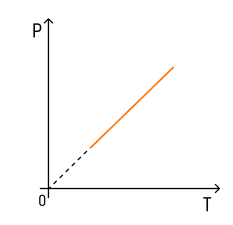
С температурой все проще. Зависимость давления от температуры при постоянных объеме и массе будет линейной:
Эта зависимость называется законом Шарля в честь ученого, открывшего ее.
Основное уравнение МКТ
Основная задача молекулярно-кинетической теории газа заключается в том, чтобы установить соотношение между давлением газа и его микроскопическими параметрами: массой молекул, их средней скоростью и концентрацией. Это соотношение называется основным уравнением молекулярно-кинетической теории газа или кратко — основным уравнением МКТ.
В основе молекулярно-кинетической теории лежат три положения.
Все вещества образованы из мельчайших частиц — молекул, которые состоят из атомов.
Молекулы химического вещества могут быть простыми и сложными, то есть состоять из одного или нескольких атомов. Молекулы и атомы представляют собой электрически нейтральные частицы. При определенных условиях молекулы и атомы могут приобретать дополнительный электрический заряд и превращаться в положительные или отрицательные ионы.
Атомы и молекулы находятся в непрерывном хаотическом движении.
Частицы взаимодействуют друг с другом силами, которые имеют электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало.
Мы уже выяснили, что причина давления газа на стенки — это удары молекул. Давление напрямую зависит от количества молекул — чем их больше, тем больше ударов о стенки и тем больше давление. А количество молекул в единице объема — это концентрация. Значит, давление газа зависит от концентрации.
Также давление пропорционально квадрату скорости, так как чем больше скорость молекулы, тем чаще она бьется о стенку сосуда. Расчеты показывают, что основное уравнение молекулярно-кинетической теории для идеального газа имеет следующий вид.
Основное уравнение МКТ
p = nkT
p — давление газа [Па]
n — концентрация [м −3 ]
T — температура газа [К]
m 0 — масса одной молекулы [кг]
v — средняя квадратичная скорость [м/с]
Коэффициент 1/3 обусловлен трехмерностью пространства: во время хаотического движения молекул все три направления равноправны.
Важный нюанс: средняя квадратичная скорость сама по себе не в квадрате! Ее формула указана выше, а в основном уравнении МКТ (да и не только в нем) она возведена в квадрат. Это значит, что формулу средней квадратичной скорости нужно подставлять не вместо v 2 , а вместо v — и потом уже возводить эту формулу в квадрат. Это часто провоцирует путаницу.
Мы знаем, что кинетическая энергия вычисляется по следующей формуле:
Кинетическая энергия
Ек = mv 2 /2
Ек — кинетическая энергия [Дж]
m — масса тела [кг]
v — скорость [м/с]
Для молекулы газа формула примет вид:
Средняя кинетическая энергия поступательного движения молекулы
Ек — средняя кинетическая энергия поступательного движения молекулы [Дж]
m0 — масса молекулы [кг]
v — скорость молекулы [м/с]
Из этой формулы можно выразить m0v 2 и подставить в основное уравнение МКТ. Подставим и получим, что давление идеального газа пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы.
Основное уравнение МКТ
p — давление газа [Па]
n — концентрация [м −3 ]
E — средняя кинетическая энергия поступательного движения молекулы [Дж]
Хранение и транспортировка газов
Если нужно перевезти значительное количество газа из одного места в другое или если газ необходимо длительно хранить, его помещают в специальные прочные металлические сосуды. Из-за того, что при уменьшении объема увеличивается давление, газ можно закачать в небольшой баллон, но он должен быть очень прочным.
Сосуды, предназначенные для транспортировки газов, выдерживают высокие давления. Поэтому с помощью специальных насосов (компрессоров) туда можно закачать значительные массы газа, которые в обычных условиях занимали бы в сотни раз больший объем.
Поскольку давление газов в баллонах даже при комнатной температуре очень велико, их ни в коем случае нельзя нагревать. Например, держать под прямыми лучами солнца или пытаться сделать в них отверстие — даже после использования.
http://infourok.ru/urok-fiziki-v-10-klasse-osnovnoe-uravnenie-molekulyarno-kineticheskoj-teorii-gazov-5162901.html
http://skysmart.ru/articles/physics/idealnyj-gaz