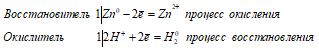Фторид натрия: способы получения и химические свойства
Фторид натрия — соль щелочного металла натрия и плавиковой кислоты. Белое вещество, плавится без разложения. Умеренно растворяется в воде (гидролиз по аниону), растворимость мало зависит от температуры.
Относительная молекулярная масса Mr = 41,99; относительная плотность тв. и ж. вещества d = 2,558; tпл = 997º C;
Способ получения
1. Фторид натрия можно получить путем взаимодействия при комнатой температуре натрия и фтора:
2Na + F2 = 2NaF
2. В результате взаимодействия разбавленной плавиковой кислоты и гидроксида натрия, образуется фторид натрия и вода:
NaOH + HF = NaF + H2O
Качественная реакция
Качественная реакция на фторид натрия — взаимодействие его с хлоридом кальция, в результате реакции происходит выпадение белого осадка:
1. При взаимодействии с хлоридом кальция , фторид натрия образует фторид кальция и хлорид натрия:
2NaF + CaCl2 → 2NaCl + CaF2↓
Химические свойства
1. Фторид натрия вступает в реакцию со сложными веществами :
1.1. Фторид натрия вступает во взаимодействие с концентрированными кислотами .
При кипении в результате взаимодействия с концентрированной серной кислотой фторид натрия образует сульфат натрия и газ фтороводород:
1.2. В реакции с насыщенным гидроксидом лития фторид натрия образует гидроксид натрия и фторид лития:
Гидролиз фторида натрия
NaF — соль образованная сильным основанием и слабой кислотой, поэтому реакция гидролиза протекает по аниону.
Молекулярное уравнение
NaF + HOH ⇄ HF + NaOH
Полное ионное уравнение
Na + + F — + HOH ⇄ HF + Na + + OH —
Сокращенное (краткое) ионное уравнение
F — + HOH ⇄ HF + OH —
Среда и pH раствора фторида натрия
В результате гидролиза образовались гидроксид-ионы (OH — ), поэтому раствор имеет щелочную среду (pH > 7).
Химимческие и физические свойства фтороводорода и фторидов металлов
Задача 819.
В каких сосудах хранят водный раствор фтороводорода? Как называют такой раствор?
Решение:
Раствор фтороводорода в воде называют «плавиковой кислотой». Это название происходит от плавикового шпата – основного сырья для получения HF. Замечательным свойством фтороводорода и плавиковой кислоты является их способность взаимодействовать с оксидом кремния (IV), входящим в состав стекла, в результате чего образуется газообразный фторид фтора SiF4:
В растворе плавиковой кислоты выделения фторида кремния не происходит, так как он взаимодействует с молекулами HF c образованием хорошо растворимой комплексной кремнефтороводородной кислоты:
или уравнение реакции в общем виде:
Ввиду того, что Фтороводород разрушает стекло, поэтому в лаборатории его хранят в сосудах из свинца или стеклянных сосудах, покрытых изнутри слоем парафина, а также в сосудах из специальных сортов пластмасс.
Задача 820.
Какова реакция среды в водных растворах фторида натрия, фторида аммония, фторида кремния?
Решение:
а) Фторид натрия NaF – соль сильного основания (NaOH) и слабой кислоты (HF) гидролизуется по аниону:
NaF ↔ Na + + F — ;
F — + H2O ↔ HF + OH —
или в молекулярной форме:
NaF + H2O ↔ F + NaOH
В результате гидролиза в растворе появляется некоторый избыток ионов ОН-, которые придают раствору щелочную реакцию, рН > 7.
б) Фторид натрия NH4F – соль слабого основания (NH4OH) и слабой кислоты (HF) гидролизуется как по катиону, так и по аниону:
NH4F ↔ NH4 + + F — ;
NH4 + + H2O ↔ NH4OH +Н + ;
F — + H2O ↔ HF + OH — .
или в молекулярной форме:
NaF + H2O ↔ HF + NaOH
В процессе гидролиза NH4F в растворе образуются слабые электролиты (NH4OH и HF), а также ионы Н + и ионы ОН — , которые соединяясь образуют воду
(Н + + ОН — ↔ Н2О). При гидролизе соли, образованной слабой кислотой и слабым основанием, реакция раствора зависит от относительной силы кислоты и основания, образующих данную соль. Если KD(кислота) = KD(основание), то катион и анион гидролизуется в равной степени и реакция раствора будет нейтральной; если KD(кислота) > KDоснование), то катион соли гидролизуется в большей степени, чем анион, так что концентрация ионов Н + в растворе будет больше, чем ионов ОН — и реакция среды будет слабокислой; наконец, если KD(кислота) — .
Так как KD(NH4OH) = 1,79 . 10 -8 . 10 -4 , то гидролиз катиона NH4 + будет преобладать над гидролизом аниона F — , значит, в растворе соли будет наблюдаться некоторый избыток ионов водорода Н + , что придаст раствору слабокислотную среду, (рН > 7 или рН = 7).
в) Фторид кремния SiF4 в водных растворах подвергается гидролизу, в результате которого образуется фтористоводородная кислота (НF) и кремниевая кислота (H2SiO3):
Образующийся фтороводород взаимодействует SiF4. При этом получается гексафторкремниевая (или кремнефтористоводородная) кислота:
Суммарный процесс можно выразить уравнением:
В результате гидролиза фторида кремния образуются кислоты, поэтому реакция раствора будет кислой, рН
Задача 821.
Могут ли галогеноводороды в каких-либо реакциях играть роль окислителя? Дать мотивированный ответ.
Решение:
Поскольку галогенид-ионы не способны присоединять электроны, то в реакциях окисления-восстановления они могут играть только роль восстановителей, за исключением ионов F-, а ионы водорода способны присоединять электроны. Поэтому галогеноводороды за счёт ионов Н + могут играть роль окислителя. Например, в реакциях с металлами ионы водорода, входящие в состав галогеноводорода, восстанавливаются последними до свободного водорода. При этом галгеноводороды могут реагировать только с металлами, стоящими в ряду напряжений до водорода, а точнее со всеми металлами, имеющими отрицательные стандартные потенциалы, Так цинк вытесняет водород из раствора соляной кислоты:
Электронные уравнения полуреакций:
Zn 0 + 2H + ↔ Zn 2+ + H2O;
К реакциям, в которых галогеноводороды играют роль окислителя, относятся реакции термической диссоциации:
Задача 822.
Действием каких галогенов можно выделить свободный бром из растворов: а) бромида калия; б) бромата калия? Дать мотивированный ответ, используя данные таблицы стандартных электродных потенциалов.
Решение:
Электродный потенциал системы: Br2 + 2 

а) В бромиде калия степень окисления брома равна -1, поэтому бром в KBr только восстановителем, В растворе бромида калия бром может быть вытеснен окислителем, электродный потенциал которого значительно больше, чем у KBr. Так как электродный потенциал системы Cl2 + 2 



б) В бромате калия KBrO3 степень окисления брома равна +5, поэтому он будет играть роль окислителя. Значит, электродный потенциал галогена, который вытеснит бром из бромата калия, должен быть меньше. Так как электродные потенциалы системы Г2 + 10 
http://chemer.ru/services/hydrolysis/salts/NaF
http://buzani.ru/zadachi/khimiya-glinka/1270-ftoridy-ftorovodorod-zadachi-819-822