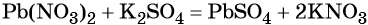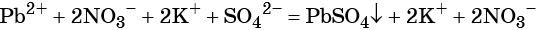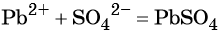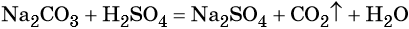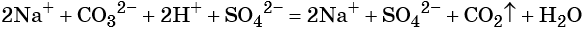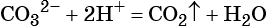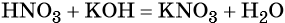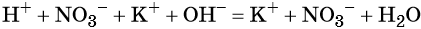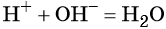Ионное уравнение серной кислоты и бромида кальция
Из предложенного перечня веществ выберите две соли, между которыми возможна реакция ионного обмена, приводящая к выпадению осадка. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
Дан следующий перечень веществ: нитрат калия, гидрофосфат аммония, серная кислота, медь, бромид кальция, перманганат калия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми которыми окислительно-восстановительная реакция протекает с выделением бурого газа, при этом выпадение осадка не наблюдается. Запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.
Для начала запишем молекулярные формулы данных веществ:
1) Уравнение реакции:
2) Электронный баланс:
2 | →
1 | →
3) Окислитель , восстановитель
Задачи 30 и 31 из реального ЕГЭ по химии
Задания 30 и 31 из реального ЕГЭ по химии-2021 — ответы и решения, все задачи на окислительно-восстановительную реакцию и реакции ионного обмена из реального экзамена ЕГЭ по химии, задания 32 из реального ЕГЭ 2021 (основная волна и резервные дни — 30 мая 2021 года) с текстовыми решениями и ответами.
| Выдержка из формулировки каждого варианта 30 задания: «В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель.» Выдержка из формулировки каждого варианта 31 задания: «Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.» Ниже приведены перечни веществ, а также дополнительные условия, которые были указаны в соответствующем варианте 30 и 31 задания. 1) Если вещество растворимо в воде, то допустимо использование водного раствора этого вещества. 2) Если концентрация кислоты указана, то следует использовать кислоту указанной концентрации. 3) Если концентрация кислоты не указана, то можно использовать и разваленную и концентрированную кислоту. |
1. Сульфид меди(II), гидросульфат калия, гидроксид бария, фосфин, гидроксид алюминия, азотная кислота.
Задание 30. Из предложенного перечня веществ выберите те, которые вступают в окислительно-восстановительную реакцию с образованием бесцветного раствора. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня веществ выберите те, между которыми реакция ионного обмена протекает без видимых признаков. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
1 | P -3 — 8e → P +5
8 | N +5 + 1e → N +4
Азот в степени окисления +5 (или азотная кислота) является окислителем.
Фосфор в степени окисления -3 (или фосфин) является восстановителем.
Ba 2+ + 2OH — + 2H + + 2NO3 — = Ba 2+ + 2NO3 — + 2H2O
2. Гидрокарбонат калия, нитрат алюминия, оксид фосфора(V), азотная кислота, сульфид меди(II), гидроксид бария.
Задание 30. Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием окрашенного раствора. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите кислую соль и вещество, между которыми протекает реакция ионного обмена с образованием осадка и выделением газа. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
1 | S -2 — 8e → S +6
Азот в степени окисления +5 (или азотная кислота) является окислителем .
Сера в степени окисления -2 (или сульфид меди (II)) является восстановителем.
3. Оксид серы(IV), перманганат калия, гидроксид магния, бромоводородная кислота, аммиак, гидроксид железа(III).
Задание 30. Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием в растворе двух солей и кислоты. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите вещества, между которыми протекает реакция ионного обмена и происходит растворение белого осадка. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
2 | Mn +7 + 5e → Mn +2
5 | S +4 — 2e → S +6
Марганец в степени окисления +7 (или перманганат калия) является окислителем
Сера в степени окисления +4 (или оксид серы (IV)) является восстановителем
Mg(OH)2 + 2H + + 2Br — = Mg 2+ + 2Br — + 2H2O
4. Перманганат натрия, нитрит натрия, гидроксид натрия, гидрокарбонат бария, серная кислота, гидрокарбонат магния.
Задание 30. Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием зеленого раствора и без образования осадка. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите вещества, между которыми реакция ионного обмена протекает с выделением газа и без образования осадка. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
2 | Mn +7 + 1e → Mn +6
1 | N +3 — 2e → N +5
Марганец в степени окисления +7 (или перманганат натрия) является окислителем.
Азот в степени окисления +3 (или нитрит натрия) является восстановителем.
5. Аммиак, перманганат калия, гидросульфат лития, нитрат стронция, иод, сульфит натрия.
Задание 30. Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием нерастворимого вещества и без выделения газа. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите кислую соль и вещество, между которыми протекает реакция ионного обмена с образованием осадка. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
2 | Mn +7 + 3e → Mn +4
3 | S +4 — 2e → S +6
Марганец в степени окисления + 7 (или перманганат калия) является окислителем
Сера в степени окисления + 4 (или сульфит натрия) является восстановителем
Li + + HSO4 — + Sr 2+ + 2NO3 — = SrSO4 + Li + + H + + 2NO3 —
6. Гидрофосфат калия, сульфит кальция, перманганат калия, хлороводород, гидроксид железа(III), нитрат марганца(II).
Задание 30. Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием осадка. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите кислую соль и вещество, между которыми протекает реакция ионного обмена без видимых признаков. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
2 | Mn +7 + 3e → Mn +4
3 | S +4 — 2e → S +6
Марганец в степени окисления + 7 (или перманганат калия) является окислителем
Сера в степени окисления + 4 (или сульфит кальция) является восстановителем
2K + + HPO4 2- + 2H + + 2Cl — = 2K + + 2Cl — + H3PO4
7. Сероводород, карбонат аммония, сульфат железа(II), дихромат калия, серная кислота, хлорид натрия.
Задание 30. Из предложенного перечня выберите вещества, между которыми в растворе протекает окислительно-восстановительная реакция с образованием трех солей. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите два сильных электролита, между которыми протекает реакция ионного обмена с образованием осадка. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
1 | Cr +6 + 3e → Cr +3
3 | Fe +2 — e → Fe +3
Хром в степени окисления + 6 (или дихромат калия) является окислителем
Железо в степени окисления + 2 (или сульфат железа (II)) является восстановителем
8. Бромид кальция, гидрофосфат аммония, перманганат калия, серная кислота, нитрат калия, медь.
Задание 30. Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием бурого газа и не сопровождается выпадением осадка. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите две соли, между которыми протекает реакция ионного обмена с образованием осадка. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
1 | Cu 0 — 2e → Cu +2
Азот в степени окисления + 5 (или нитрат калия) является окислителем
Медь в степени окисления 0 является восстановителем
Ca 2 + + 2Br — + 2NH4 + + HPO4 2- = CaHPO4 + 2NH4 + + 2Br —
9. Бромоводород, гидросульфат калия, перманганат калия, графит, нитрат серебра, ацетат бария.
Задание 30. Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием простого вещества. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите две соли, между которыми протекает реакция ионного обмена с образованием белого осадка. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
2 | Mn +7 + 5e → Mn +2
5 | 2Br — — 2e → Br2 0
Марганец в степени окисления + 7 (или перманганат калия) является окислителем
Бром в степени окисления -1 (или бромоводород) является восстановителем
Ba 2 + + 2CH3COO — + K + + HSO4 — = BaSO4 + CH3COO — + K + + CH3COOH
10. Оксид хрома(III), дихромат аммония, гидрокарбонат натрия, графит, хлорид железа(III), серная кислота.
Задание 30. Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием двух кислотных оксидов. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите две соли, между которыми протекает реакция ионного обмена с образованием осадка и выделением газа. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
1 | C 0 — 4e → C +4
2 | S +6 + 2e → S +4
Сера в степени окисления + 6 (или серная кислота) является окислителем
Углерод в степени окисления 0 является восстановителем
Fe 3 + + 3Cl — + 3Na + + 3HCO3 — = Fe(OH)3 + 3CO2 + 3Na + + 3Cl —
11. Оксид серы(IV), гидроксокарбонат меди(II), перманганат калия, дигидрофосфат натрия, аммиак, гидроксид калия.
Задание 30. Из предложенного перечня выберите вещества, окислительно-восстановительная реакция между которыми протекает с образованием осадка и выделением газа. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите кислую соль и вещество, которое вступает с этой кислой солью в реакцию ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
1 | 2N -3 — 6e → N2 0
2 | Mn +7 + 3e → Mn +4
Марганец в степени окисления + 7 (или перманганат калия) является окислителем
Азот в степени окисления -3 (или аммиак) является восстановителем
3Na + + 3H2PO4 2- + 6K + + 6OH — = 6K + + 2PO4 3- + 3Na + + PO4 3- + 6H2O
12. Оксид хрома(VI), хлорид железа(II), азотная кислота, аммиак, иод, фторид аммония.
Задание 30. Из предложенного перечня выберите вещества, между которыми окислительно-восстановительная реакция протекает с образованием кислоты. При этом одна молекула восстановителя . отдает десять электронов. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите два сильных электролита, между которыми протекает реакция ионного обмена без видимых признаков. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
1 | I2 0 — 10e → 2I —
10 | N +5 + 1e → N +4
Азот в степени окисления +5 (или азотная кислота) является окислителем
Йод в степени окисления 0 является восстановителем
13. Оксид серы(IV), фосфин, аммиак, дигидрофосфат натрия, пероксид натрия, гидроксид натрия.
Задание 30. Из предложенного перечня выберите вещества, между которыми окислительно-восстановительная реакция протекает с образованием щелочи и выделением газа. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите кислую соль и вещество, между которыми протекает реакция ионного обмена с образованием средней соли. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
1 | 2N -3 — 6e → N2 0
6 | O -1 + 1e → O -2
Азот в степени окисления -3 (или аммиак) является восстановителем
Кислород в степени окисления -1 (или пероксид натрия) является окислителем
14. Серная кислота, гидросульфат аммония, фосфин, сульфид меди(II), гидроксид бария, гидроксид хрома(III).
Задание 30. Из предложенного перечня выберите вещества, между которыми окислительно-восстановительная реакция протекает с образованием бесцветного раствора кислоты. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите вещества, между которыми протекает реакция ионного обмена с образованием окрашенного раствора и без выделения газа. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
1 | P -3 — 8e → P +5
4 | S +6 + 2e → S +4
Фосфор в степени окисления -3 (или фосфин) является восстановителем
Сера в степени окисления +6 (или серная кислота) является окислителем
15. Бром, нитрат бария, гидроксид хрома(III), гидрокарбонат калия, оксид серы(IV), нитрат алюминия.
Задание 30. Из предложенного перечня выберите вещества, между которыми окислительно-восстановительная реакция протекает в растворе с образованием двух кислот. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций с участием выбранных веществ. Составьте электронный баланс, укажите окислитель и восстановитель
Задание 31. Их предложенного перечня выберите вещества, между которыми протекает реакция ионного обмена с образованием осадка и выделением газа. Запишите молекулярное, полное и сокращённое ионное уравнения реакции с участием выбранных веществ.
1 | S +4 — 2e → S +6
1 | Br2 0 + 2e → 2Br —
Фосфор в степени окисления -3 (или фосфин) является восстановителем
Сера в степени окисления +6 (или серная кислота) является окислителем
Реакции ионного обмена и условия их осуществления
Реакциями ионного обмена называют химические реакции, которые протекают между ионами без изменения степеней окисления элементов и приводят к обмену составных частей реагентов.
Уравнения обменных реакций записывают в молекулярной форме (с указанием формул всех реагирующих веществ со стехиометрическими коэффициентами); в полной ионной форме (с указанием всех существующих в растворе ионов) и в сокращённой ионной форме (с указанием только тех ионов, которые непосредственно взаимодействуют между собой). При написании уравнений реакций в ионной форме формулы малодиссоциирующих веществ (слабых электролитов) записывают в молекулярной форме.
Уравнения реакций обмена в водных растворах электролитов составляют так.
- Записывают в левой части уравнения все формулы веществ, вступивших в реакцию, в молекулярной или ионной форме.
- Руководствуясь знаниями физико-химических свойств реагентов и таблицами растворимости веществ, составляют формулы продуктов реакции.
- Проверяют число атомов каждого элемента в обеих частях уравнения и определяют необходимые стехиометрические коэффициенты перед формулами.
Реакции ионного обмена в растворах электролитов протекают практически необратимо и до конца, если в качестве продуктов образуются осадки (малорастворимые вещества), газы (легколетучие вещества), слабые электролиты (малодиссоциированные соединения) и комплексные ионы.
Если при взаимодействии растворов электролитов не образуется ни одно из указанных видов соединений, химическое взаимодействие практически не происходит.
Уравнения обменных реакций можно записать в молекулярной форме, полной ионной форме, с указанием всех существующих в растворе ионов и в сокращённой ионной форме, которая, собственно, и выражает взаимодействие ионов. Следует отметить, что при написании уравнений реакций в ионной форме малодиссоциирующие вещества (слабые электролиты) записывают в молекулярной форме.
Пример 1. Реакция между нитратом свинца и сульфатом калия. В результате этой реакции образуется нерастворимый сульфат свинца и выделяется растворимый нитрат калия:
(полная ионно-молекулярная форма),
(сокращённая ионно-молекулярная форма).
Пример 2. Взаимодействие карбоната натрия с серной кислотой. При этом выделяется углекислый газ и вода, а в растворе остаются катионы натрия и сульфат-ионы:
(полная ионно-молекулярная форма),
(сокращённая ионно-молекулярная форма).
Пример 3. Реакция между азотной кислотой и едким калием. В результате данной реакции образуется малодиссоциированное соединение — вода и в растворе остаются катионы калия и нитрат-ионы:
(полная ионно-молекулярная форма),
(сокращённая ионно-молекулярная форма).
Тренировочные задания
1. Осадок образуется при взаимодействии водных растворов
2. Газ выделяется при взаимодействии водных растворов
3. Краткое ионное уравнение H + + OH – = H2O описывает взаимодействие
1) гидроксида кальция и фосфорной кислоты
2) гидроксида лития и фосфорной кислоты
3) гидроксида натрия и бромоводородной кислоты
4) гидроксида алюминия и бромоводородной кислоты
4. Краткое ионное уравнение 3Ba 2+ + 2PO4 3– = Ba3(PO4)2↓ описывает взаимодействие
1) карбоната бария и фосфорной кислоты
2) карбоната бария и фосфата натрия
3) хлорида бария и фосфорной кислоты
4) хлорида бария и фосфата натрия
5. Краткое ионное уравнение Ba 2+ + SO4 2– = BaSO4↓ описывает взаимодействие
1) хлорида бария и сульфата натрия
2) хлорида бария и сернистой кислоты
3) гидроксида бария и сульфата натрия
4) гидроксида бария и серной кислоты
6. Краткое ионное уравнение Ag + + Cl – = AgCl↓ описывает взаимодействие
1) хлорида кальция и бромида серебра
2) фосфата серебра и соляной кислоты
3) карбоната серебра и хлорида натрия
4) нитрата серебра и хлорида калия
7. Краткое ионное уравнение H + + OH – = H2O отвечает взаимодействию
1) азотной кислоты и гидроксида железа (III)
2) бромоводородной кислоты и гидроксида натрия
3) азотной кислоты и гидроксида меди
4) сернистой кислоты и гидроксида кальция
8. Краткое ионное уравнение 2Н + + S 2– = Н2S↑ отвечает взаимодействию
1) соляной кислоты и сульфида железа (II)
2) сернистой кислоты и сульфида калия
3) азотной кислоты и сульфида меди
4) азотной кислоты и сульфида натрия
9. Краткое ионное уравнение 2Н + + CO3 2– = CO2↑ + H2O отвечает взаимодействию
1) соляной кислоты и карбоната кальция
2) сернистой кислоты и карбоната бария
3) азотной кислоты и карбоната калия
4) серной кислоты и карбоната бария
10. Краткое ионное уравнение 2Н + + CaCO3 = Ca 2+ + CO2↑ + H2O отвечает взаимодействию
1) соляной кислоты и карбоната кальция
2) сернистой кислоты и карбоната кальция
3) фосфорной кислоты и карбоната кальция
4) серной кислоты и карбоната кальция
11. Краткое ионное уравнение Al 3+ + 3OH – = Al(OH)3↓ отвечает взаимодействию
1) сульфата алюминия и гидроксида кальция
2) сульфата алюминия и гидроксида бария
3) сульфата алюминия и гидроксида меди
4) сульфата алюминия и гидроксида натрия
12. Краткое и полное ионное уравнения совпадают для реакции
1) соляной кислоты и карбоната калия
2) уксусной кислоты и карбоната бария
3) уксусной кислоты и гидроксида калия
4) серной кислоты и гидроксида калия
13. Одновременно в растворе не могут существовать ионы
1) Ba 2+ , Fe 2+ , PO4 3– , CO3 2–
2) Ba 2+ , NO3 – , Cl – , K +
3) CH3COO – , Li + , Br – , Al3 +
4) Mg 2+ , Br – , K + , Cl –
14. Одновременно в растворе могут существовать ионы
1) Ba 2+ , Fe 2+ , PO4 3– , SO4 2–
2) Ba 2+ , SO4 2– , Ca 2+ , PO4 3–
3) Na + , Ba 2+ , NO3 – , Cl –
4) Mg 2+ , Ca 2+ , SO3 2– , CO3 2–
15. Образование осадка происходит при взаимодействии водных растворов
16. Образование газа происходит при взаимодействии водных растворов
1) сульфата калия и хлорида бария
2) гидроксида алюминия и серной кислоты
3) хлорида кальция и карбоната натрия
4) соляной кислоты и карбоната натрия
17. С выпадением осадка протекает реакция ионного обмена между растворами
1) нитрата натрия и фторида калия
2) хлорида алюминия и избытка гидроксида калия
3) нитрата серебра и фторида натрия
4) нитрата магния и гидроксида калия
18. С выделением газа протекает реакция ионного обмена между растворами
1) карбоната калия и бромоводородной кислоты
2) сульфата натрия и гидроксидом калия
3) нитрата серебра и бромида цинка
4) нитрата алюминия и гидроксида бария
19. С выделением газа протекает реакция ионного обмена между растворами
1) гидроксида бария и азотной кислоты
2) сульфата алюминия и нитрата бария
3) нитрата серебра и йодида лития
4) азотной кислотой и карбоната аммония
20. С выделением воды протекает реакция ионного обмена между растворами
1) нитрата меди и хлорида железа
2) гидрокарбоната натрия и гидроксида натрия
3) нитрата ртути и бромида лития
4) нитрата аммония и нитрита натрия
http://chemege.ru/real-ege-po-ximii-2021-30-31/
http://himi4ka.ru/ogje-2018-po-himii/urok-11-reakcii-ionnogo-obmena-i-uslovija-ih-osushhestvlenija.html