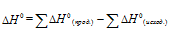Вычисление энтальпии образования вещества
Вычисление энтальпии образования озона из кислорода
Задача 6.
Исходя из энтальпий реакций окисления Аs2О3 кислородом и озоном:
Аs2О3 + О2 = Аs2О5; ∆Н 0 298х.р. = -271 кДж/моль;
3Аs2О3 + 2О3 = 3Аs2О5; ∆Н 0 298х.р. = -1096 кДж/моль, вычислите энтальпию образования озона из кислорода.
Решение:
Для решения задачи запишем оба уравнения реакций, умножим первое на третье и вычтем из него второе.
А если учесть, что фактическое уравнение реакции образования озона из кислорода имеет вид:
∆Н 0 (О3) = (283 кДж)/2 = 141,5 кДж.
1 Ответ: ∆Н 0 (О3) = 141,5 кДж.
Вычисление энтальпии образования ацетилена по реакции его сгорания
Задача 7.
При сгорании 1 литра С2Н2 (О°С и 760 мм рт. ст.) выделяется 58,02кДж тепла. Вычислить энтальпию образования ацетилена.
Решение:
В основе термохимических расчетов лежит закон Гесса (1840 г.): тепловой эффект реакции зависит только от природы и физического состояния исходных веществ и конечных продуктов, но не зависит от пути перехода.
В термохимических расчетах применяют чаще следствие из закона Гесса: тепловой эффект реакции (∆Hх.р.) равен сумме энтальпий образования ∆Hобр. продуктов реакции за вычетом суммы энтальпий образования исходных веществ с учетом стехиометрических коэффициентов:
Запишем термохимическое уравнение реакции:
Из условия задачи вытекает, что при сгорании 1 л ацетилена выделяется 58,02 кДж. тепла. Находим ∆Н 0 при сгорании 1 моля ацетилена (С2Н2), получим:
58,02 . 22,4 = 1299,65кДж тепла, т.е.∆Н 0 = -1299,65 кДж.
Отсюда можно записать:
Пользуясь табличными данными: ∆Н 0 (СО2(г) = -393,51; ∆Н 0 (Н2О(ж)) = -285,83) находим:
∆Н 0 (С2Н2) = 2(-393,51) + (-285,83) + 1299,65 = 226,8 кДж.
1 По табличным данным при 0 о С: ∆Н 0 (О3) = 144,457 кДж/моль. Можно отнести это на счет погрешностей при использовании данных для нормальных условий, т.е. при t = 20 — 25 o C.
Объясните, исходя из уравнения реакции горения метана, почему его используют как топливо?
Химия | 5 — 9 классы
Объясните, исходя из уравнения реакции горения метана, почему его используют как топливо?
Так как если загорится получится простая вода и углекислый газ.
А ещё он экологичный.
Пригорении не выделяется всяких вредных газов.
Так же выделяется энергия(экзотермическая реакция)
ну а ещё он дешевле нефти и газа).
Составить уравнение реакции горения метана и, применив следствие из закона Гесса, определить теплоту сгорания метана?
Составить уравнение реакции горения метана и, применив следствие из закона Гесса, определить теплоту сгорания метана.
Уравнение реакции горения метана уравнение реакции горения этилена?
Уравнение реакции горения метана уравнение реакции горения этилена.
Записать уравнения реакции горения метана?
Записать уравнения реакции горения метана.
Как исходя из метана получить аминоуксусную кислоту?
Как исходя из метана получить аминоуксусную кислоту?
Приведите уравнения реакций.
Сумма коэффициента уравнении реакции горения метана CH4 в кислороде равна?
Сумма коэффициента уравнении реакции горения метана CH4 в кислороде равна.
Записать уравнение реакции горения метана, этена, пропена, расставить коэффиценты?
Записать уравнение реакции горения метана, этена, пропена, расставить коэффиценты.
Напишите уравнения реакций с помощью которых можно получить уксусную кислоту исходя из метана?
Напишите уравнения реакций с помощью которых можно получить уксусную кислоту исходя из метана.
Ответьте пожалуйста ?
1)Составить уравнение реакций замещение метана.
2)Уравнение реакции горения этана.
Напишите схему реакции образования метана и горения метана, почему метан не взаимодействует с бромной водой и перманганатом калия?
Напишите схему реакции образования метана и горения метана, почему метан не взаимодействует с бромной водой и перманганатом калия.
! 60 баллов?
Составьте формулу гомолога метана, при горении которого образуется в пять раз больше углекислого газа, чем при горении метана.
Ответ подтвердите уравнениями реакций.
Вы перешли к вопросу Объясните, исходя из уравнения реакции горения метана, почему его используют как топливо?. Он относится к категории Химия, для 5 — 9 классов. Здесь размещен ответ по заданным параметрам. Если этот вариант ответа не полностью вас удовлетворяет, то с помощью автоматического умного поиска можно найти другие вопросы по этой же теме, в категории Химия. В случае если ответы на похожие вопросы не раскрывают в полном объеме необходимую информацию, то воспользуйтесь кнопкой в верхней части сайта и сформулируйте свой вопрос иначе. Также на этой странице вы сможете ознакомиться с вариантами ответов пользователей.
Ню = м / М = 108, 5 / 217(эт М) = 0, 5ню = v / vm, следовательно V = ню * вм = 0, 5 * 22, 4 = 11, 2.
Оксиген, азот и натрий ковалентный неполярный, все остальные полярные.
Ионная ионная металлическая ковалентная полярная ковалентная полярная ковалентная не полярная ковалентная не полярная.
1) 2Al + 6HCl — > 2AlCl3 + 3H2 / AlCl3 — соль 2) 2Li + 2HOH — > 2LiOH + H2 / LiOH — основание 2LiOH — > Li2O + H2O / Li2O — оксид ме (гидроксид лития особенный и способен к раздражению).
Я невпевнений але Ba(oh)2 + H2So4 = baso4 + h2o.
X1 = C2H2 X2 = C2Na2 X3 = CH3COOH.
Реакции есть на фотографии.
M(CO) = 50 * 56 / 100 = 28г M(CO) = 28г / моль nCO) = 28 / 28 = 1моль CuO + CO = Cu + CO2 nCuO : nCO = 1 : 1 n(CuO) = 1моль количество вещества оксида меди равно = 1моль.
Ответ никакая относительная площадь.
2P + 3Cl2 — — — — >2PCl3 p ^ < 3 + >\ : \ : \ : \ : \ : \ : 2 \ \ 2cl + 2e ^ <2>— > 2cl <> ^ < - >\ : \ : \ : \ : 3″ alt = » p ^ <0>— 3e ^ < - >— > p ^ < 3 + >\ : \ : \ : \ : \ : \ : 2 \ \ 2cl + 2e ^ <2>— > 2cl <> ^ < - >\ : \ : \ : \ : 3″ a..
Школе NET
Register
Do you already have an account? Login
Login
Don’t you have an account yet? Register
Newsletter
Submit to our newsletter to receive exclusive stories delivered to you inbox!
- Главная
- Вопросы & Ответы
- Вопрос 7492878
Пармезан Черница
Исходя из уравнения реакции горения углерода С О2 = СО2 393 кДж вычислите сколько теплоты выделится при сгорании 5 кг угля
http://himia.my-dict.ru/q/3263357_obasnite-ishoda-iz-uravnenia-reakcii-gorenia/
http://shkolenet.ru/QA/7492878/